Dimethylformamid

| |||
|
| |||
| Bezeichnungen | |||
|---|---|---|---|
| Bevorzugter IUPAC-Name
N,N-Dimethylformamid | |||
| Andere Bezeichnungen
Dimethylformamid
N,N-Dimethylmethanamid DMF | |||
| Bezeichner | |||
3D-Modell (JSmol)
|
|||
| 3DMet | |||
Beilstein-Referenz
|
605365 | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Arzneimittelbank | |||
| EC-Nummer |
| ||
| KEGG | |||
| MeSH | Dimethylformamid | ||
PubChem CID
|
|||
| RTECS-Nummer |
| ||
| UNII | |||
| UN-Nummer | 2265 | ||
InChI
| |||
SMILES
| |||
| Eigenschaften | |||
Chemische Formel
|
C3H7NO | ||
| Molare Masse | 73,095 g-mol-1 | ||
| Erscheinungsbild | Farblose Flüssigkeit | ||
| Geruch | fischig, ammoniakalisch | ||
| Dichte | 0,948 g/ml | ||
| Schmelzpunkt | -61 °C (-78 °F; 212 K) | ||
| Siedepunkt | 153 °C (307 °F; 426 K) | ||
Löslichkeit in Wasser
|
mischbar | ||
| log P | −0.829 | ||
| Dampfdruck | 516 Pa | ||
| Acidität (pKa) | -0,3 (für die konjugierte Säure) (H2O) | ||
| UV-vis (λmax) | 270 nm | ||
| Absorptionsgrad | 1.00 | ||
Brechungsindex (nD)
|
1,4305 (bei 20 °C) | ||
| Viskosität | 0,92 mPa s (bei 20 °C) | ||
| Struktur | |||
Dipolmoment
|
3.86 D | ||
| Thermochemie | |||
Wärmekapazität (C)
|
146,05 J/(K-mol) | ||
Std. Bildungsenthalpie
Bildung (ΔfH⦵298) |
-239,4 ± 1,2 kJ/mol | ||
Std. Bildungsenthalpie
Verbrennung (ΔcH⦵298) |
-1,9416 ± 0,0012 MJ/mol | ||
| Gefahren | |||
| GHS-Kennzeichnung: | |||
Piktogramme
|
  
| ||
Signalwort
|
Gefahr | ||
Gefahrenhinweise
|
H226, H312, H319, H332, H360 | ||
Sicherheitshinweise
|
P280, P305+P351+P338, P308+P313 | ||
| NFPA 704 (Feuerdiamant) | |||
| Flammpunkt | 58 °C (136 °F; 331 K) | ||
Selbstentzündung
temperatur |
445 °C (833 °F; 718 K) | ||
| Explosionsgrenzen | 2.2–15.2% | ||
Schwellengrenzwert (TLV)
|
30 mg/m (TWA) | ||
| Tödliche Dosis oder Konzentration (LD, LC): | |||
LD50 (mediane Dosis)
|
| ||
LC50 (mittlere Konzentration)
|
3092 ppm (Maus, 2 h) | ||
LCLo (niedrigste veröffentlichte)
|
5000 ppm (Ratte, 6 Std.) | ||
| NIOSH (US-Grenzwerte für die Gesundheit): | |||
PEL (Zulässig)
|
TWA 10 ppm (30 mg/m3) [Haut] | ||
REL (Empfohlen)
|
TWA 10 ppm (30 mg/m3) [Haut] | ||
IDLH (Unmittelbare Gefahr)
|
500 ppm | ||
| Verwandte Verbindungen | |||
Verwandte Alkanamide
|
| ||
Verwandte Verbindungen
|
| ||
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien in ihrem Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |||
Dimethylformamid ist eine organische Verbindung mit der Formel (CH3)2NC(O)H. Diese farblose Flüssigkeit wird üblicherweise als DMF abgekürzt (obwohl diese Abkürzung manchmal auch für Dimethylfuran oder Dimethylfumarat verwendet wird) und ist mit Wasser und den meisten organischen Flüssigkeiten mischbar. DMF ist ein gängiges Lösungsmittel für chemische Reaktionen. Dimethylformamid ist geruchlos, doch haben technisch hochwertige oder abgebaute Proben aufgrund von Verunreinigungen durch Dimethylamin oft einen fischigen Geruch. Verunreinigungen durch den Abbau von Dimethylamin können durch Durchperlen der Proben mit einem Inertgas wie Argon oder durch Beschallen der Proben unter reduziertem Druck entfernt werden. Wie sein Name schon sagt, ist es strukturell mit Formamid verwandt. DMF ist ein polares (hydrophiles) aprotisches Lösungsmittel mit einem hohen Siedepunkt. Es erleichtert Reaktionen, die polaren Mechanismen folgen, wie z. B. SN2-Reaktionen. ⓘ
Die Verwendung als Lösungsmittel für Polyacrylnitril, das dessen Verwendung als Kunstfaser ermöglichte (Orlon, Dralon u. a.), wurde 1941 von Herbert Rein bei IG Farben und 1944 unabhängig bei DuPont in den USA entdeckt. ⓘ
Struktur und Eigenschaften
Wie bei den meisten Amiden weisen die spektroskopischen Daten auf einen partiellen Doppelbindungscharakter der C-N- und C-O-Bindungen hin. So zeigt das Infrarotspektrum eine C=O-Streckfrequenz bei nur 1675 cm-1, während ein Keton bei 1700 cm-1 absorbieren würde. ⓘ
DMF ist ein klassisches Beispiel für ein fluxionales Molekül. ⓘ
Das 1H-NMR-Spektrum bei Raumtemperatur zeigt zwei Methylsignale, die auf eine behinderte Drehung um die (O)C-N-Bindung hindeuten. Bei Temperaturen nahe 100 °C zeigt das 500-MHz-NMR-Spektrum dieser Verbindung nur ein Signal für die Methylgruppen. ⓘ
DMF ist mit Wasser mischbar. Der Dampfdruck bei 20 °C beträgt 3,5 hPa. Aus einer experimentell bestimmten Gleichgewichtskonstante bei 25 °C lässt sich eine Konstante des Henry'schen Gesetzes von 7,47 × 10-5 hPa m3 mol-1 ableiten. Der Verteilungskoeffizient log POW wird mit -0,85 gemessen. Da die Dichte von DMF (0,95 g cm-3 bei 20 °C) mit der von Wasser vergleichbar ist, ist eine signifikante Flotation oder Schichtung in Oberflächengewässern im Falle von zufälligen Verlusten nicht zu erwarten. ⓘ

Reaktionen
DMF wird durch starke Säuren und Basen hydrolysiert, insbesondere bei erhöhten Temperaturen. Mit Natriumhydroxid wandelt sich DMF in Formiat und Dimethylamin um. DMF wird in der Nähe seines Siedepunkts dekarbonyliert, wobei Dimethylamin entsteht. Die Destillation wird daher unter vermindertem Druck bei niedrigeren Temperaturen durchgeführt. ⓘ
Eine der Hauptverwendungen von DMF in der organischen Synthese ist die Vilsmeier-Haack-Reaktion, die zur Formylierung von aromatischen Verbindungen verwendet wird. Dabei wird DMF zunächst in ein Chloriminium-Ion, [(CH3)2N=CH(Cl)]+, umgewandelt, das als Vilsmeier-Reagenz bekannt ist und Arene angreift. ⓘ
Lithiumorganische Verbindungen und Grignard-Reagenzien reagieren mit DMF nach Hydrolyse in einer nach Bouveault benannten Reaktion zu Aldehyden. ⓘ
Dimethylformamid bildet 1:1-Addukte mit einer Vielzahl von Lewis-Säuren wie der weichen Säure I2 und der harten Säure Phenol. Es wird als harte Lewis-Base eingestuft, und seine ECW-Modellbasenparameter sind EB= 2,19 und CB= 1,31. Ihre relative Donorstärke gegenüber einer Reihe von Säuren im Vergleich zu anderen Lewis-Basen lässt sich anhand von C-B-Diagrammen veranschaulichen. ⓘ
Herstellung
Die großtechnische Herstellung von DMF erfolgt auf zwei verschiedenen Wegen, nach einem einstufigen und einem zweistufigen Prozess. Bei der einstufigen Synthese wird Dimethylamin mit Kohlenmonoxid bei erhöhter Temperatur und erhöhtem Druck direkt zu DMF umgesetzt. Die Reaktion wird in der Flüssigphase mit Hilfe eines Katalysators (Natriumethanolat) durchgeführt:
Bei der zweistufigen Synthese wird die Umsetzung von Dimethylamin mit Ameisensäuremethylester durchgeführt, es entsteht Methanol als Kuppelprodukt:
Beide Synthesen verlaufen mit hohen Ausbeuten ohne die Bildung nennenswerter Nebenprodukte. Die Produktaufarbeitung erfolgt in beiden Fällen durch mehrstufige Destillation. ⓘ
DMF wurde erstmals 1893 von dem französischen Chemiker Albert Verley (8. Januar 1867 - 27. November 1959) durch Destillation einer Mischung aus Dimethylaminhydrochlorid und Kaliumformiat hergestellt. ⓘ
Obwohl derzeit nicht praktikabel, kann DMF aus überkritischem Kohlendioxid unter Verwendung von Katalysatoren auf Rutheniumbasis hergestellt werden. ⓘ
Anwendungen
DMF wird in erster Linie als Lösungsmittel mit niedriger Verdampfungsrate verwendet. DMF wird bei der Herstellung von Acrylfasern und Kunststoffen verwendet. Es wird auch als Lösungsmittel bei der Peptidkopplung für Pharmazeutika, bei der Entwicklung und Herstellung von Pestiziden und bei der Herstellung von Klebstoffen, Kunstleder, Fasern, Filmen und Oberflächenbeschichtungen verwendet. ⓘ
- Es wird als Reagenz in der Bouveault-Aldehydsynthese und in der Vilsmeier-Haack-Reaktion, einer weiteren nützlichen Methode zur Bildung von Aldehyden, verwendet.
- Es ist ein gängiges Lösungsmittel in der Heck-Reaktion.
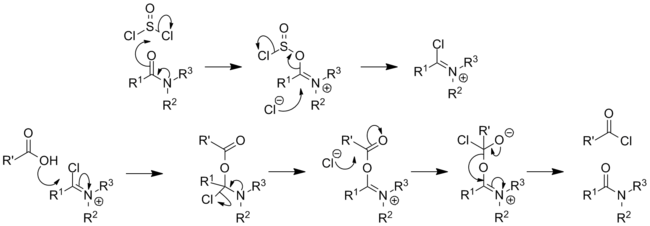
- Es ist auch ein gängiger Katalysator für die Synthese von Acylhalogeniden, insbesondere für die Synthese von Acylchloriden aus Carbonsäuren mit Oxalyl- oder Thionylchlorid. Der katalytische Mechanismus besteht in der reversiblen Bildung eines Imidoylchlorids (auch bekannt als "Vilsmeier-Reagenz"):
- DMF durchdringt die meisten Kunststoffe und lässt sie aufquellen. Aufgrund dieser Eigenschaft eignet sich DMF für die Festphasen-Peptidsynthese und als Bestandteil von Abbeizmitteln.
- DMF wird als Lösungsmittel zur Gewinnung von Olefinen wie 1,3-Butadien durch Extraktivdestillation verwendet.
- Es wird auch bei der Herstellung von Lösemittelfarbstoffen als wichtiger Rohstoff verwendet. Es wird bei der Reaktion verbraucht.
- Reines Acetylengas kann nicht verdichtet und gelagert werden, ohne dass Explosionsgefahr besteht. Industrielles Acetylen wird in Gegenwart von Dimethylformamid sicher verdichtet, das eine sichere, konzentrierte Lösung bildet. Die Hülle ist außerdem mit Agamassan gefüllt, was den Transport und die Verwendung sicher macht. ⓘ
Als billiges und gängiges Reagenz hat DMF viele Verwendungsmöglichkeiten in einem Forschungslabor.
- DMF eignet sich gut zum Trennen und Suspendieren von Kohlenstoffnanoröhrchen und wird vom NIST für die Verwendung in der Nahinfrarotspektroskopie dieser Röhrchen empfohlen.
- DMF kann als Standard in der Protonen-NMR-Spektroskopie verwendet werden und ermöglicht eine quantitative Bestimmung einer unbekannten Verbindung.
- Bei der Synthese von metallorganischen Verbindungen wird es als Quelle für Kohlenmonoxid-Liganden verwendet.
- DMF ist ein gängiges Lösungsmittel beim Elektrospinnen.
- DMF wird häufig für die solvothermische Synthese von metallorganischen Gerüsten verwendet.
- DMF-d7 in Gegenwart einer katalytischen Menge KOt-Bu unter Mikrowellenerhitzung ist ein Reagenz für die Deuterierung von polyaromatischen Kohlenwasserstoffen. ⓘ
Sicherheit
Reaktionen, die die Verwendung von Natriumhydrid in DMF als Lösungsmittel einschließen, sind in gewissem Maße gefährlich; es wurde über exotherme Zersetzungen bei Temperaturen von nur 26 °C berichtet. Im Labormaßstab wird jedes thermische Durchgehen (in der Regel) schnell bemerkt und mit einem Eisbad unter Kontrolle gebracht, und dies ist nach wie vor eine beliebte Reagenzienkombination. Im Technikumsmaßstab hingegen wurden mehrere Unfälle gemeldet. ⓘ
Am 20. Juni 2018 veröffentlichte die dänische Umweltschutzbehörde einen Artikel über die Verwendung von DMF in Squishies. Die Dichte der Verbindung in dem Spielzeug führte dazu, dass alle Squishies vom dänischen Markt genommen wurden. Es wurde empfohlen, alle Squishies über den Hausmüll zu entsorgen. ⓘ
Toxizität
Die akute LD50 (oral, Ratten und Mäuse) beträgt 2,2-7,55 g/kg. Die Gefährlichkeit von DMF wurde untersucht. ⓘ
Eigenschaften
Physikalische Eigenschaften
DMF ist eine farblose bis gelbliche, schwerflüchtige Flüssigkeit, die sich mit Wasser und vielen organischen Lösungsmitteln mischt. Bei Normaldruck siedet die Verbindung bei 153 °C. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 3,93068, B = 1337,716 und C = −82,648 im Temperaturbereich von 303 K bis 363 K. Wichtige thermodynamische Größen werden in der folgenden Tabelle gegeben:
| Eigenschaft | Typ | Wert [Einheit] | Bemerkungen |
|---|---|---|---|
| Standardbildungsenthalpie | ΔfH0liquid | −239,4 kJ·mol−1 | als Flüssigkeit |
| Verbrennungsenthalpie | ΔcH0liquid | −1941,6 kJ·mol−1 | als Flüssigkeit |
| Wärmekapazität | cp | 148,16 J·mol−1·K−1 (25 °C) 2,03 J·g−1·K−1 (25 °C) |
als Flüssigkeit |
| Kritische Temperatur | Tc | 649,6 K | |
| Kritische Dichte | ρc | 3,82 mol·l−1 | |
| Verdampfungsenthalpie | ΔVH0 ΔVH |
46,7 kJ·mol−1 39,409 kJ·mol−1 |
am Siedepunkt |
| Schmelzenthalpie | ΔFH | 8,95 kJ·mol−1 |
Die Temperaturabhängigkeit der Verdampfungsenthalpie lässt sich entsprechend der vereinfachten Watsongleichung ΔVH=A·(1−Tr)n (ΔVH in kJ/mol, Tr =(T/Tc) reduzierte Temperatur) mit A = 59,3545 kJ/mol, n = 0,381 und Tc = 647,0 K im Temperaturbereich zwischen 213 K und 647 K beschreiben. ⓘ
Die Verbindung bildet azeotrop siedende Gemische mit n-Heptan bei 97 °C bei einem Gehalt von 5 Ma% bzw. mit Ethylbenzol bei 134 °C mit einem Gehalt von 15 Ma%. Keine Azeotrope werden mit Wasser, Methanol, Ethanol, Benzol, Toluol, und Acetonitril gebildet. ⓘ
Chemische Eigenschaften
Das Amid zersetzt sich unter Licht und Hitzeeinwirkung zu Dimethylamin und Kohlenstoffmonoxid. Lösungen in Wasser sind hydrolysebeständig. Zusätze von Säuren oder Basen katalysieren den Zerfall in Ameisensäure und Dimethylamin. Als Lösungsmittel ist die Verbindung gegenüber einer Reihe von Stoffen nicht inert. Mit Stoffen wie Natriumhydrid, Natriumtetrahydroborat, Lithiumazid, Natrium, Thionylchlorid und Triethylaluminium treten heftige Reaktionen ein. Es reagiert auch mit halogenierten Kohlenwasserstoffen, wie Tetrachlorkohlenstoff. ⓘ
Sicherheitstechnische Kenngrößen
Dimethylformamid bildet entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von 58 °C. Der Explosionsbereich liegt zwischen 2,2 Vol.‑% (70 g/m³) als untere Explosionsgrenze (UEG) und 16 Vol.‑% (500 g/m³) als obere Explosionsgrenze (OEG). Hier ergibt sich ein oberer Explosionspunkt von 51 °C. Der maximale Explosionsdruck beträgt 7,2 bar. Die Grenzspaltweite wurde mit 1,02 mm bestimmt. Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA. Die Zündtemperatur beträgt 440 °C. Der Stoff fällt somit in die Temperaturklasse T2. ⓘ
Sicherheitshinweise
Sowohl nach akuter, als auch nach chronischer Einwirkung, kann es zu einer Leberzellschädigung kommen. Histologisch zeigen sich dann mikrovesikuläre Fetteinlagerungen (Fettleber) und Veränderungen des Lebergewebes ohne ausgeprägte Entzündungen. ⓘ
DMF ist in Anlage 6 zu Nummer 30 des Anhangs XVII der REACH-Verordnung (EG) Nr. 1907/2006 als fortpflanzungsgefährdend der Kategorie 2 gelistet. ⓘ