Aluminiumchlorid
 Aluminiumtrichloridhexahydrat, (oben) rein und (unten) verunreinigt mit Eisen(III)-chlorid
| |||
|
| |||
| Bezeichnungen | |||
|---|---|---|---|
| IUPAC-Bezeichnung
Aluminiumchlorid
| |||
| Andere Namen
Aluminium(III)-chlorid
Aluminiumtrichlorid | |||
| Bezeichnungen | |||
| |||
3D-Modell (JSmol)
|
| ||
| ChEBI | |||
| ChemSpider | |||
| EC-Nummer |
| ||
Gmelin Referenz
|
1876 | ||
PubChem CID
|
|||
| RTECS-Nummer |
| ||
| UNII |
| ||
InChI
| |||
SMILES
| |||
| Eigenschaften | |||
Chemische Formel
|
AlCl3 | ||
| Molekulare Masse | 133,341 g/mol (wasserfrei) 241,432 g/mol (Hexahydrat) | ||
| Erscheinungsbild | Weißer oder blassgelber Feststoff, hygroskopisch | ||
| Dichte | 2,48 g/cm3 (wasserfrei) 2,398 g/cm3 (Hexahydrat) | ||
| Schmelzpunkt |
| ||
Löslichkeit in Wasser
|
439 g/l (0 °C) 449 g/l (10 °C) 458 g/l (20 °C) 466 g/l (30 °C) 473 g/l (40 °C) 481 g/l (60 °C) 486 g/l (80 °C) 490 g/l (100 °C) | ||
| Löslichkeit |
| ||
| Dampfdruck | 133,3 Pa (99 °C) 13,3 kPa (151 °C) | ||
| Viskosität | 0,35 cP (197 °C) 0,26 cP (237 °C) | ||
| Struktur | |||
Kristallstruktur
|
Monoklin, mS16 | ||
Raumgruppe
|
C12/m1, Nr. 12 | ||
Gitterkonstante
|
a = 0,591 nm, b = 0,591 nm, c = 1,752 nm
| ||
Gittervolumen (V)
|
0,52996 nm3 | ||
Formeleinheiten (Z)
|
6 | ||
Koordinationsgeometrie
|
Oktaedrisch (fest) Tetraedrisch (flüssig) | ||
Molekulare Form
|
Trigonal planar (monomere Dämpfe) | ||
| Thermochemie | |||
Wärmekapazität (C)
|
91,1 J/mol-K | ||
Std. molare
Entropie (S |
109.3 J/mol-K | ||
Std. Bildungsenthalpie
Bildung (ΔfH⦵298) |
-704,2 kJ/mol | ||
Gibbssche freie Energie (ΔfG˚)
|
-628,8 kJ/mol | ||
| Pharmakologie | |||
ATC-Code
|
D10AX01 (WHO) | ||
| Gefahren | |||
| GHS-Kennzeichnung: | |||
Piktogramme
|

| ||
Signalwort
|
Gefahr | ||
Gefahrenhinweise
|
H314 | ||
Sicherheitshinweise
|
P260, P280, P301+P330+P331, P303+P361+P353, P305+P351+P338+P310, P310 | ||
| NFPA 704 (Feuerdiamant) | |||
| Tödliche Dosis oder Konzentration (LD, LC): | |||
LD50 (mittlere Dosis)
|
380 mg/kg, Ratte (oral, wasserfrei) 3311 mg/kg, Ratte (oral, Hexahydrat) | ||
| NIOSH (US-Grenzwerte für die Gesundheit): | |||
PEL (Zulässig)
|
Keine | ||
REL (Empfohlen)
|
2 mg/m3 | ||
IDLH (Unmittelbare Gefahr)
|
N.D. | ||
| Verwandte Verbindungen | |||
Andere Anionen
|
Aluminiumfluorid Aluminiumbromid Aluminiumjodid | ||
Sonstige Kationen
|
Bortrichlorid Galliumtrichlorid Indium(III)-chlorid Magnesiumchlorid | ||
Verwandte Lewis-Säuren
|
Eisen(III)-chlorid Bortrifluorid | ||
Wenn nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |||
Aluminiumchlorid (AlCl3), auch bekannt als Aluminiumtrichlorid, bezeichnet Verbindungen mit der Formel AlCl3(H2O)n (n = 0 oder 6). Sie bestehen aus Aluminium- und Chloratomen im Verhältnis 1:3, wobei eine Form auch sechs Hydratationswässer enthält. Beide sind weiße Feststoffe, aber Proben sind oft mit Eisen(III)-chlorid verunreinigt, was eine gelbe Farbe ergibt. ⓘ
Das wasserfreie Material ist kommerziell wichtig. Er hat einen niedrigen Schmelz- und Siedepunkt. Er wird hauptsächlich bei der Herstellung von Aluminiummetall produziert und verbraucht, aber auch in anderen Bereichen der chemischen Industrie werden große Mengen verwendet. Die Verbindung wird oft als Lewis-Säure bezeichnet. Sie ist ein Beispiel für eine anorganische Verbindung, die sich bei milder Temperatur reversibel von einem Polymer in ein Monomer verwandelt. ⓘ
Struktur
Wasserfrei

Aluminiumchlorid bildet farblose, hexagonale Kristalle (monokline Kristallstruktur, Raumgruppe C2/m (Raumgruppen-Nr. 12), a = 5,914 Å, b = 10,234 Å, c = 6,148 Å, β = 108,25°). Es ist in vielen organischen Lösungsmitteln löslich. Das meist auf Grund von Verunreinigungen mit Eisenchloriden hellgelbe Pulver wirkt stark hygroskopisch. In feuchter Luft raucht es wegen teilweiser Hydrolyse zu Chlorwasserstoff und Aluminiumoxidchlorid. In Wasser löst es sich unter starker Erwärmung unter Bildung des Hexahydrats. In unpolaren Lösungsmitteln, flüssiger Phase sowie im Dampfzustand liegt Aluminiumchlorid als Dimer (Al2Cl6) vor, in dem das Aluminiumatom tetraedrisch koordiniert ist (analog zum Aluminiumbromid). Im festen Zustand liegt ein Ionengitter vor, in dem das Aluminiumion 6-fach durch Cl− koordiniert ist. Beim Schmelzen bricht das Ionengitter unter Bildung des Dimeren zusammen. Da dieses kovalent aufgebaut ist, leitet flüssiges Aluminiumchlorid den elektrischen Strom nur schlecht. ⓘ
Die Bindungsverhältnisse in Aluminium(III)-chlorid sind als Grenzfall zwischen kovalenter und ionischer Bindung einzuordnen, es hat eine Elektronegativitäts-Differenz ΔEN von 1,55 (nach Pauling). Damit sollte es sich eigentlich um eine polare Atombindung handeln. ⓘ
AlCl3 nimmt je nach Temperatur und Zustand (fest, flüssig, gasförmig) drei Strukturen an. Festes AlCl3 hat eine blattförmige Schichtstruktur mit kubisch dicht gepackten Chloridionen. In diesem Gerüst weisen die Al-Zentren eine oktaedrische Koordinationsgeometrie auf. Yttrium(III)-chlorid weist die gleiche Struktur auf, ebenso wie eine Reihe von anderen Verbindungen. Im geschmolzenen Zustand liegt Aluminiumtrichlorid als Dimer Al2Cl6 mit tetrakoordiniertem Aluminium vor. Diese Strukturänderung hängt mit der geringeren Dichte der flüssigen Phase (1,78 g/cm3) gegenüber festem Aluminiumtrichlorid (2,48 g/cm3) zusammen. Al2Cl6-Dimere finden sich auch in der Dampfphase. Bei höheren Temperaturen dissoziieren die Al2Cl6-Dimere zu trigonalem, planarem AlCl3, das strukturell mit BF3 vergleichbar ist. Die Schmelze leitet Elektrizität schlecht, im Gegensatz zu stärker ionischen Halogeniden wie Natriumchlorid. ⓘ
Das Aluminiumchloridmonomer gehört in seiner monomeren Form zur Punktgruppe D3h und in seiner dimeren Form zu D2h. ⓘ
Hexahydrat
Das Hexahydrat besteht aus oktaedrischen [Al(H2O)6]3+-Zentren und Chlorid-Gegenionen. Wasserstoffbrücken verbinden das Kation und die Anionen. Die hydratisierte Form von Aluminiumchlorid weist eine oktaedrische Molekülgeometrie auf, wobei das zentrale Aluminiumion von sechs Wasserligandenmolekülen umgeben ist. Da es koordinativ gesättigt ist, ist das Hydrat als Katalysator für die Friedel-Crafts-Alkylierung und verwandte Reaktionen von geringem Wert. ⓘ
Verwendungen
Alkylierung und Acylierung von Arenen
AlCl3 ist ein gängiger Lewis-Säure-Katalysator für Friedel-Crafts-Reaktionen, sowohl für Acylierungen als auch für Alkylierungen. Wichtige Produkte sind Detergenzien und Ethylbenzol. Für diese Art von Reaktionen wird Aluminiumchlorid hauptsächlich verwendet, z. B. bei der Herstellung von Anthrachinon (das in der Farbstoffindustrie verwendet wird) aus Benzol und Phosgen. Bei der allgemeinen Friedel-Crafts-Reaktion reagiert ein Acylchlorid oder Alkylhalogenid wie dargestellt mit einem aromatischen System:
Die Alkylierungsreaktion ist weiter verbreitet als die Acylierungsreaktion, obwohl ihre Durchführung technisch anspruchsvoller ist. Für beide Reaktionen sollten das Aluminiumchlorid sowie andere Materialien und die Ausrüstung trocken sein, obwohl eine Spur von Feuchtigkeit für den Ablauf der Reaktion notwendig ist. Für die Alkylierung und Acylierung von Aren liegen detaillierte Verfahren vor. ⓘ
Ein allgemeines Problem bei der Friedel-Crafts-Reaktion besteht darin, dass der Aluminiumchlorid-Katalysator manchmal in voller stöchiometrischer Menge benötigt wird, da er mit den Produkten einen starken Komplex bildet. Diese Komplikation führt mitunter zu einer großen Menge an korrosiven Abfällen. Aus diesen und ähnlichen Gründen wurde die Verwendung von Aluminiumchlorid häufig durch Zeolithe verdrängt. ⓘ
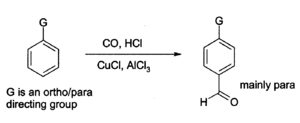
Aluminiumchlorid kann auch verwendet werden, um Aldehydgruppen in aromatische Ringe einzubringen, z. B. über die Gattermann-Koch-Reaktion, bei der Kohlenmonoxid, Chlorwasserstoff und ein Kupfer(I)-chlorid als Co-Katalysator verwendet werden.
Weitere Anwendungen in der organischen und organometallischen Synthese
Aluminiumchlorid findet eine Vielzahl weiterer Anwendungen in der organischen Chemie. So kann es beispielsweise die "Ene-Reaktion" katalysieren, wie die Addition von 3-Buten-2-on (Methylvinylketon) an Carvon:
Es wird verwendet, um eine Vielzahl von Kohlenwasserstoff-Kopplungen und -Umlagerungen zu induzieren. ⓘ
Aluminiumchlorid in Verbindung mit Aluminium in Gegenwart eines Arens kann zur Synthese von Bis(aren)-Metallkomplexen, z. B. Bis(benzol)chrom, aus bestimmten Metallhalogeniden über die so genannte Fischer-Hafner-Synthese verwendet werden. Dichlorphenylphosphin wird durch Reaktion von Benzol und Phosphortrichlorid, katalysiert durch Aluminiumchlorid, hergestellt. ⓘ
Reaktionen
Wasserfreies Aluminiumchlorid ist eine starke Lewis-Säure, die in der Lage ist, selbst mit schwachen Lewis-Basen wie Benzophenon und Mesitylen Lewis-Säure-Base-Addukte zu bilden. In Gegenwart von Chloridionen bildet es Tetrachloraluminat (AlCl4-). ⓘ
Aluminiumchlorid reagiert mit Calcium- und Magnesiumhydriden in Tetrahydrofuran unter Bildung von Tetrahydroaluminaten. ⓘ
Reaktionen mit Wasser
Wasserfreies Aluminiumchlorid ist hygroskopisch und hat eine ausgeprägte Affinität zu Wasser. Es dampft in feuchter Luft und zischt, wenn es mit flüssigem Wasser vermischt wird, da die Cl-Liganden durch H2O-Moleküle verdrängt werden und das Hexahydrat [Al(H2O)6]Cl3 bilden. Die wasserfreie Phase kann beim Erhitzen des Hexahydrats nicht wiederhergestellt werden. Stattdessen geht HCl verloren, so dass Aluminiumhydroxid oder Aluminiumoxid zurückbleibt:
- Al(H2O)6Cl3 → Al(OH)3 + 3 HCl + 3 H2O ⓘ
Wie Metall-Aquo-Komplexe ist wässriges AlCl3 aufgrund der Ionisierung der Aquoliganden sauer:
- [Al(H2O)6]3+ ⇌ [Al(OH)(H2O)5]2+ + H+ ⓘ
Wässrige Lösungen verhalten sich ähnlich wie andere Aluminiumsalze, die hydratisierte Al3+-Ionen enthalten, und ergeben bei der Reaktion mit verdünnter Natronlauge einen gallertartigen Niederschlag von Aluminiumhydroxid:
- AlCl3 + 3 NaOH → [Al(OH)3] + 3 NaCl ⓘ
Synthese
Aluminiumchlorid wird in großem Maßstab durch die exotherme Reaktion von Aluminiummetall mit Chlor oder Chlorwasserstoff bei Temperaturen zwischen 650 und 750 °C hergestellt.
- 2 Al + 3 Cl2 → 2 AlCl3
- 2 Al + 6 HCl → 2 AlCl3 + 3 H2 ⓘ
Aluminiumchlorid kann durch eine einfache Verdrängungsreaktion zwischen Kupferchlorid und Aluminiummetall gebildet werden.
- 2 Al + 3 CuCl2 → 2 AlCl3 + 3 Cu
In den USA wurden 1993 etwa 21.000 Tonnen hergestellt, wobei die bei der Aluminiumherstellung verbrauchten Mengen nicht mitgezählt wurden. ⓘ
Hydratisiertes Aluminiumtrichlorid wird durch Auflösen von Aluminiumoxiden in Salzsäure hergestellt. Auch metallisches Aluminium löst sich leicht in Salzsäure auf ─ unter Freisetzung von Wasserstoffgas und Erzeugung erheblicher Wärme. Beim Erhitzen dieses Feststoffs entsteht kein wasserfreies Aluminiumtrichlorid, sondern das Hexahydrat zersetzt sich beim Erhitzen zu Aluminiumhydroxid:
- Al(H2O)6Cl3 → Al(OH)3 + 3 HCl + 3 H2O ⓘ
Aluminium bildet auch ein niederes Chlorid, Aluminium(I)-chlorid (AlCl), das jedoch sehr instabil ist und nur in der Dampfphase bekannt ist. ⓘ
So muss die Herstellung von wasserfreiem Aluminiumchlorid durch Überleiten von Chlor über Kohlenstoff und Aluminiumoxid bei etwa 800 °C oder direkt aus den Elementen erfolgen:
- Fehler beim Parsen (Syntaxfehler): {\displaystyle \ce{Al2O3 + 3C + 3Cl2 -> 2AlCl3 + 3CO <span title="Aus: Deutsche Wikipedia, Abschnitt "Synthese"" class="plainlinks">[https://de.wikipedia.org/wiki/Aluminiumchlorid#Synthese <span style="color:#dddddd">ⓘ</span>]</span>}}
beziehungsweise:
- Fehler beim Parsen (Syntaxfehler): {\displaystyle \ce{2Al + 3Cl2 -> 2AlCl3 <span title="Aus: Deutsche Wikipedia, Abschnitt "Synthese"" class="plainlinks">[https://de.wikipedia.org/wiki/Aluminiumchlorid#Synthese <span style="color:#dddddd">ⓘ</span>]</span>}}
Für die großtechnische Herstellung von Aluminiumchlorid werden aufgrund der hohen Aggressivität der beteiligten Reaktanten emaillierte Rührbehälter verwendet. ⓘ
Natürliches Vorkommen
Wasserfreies Aluminiumchlorid kommt nicht als Mineral vor. Das Hexahydrat ist jedoch als das seltene Mineral Chloraluminit bekannt. Ein komplexeres, basisches und hydratisiertes Aluminiumchloridmineral ist Cadwaladerit. ⓘ
Sicherheit
Wasserfreies AlCl3 reagiert heftig mit Basen, so dass geeignete Vorsichtsmaßnahmen erforderlich sind. Es kann beim Einatmen oder bei Kontakt zu Reizungen der Augen, der Haut und der Atemwege führen. ⓘ
Sicherheitshinweise
Aluminiumchlorid wurde 2014 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Aluminiumchlorid waren die Besorgnisse bezüglich Exposition von Arbeitnehmern, hoher (aggregierter) Tonnage und hohes Risikoverhältnis (Risk Characterisation Ratio, RCR) sowie der Gefahren ausgehend von einer möglichen Zuordnung zur Gruppe der CMR-Substanzen. Die Neubewertung läuft seit 2015 und wird von Frankreich durchgeführt. Um zu einer abschließenden Bewertung gelangen zu können, wurden weitere Informationen nachgefordert. ⓘ
Handelspräparate
- Monopräparate
Everdry (D), Gargarisma zum Gurgeln (D), Mallebrin (Ursprünglicher Wirkstoff Aluminiumchlorat) (D)
- Kombinationspräparate
AHC20 (CH), AHC30 (CH), Never-Sweat (D), Odaban (GB), Seven days (D), Yerka (D), Purax (D) ⓘ