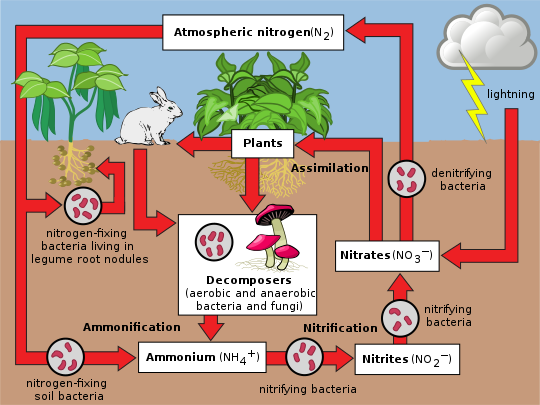
Stickstoffkreislauf

Der Stickstoffkreislauf ist der biogeochemische Kreislauf, durch den Stickstoff in verschiedene chemische Formen umgewandelt wird, während er zwischen atmosphärischen, terrestrischen und marinen Ökosystemen zirkuliert. Die Umwandlung von Stickstoff kann sowohl durch biologische als auch durch physikalische Prozesse erfolgen. Wichtige Prozesse im Stickstoffkreislauf sind Fixierung, Ammonifikation, Nitrifikation und Denitrifikation. Der größte Teil der Erdatmosphäre (78 %) besteht aus atmosphärischem Stickstoff und ist damit die größte Stickstoffquelle. Allerdings ist der atmosphärische Stickstoff für die biologische Nutzung nur begrenzt verfügbar, was in vielen Ökosystemen zu einer Verknappung des nutzbaren Stickstoffs führt. ⓘ
Der Stickstoffkreislauf ist für Ökologen von besonderem Interesse, da die Stickstoffverfügbarkeit die Geschwindigkeit wichtiger Ökosystemprozesse, einschließlich Primärproduktion und Zersetzung, beeinflussen kann. Menschliche Aktivitäten wie die Verbrennung fossiler Brennstoffe, die Verwendung von künstlichem Stickstoffdünger und die Freisetzung von Stickstoff in Abwässern haben den globalen Stickstoffkreislauf dramatisch verändert. Die Veränderung des globalen Stickstoffkreislaufs durch den Menschen kann sich negativ auf das natürliche Umweltsystem und auch auf die menschliche Gesundheit auswirken. ⓘ

Der Stickstoffkreislauf oder Stickstoffzyklus ist die stetige Wanderung und biogeochemische Umsetzung des Bioelementes Stickstoff in der Erdatmosphäre, in Gewässern, in Böden und in Biomasse. ⓘ
Vorgänge
| Teil einer Serie über ⓘ |
| Biogeochemische Kreisläufe |
|---|
 |
|
Stickstoff kommt in der Umwelt in einer Vielzahl von chemischen Formen vor, darunter organischer Stickstoff, Ammonium (NH+4), Nitrit (NO-2), Nitrat (NO-3), Distickstoffoxid (N2O), Stickstoffoxid (NO) oder anorganisches Stickstoffgas (N2). Organischer Stickstoff kann in Form von lebenden Organismen, Humus oder in den Zwischenprodukten der Zersetzung organischer Stoffe enthalten sein. Die Prozesse im Stickstoffkreislauf bestehen darin, Stickstoff von einer Form in eine andere umzuwandeln. Viele dieser Prozesse werden von Mikroben durchgeführt, entweder um Energie zu gewinnen oder um Stickstoff in einer Form zu akkumulieren, die sie für ihr Wachstum benötigen. So werden zum Beispiel die stickstoffhaltigen Abfälle im Urin von Tieren von nitrifizierenden Bakterien im Boden abgebaut, um von den Pflanzen genutzt zu werden. Das nebenstehende Diagramm zeigt, wie diese Prozesse zusammen den Stickstoffkreislauf bilden. ⓘ
- Zu viele Fische, Fütterung, Pflanzenreste und Laub reichern das Teichwasser mit organischem Material an, in dem Stickstoff-Verbindungen enthalten sind. Auch zum Nachfüllen verwendetes Regenwasser aus Zisternen, Pollenflug und Gartendünger tragen zur Überdüngung des Teiches bei.
- Mikroorganismen zersetzen die Biomasse unter Verbrauch von Sauerstoff und setzen dabei den enthaltenen Stickstoff als Ammonium bzw. giftiges Ammoniak frei. Ab pH-Wert 8,5 liegt davon so viel als Ammoniak vor, dass es für Fische bedrohlich ist; (das pH-Optimum liegt bei 7–8).
- Die nitrifizierenden Bakterien, z. B. Bakterien der Gattungen Nitrosomonas und Nitrobacter, oxidieren beides unter oxischen Bedingungen zu Nitrat (Nitrifikation). Dieses Endprodukt des Eiweißabbaus ist wichtiger Mineralstoff aller Pflanzen und für Fische ungefährlich.
- Durch Pflanzenreste kommt totes organisches Material in den Teich, wodurch der Kreislauf geschlossen wird. ⓘ
Auswirkungen von Störungen
- Die Teichpflanzen können das Nitrat meist nur teilweise verbrauchen. Die überschüssige Menge wird bei jedem Kreislauf größer und überdüngt das Wasser. Algen nehmen überhand und trüben den Teich.
- Ist der Überschuss aufgebraucht, sterben die meisten Algen ab. Ihre Zersetzung durch Mikroorganismen verbraucht viel Sauerstoff, vor allem nachts. Wenn die Fische an der Oberfläche nach Luft schnappen, ist dies ein sicherer Hinweis auf Sauerstoffmangel.
- Unter anoxischen Bedingungen, die im Sediment (Schlamm) oder – bei starker Sauerstoffzehrung infolge starker Belastung mit organischen Stoffen – auch im Wasserkörper herrschen können, reduzieren viele Bakterien Nitrat zu Nitrit, das für Fische giftig ist. ⓘ
Behebung der Störungen
- Sauerstoffmangel lässt sich technisch beheben, indem Sauerstoff aus der Luft eingebracht wird, z. B. durch Umpumpen des Wassers, Wasserspiele, Bachläufe und Quellsteine.
- Dennoch bleibt das Wasser trüb, weil die überschüssigen Mineralstoffe noch im Wasser sind und zur nächsten Algenblüte führen. Darum ist das überschüssige Nitrat zu entfernen – etwa durch bakterielle Denitrifikation. ⓘ
Stickstofffixierung
Die Umwandlung von Stickstoffgas (N2) in Nitrate und Nitrite durch atmosphärische, industrielle und biologische Prozesse wird als Stickstofffixierung bezeichnet. Atmosphärischer Stickstoff muss in eine verwertbare Form umgewandelt oder "fixiert" werden, damit er von Pflanzen aufgenommen werden kann. Zwischen 5 und 10 Milliarden kg pro Jahr werden durch Blitzeinschläge fixiert, aber der größte Teil der Fixierung erfolgt durch frei lebende oder symbiotische Bakterien, die als Diazotrophe bekannt sind. Diese Bakterien verfügen über das Enzym Nitrogenase, das gasförmigen Stickstoff mit Wasserstoff verbindet, um Ammoniak zu erzeugen, das von den Bakterien in andere organische Verbindungen umgewandelt wird. Die meisten biologischen Stickstofffixierungen erfolgen durch die Aktivität der Mo-Nitrogenase, die in einer Vielzahl von Bakterien und einigen Archaeen vorkommt. Mo-Nitrogenase ist ein komplexes Zweikomponenten-Enzym, das mehrere metallhaltige prosthetische Gruppen aufweist. Ein Beispiel für freilebende Bakterien ist Azotobacter. Symbiotische stickstofffixierende Bakterien wie Rhizobium leben normalerweise in den Wurzelknöllchen von Leguminosen (wie Erbsen, Luzerne und Robinien). Dort gehen sie eine wechselseitige Beziehung mit der Pflanze ein und produzieren Ammoniak im Austausch gegen Kohlenhydrate. Aufgrund dieser Beziehung erhöhen Leguminosen häufig den Stickstoffgehalt stickstoffarmer Böden. Auch einige Nicht-Leguminosen können solche Symbiosen eingehen. Heute werden etwa 30 % des gesamten fixierten Stickstoffs industriell nach dem Haber-Bosch-Verfahren hergestellt, bei dem Stickstoffgas und eine Wasserstoffquelle (Erdgas oder Erdöl) unter hohen Temperaturen und Drücken in Ammoniak umgewandelt werden. ⓘ
Assimilation
Pflanzen können über ihre Wurzelhaare Nitrat oder Ammonium aus dem Boden aufnehmen. Wird Nitrat aufgenommen, wird es zunächst zu Nitrit- und dann zu Ammonium-Ionen reduziert und in Aminosäuren, Nukleinsäuren und Chlorophyll eingebaut. Bei Pflanzen, die eine symbiotische Beziehung zu Rhizobien haben, wird ein Teil des Stickstoffs in Form von Ammoniumionen direkt von den Knöllchen aufgenommen. Heute weiß man, dass es einen komplexeren Kreislauf von Aminosäuren zwischen Rhizobia-Bakteroiden und Pflanzen gibt. Die Pflanze stellt den Bacteroiden Aminosäuren zur Verfügung, so dass eine Ammoniakassimilation nicht erforderlich ist, und die Bacteroide geben die Aminosäuren (zusammen mit dem neu fixierten Stickstoff) an die Pflanze zurück, so dass eine wechselseitige Beziehung entsteht. Während viele Tiere, Pilze und andere heterotrophe Organismen Stickstoff durch die Aufnahme von Aminosäuren, Nukleotiden und anderen kleinen organischen Molekülen erhalten, sind andere Heterotrophe (einschließlich vieler Bakterien) in der Lage, anorganische Verbindungen wie Ammonium als einzige N-Quellen zu nutzen. Die Verwertung verschiedener N-Quellen wird in allen Organismen sorgfältig reguliert. ⓘ
Ammonifikation
Wenn eine Pflanze oder ein Tier stirbt oder ein Tier Abfallstoffe ausscheidet, ist die ursprüngliche Form des Stickstoffs organisch. Bakterien oder Pilze wandeln den organischen Stickstoff in den Überresten wieder in Ammonium (NH+4) um, ein Prozess, der Ammonifikation oder Mineralisierung genannt wird. Die beteiligten Enzyme sind:
- GS: Gln-Synthetase (zytosolisch & plastisch)
- GOGAT: Glu-2-Oxoglutarat-Aminotransferase (Ferredoxin- und NADH-abhängig)
- GDH: Glu-Dehydrogenase:
- Geringe Rolle bei der Ammonium-Assimilation.
- Wichtig für den Aminosäure-Katabolismus. ⓘ

Nitrifikation
Die Umwandlung von Ammonium in Nitrat wird in erster Linie von bodenlebenden Bakterien und anderen nitrifizierenden Bakterien durchgeführt. In der ersten Stufe der Nitrifikation erfolgt die Oxidation von Ammonium (NH+4) durch Bakterien wie Nitrosomonas, die Ammoniak in Nitrite (NO-2) umwandeln. Andere Bakterienarten, wie Nitrobacter, sind für die Oxidation der Nitrite (NO-2) zu Nitraten (NO-3) verantwortlich. Es ist wichtig, dass das Ammoniak (NH3) in Nitrate oder Nitrite umgewandelt wird, da Ammoniakgas für Pflanzen giftig ist. ⓘ
Aufgrund ihrer sehr hohen Löslichkeit und der Tatsache, dass Böden kaum in der Lage sind, Anionen zurückzuhalten, können Nitrate ins Grundwasser gelangen. Ein erhöhter Nitratgehalt im Grundwasser ist für die Trinkwassernutzung bedenklich, da Nitrat den Sauerstoffgehalt im Blut von Säuglingen beeinträchtigen und Methämoglobinämie oder das Blue-Baby-Syndrom verursachen kann. Dort, wo Grundwasser den Flusslauf anreichert, kann mit Nitrat angereichertes Grundwasser zur Eutrophierung beitragen, einem Prozess, der zu einer hohen Algenpopulation und -wachstum führt, insbesondere zu Blaualgenpopulationen. Nitrat ist zwar nicht direkt giftig für Fische wie Ammoniak, kann aber indirekte Auswirkungen auf Fische haben, wenn es zu dieser Eutrophierung beiträgt. Stickstoff hat in einigen Gewässern zu schweren Eutrophierungsproblemen beigetragen. Seit 2006 wird die Ausbringung von Stickstoffdünger in Großbritannien und den Vereinigten Staaten zunehmend kontrolliert. Dies geschieht nach dem gleichen Muster wie die Kontrolle der Phosphordüngung, deren Beschränkung normalerweise als wesentlich für die Erholung eutrophierter Gewässer angesehen wird. ⓘ
Denitrifikation
Unter Denitrifikation versteht man die Reduktion von Nitraten zu Stickstoffgas (N2), wodurch der Stickstoffkreislauf geschlossen wird. Dieser Prozess wird von Bakterienarten wie Pseudomonas und Paracoccus unter anaeroben Bedingungen durchgeführt. Sie verwenden das Nitrat als Elektronenakzeptor anstelle von Sauerstoff bei der Atmung. Diese fakultativ (d. h. wahlweise) anaeroben Bakterien können auch unter aeroben Bedingungen leben. Die Denitrifikation findet unter anaeroben Bedingungen statt, z. B. in wassergesättigten Böden. Die denitrifizierenden Bakterien nutzen die Nitrate im Boden zur Atmung und produzieren dabei Stickstoffgas, das inert und für Pflanzen nicht verfügbar ist. Die Denitrifikation kommt sowohl bei frei lebenden Mikroorganismen als auch bei obligaten Symbionten anaerober Wimpertierchen vor. ⓘ
Fluss des Stickstoffs durch das Ökosystem. Bakterien sind ein Schlüsselelement des Kreislaufs und liefern verschiedene Formen von Stickstoffverbindungen, die von höheren Organismen aufgenommen werden können. ⓘ
Einfache Darstellung des Stickstoffkreislaufs. Blau steht für die Stickstoffspeicherung, grün für Prozesse, die Stickstoff von einem Ort zum anderen bewegen, und rot für die beteiligten Bakterien ⓘ
Dissimilatorische Nitratreduktion zu Ammonium
Die dissimilatorische Nitratreduktion zu Ammonium (DNRA) oder Nitrat/Nitrit-Ammonifikation ist ein anaerober Atmungsprozess. Mikroben, die DNRA betreiben, oxidieren organisches Material und nutzen Nitrat als Elektronenakzeptor, indem sie es zu Nitrit und dann zu Ammonium reduzieren (NO-3 → NO-2 → NH+4). Sowohl denitrifizierende als auch Nitrat-Ammonifizierungsbakterien konkurrieren um Nitrat in der Umwelt, obwohl DNRA dazu dient, bioverfügbaren Stickstoff als lösliches Ammonium zu erhalten, anstatt Distickstoffgas zu erzeugen. ⓘ
Anaerobe Ammoniak-Oxidation
Bei diesem biologischen Prozess werden Nitrit und Ammoniak direkt in molekulares Stickstoffgas (N2) umgewandelt. Dieser Prozess macht einen großen Teil der Stickstoffumwandlung in den Ozeanen aus. Die Gleichgewichtsformel für diese chemische Reaktion "Anammox" lautet: NH+4 + NO-2 → N2 + 2 H2O (ΔG° = -357 kJ⋅mol-1). ⓘ
Andere Prozesse
Obwohl die Stickstofffixierung in den meisten Ökosystemen die Hauptquelle für pflanzenverfügbaren Stickstoff ist, dient in Gebieten mit stickstoffreichem Grundgestein auch der Abbau dieses Gesteins als Stickstoffquelle. Die Nitratreduktion ist auch Teil des Eisenkreislaufs. Unter anoxischen Bedingungen kann Fe(II) ein Elektron an NO-3 abgeben und wird zu Fe(III) oxidiert, während NO-3 je nach den Bedingungen und den beteiligten Mikrobenarten zu NO-2, N2O, N2 und NH+4 reduziert wird. Die Fäkalienfahnen der Wale fungieren auch als Knotenpunkt im marinen Stickstoffkreislauf, indem sie den Stickstoff in den epipelagischen Zonen der Ozeane konzentrieren, bevor er sich in den verschiedenen Meeresschichten ausbreitet, was letztlich die ozeanische Primärproduktivität erhöht. ⓘ
Mariner Stickstoffkreislauf


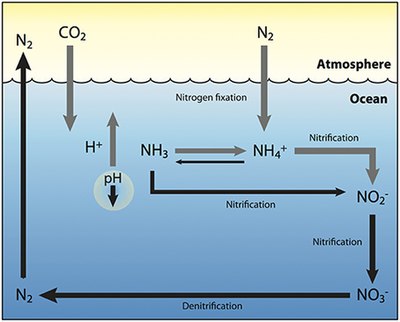
Der Stickstoffkreislauf ist auch im Meer ein wichtiger Prozess. Der Gesamtzyklus ist zwar ähnlich, aber es gibt verschiedene Akteure und Übertragungswege für Stickstoff im Ozean. Stickstoff gelangt durch Niederschlag, Abfluss oder als N2 aus der Atmosphäre in das Wasser. Stickstoff kann von Phytoplankton nicht als N2 verwertet werden und muss daher einer Stickstofffixierung unterzogen werden, die vor allem von Cyanobakterien durchgeführt wird. Ohne die Zufuhr von fixiertem Stickstoff in den Meereskreislauf wäre der fixierte Stickstoff in etwa 2000 Jahren aufgebraucht. Das Phytoplankton benötigt Stickstoff in biologisch verfügbaren Formen für die anfängliche Synthese organischer Stoffe. Ammoniak und Harnstoff werden durch Ausscheidungen des Planktons in das Wasser abgegeben. Die Stickstoffquellen werden durch die Abwärtsbewegung der organischen Substanz aus der euphotischen Zone entfernt. Dies kann durch das Absinken von Phytoplankton, vertikale Durchmischung oder das Absinken von Abfällen von Vertikalwanderern geschehen. Das Absinken führt dazu, dass Ammoniak in geringere Tiefen unterhalb der euphotischen Zone eingetragen wird. Bakterien sind in der Lage, Ammoniak in Nitrit und Nitrat umzuwandeln, aber sie werden durch Licht gehemmt, so dass dies unterhalb der euphotischen Zone geschehen muss. Die Ammonifikation oder Mineralisierung wird von Bakterien durchgeführt, um organischen Stickstoff in Ammoniak umzuwandeln. Anschließend kann eine Nitrifikation stattfinden, bei der das Ammonium in Nitrit und Nitrat umgewandelt wird. Nitrat kann durch vertikale Durchmischung und Auftrieb in die euphotische Zone zurückgeführt werden, wo es vom Phytoplankton aufgenommen werden kann, um den Kreislauf fortzusetzen. N2 kann durch Denitrifikation in die Atmosphäre zurückgeführt werden. ⓘ
Man geht davon aus, dass Ammonium die bevorzugte Quelle für gebundenen Stickstoff für das Phytoplankton ist, da seine Assimilation keine Redoxreaktion erfordert und daher wenig Energie benötigt. Nitrat erfordert eine Redoxreaktion für die Assimilation, ist aber häufiger vorhanden, so dass sich die meisten Phytoplanktonarten so angepasst haben, dass sie die für diese Reduktion erforderlichen Enzyme besitzen (Nitratreduktase). Es gibt einige bemerkenswerte und bekannte Ausnahmen, darunter die meisten Prochlorococcus und einige Synechococcus, die Stickstoff nur in Form von Ammonium aufnehmen können. ⓘ
Die Nährstoffe im Ozean sind nicht gleichmäßig verteilt. Gebiete mit Auftrieb liefern Stickstoff aus dem Bereich unterhalb der euphotischen Zone. Die Küstengebiete liefern Stickstoff aus dem Abfluss, und an der Küste kommt es leicht zu Auftrieb. Allerdings ist die Geschwindigkeit, mit der Stickstoff vom Phytoplankton aufgenommen werden kann, in oligotrophen Gewässern das ganze Jahr über und in gemäßigten Gewässern im Sommer verringert, was zu einer geringeren Primärproduktion führt. Auch die Verteilung der verschiedenen Stickstoffformen ist in den Ozeanen unterschiedlich. ⓘ
Nitrat ist im oberflächennahen Wasser verarmt, außer in Auftriebsgebieten. In den Auftriebsgebieten an der Küste sind die Nitrat- und Chlorophyllwerte aufgrund der erhöhten Produktion normalerweise hoch. Es gibt jedoch auch Regionen mit hohem Oberflächennitrat, aber niedrigem Chlorophyll, die als HNLC-Regionen (high nitrogen, low chlorophyll) bezeichnet werden. Die beste Erklärung für HNLC-Regionen ist der Eisenmangel im Ozean, der eine wichtige Rolle bei der Ozeandynamik und den Nährstoffkreisläufen spielen kann. Der Eiseneintrag variiert je nach Region und wird dem Ozean durch Staub (aus Staubstürmen) und durch Auswaschung aus Gestein zugeführt. Eisen wird als das wirklich begrenzende Element für die Produktivität der Ökosysteme im Ozean angesehen. ⓘ
Ammonium und Nitrit weisen eine maximale Konzentration in 50-80 m Tiefe (unteres Ende der euphotischen Zone) auf, während die Konzentration unterhalb dieser Tiefe abnimmt. Diese Verteilung lässt sich dadurch erklären, dass Nitrit und Ammonium Zwischenprodukte sind. Sie werden beide in der Wassersäule schnell produziert und verbraucht. Die Menge an Ammonium im Ozean ist um etwa 3 Größenordnungen geringer als die von Nitrat. Von Ammonium, Nitrit und Nitrat hat Nitrit die schnellste Umsatzrate. Es kann bei der Nitratassimilation, der Nitrifikation und der Denitrifikation gebildet werden, wird aber sofort wieder verbraucht. ⓘ
Neuer vs. regenerierter Stickstoff
Stickstoff, der in die euphotische Zone gelangt, wird als neuer Stickstoff bezeichnet, weil er von außerhalb der produktiven Schicht neu hinzukommt. Der neue Stickstoff kann von unterhalb der euphotischen Zone oder aus externen Quellen stammen. Äußere Quellen sind der Auftrieb aus dem Tiefenwasser und die Stickstofffixierung. Wird die organische Substanz gefressen, veratmet, als Ammoniak an das Wasser abgegeben und vom Phytoplankton wieder in die organische Substanz eingebaut, spricht man von recycelter/regenerierter Produktion. ⓘ
Die Neuproduktion ist ein wichtiger Bestandteil der Meeresumwelt. Ein Grund dafür ist, dass nur ein kontinuierlicher Eintrag von neuem Stickstoff die Gesamtkapazität des Ozeans für eine nachhaltige Fischernte bestimmen kann. Die Entnahme von Fischen aus Gebieten mit regeneriertem Stickstoff führt zu einem Rückgang des Stickstoffs und damit zu einem Rückgang der Primärproduktion. Dies wird sich negativ auf das System auswirken. Wenn jedoch Fische aus Gebieten mit neuem Stickstoff geerntet werden, wird der Stickstoff wieder aufgefüllt. ⓘ
Künftige Versauerung
Wie das Diagramm rechts zeigt, wird zusätzliches Kohlendioxid vom Ozean aufgenommen und reagiert mit Wasser. Dabei entsteht Kohlensäure, die in Bikarbonat (H2CO3) und Wasserstoff (H+)-Ionen zerfällt (grauer Pfeil), wodurch sich das bioverfügbare Karbonat verringert und der pH-Wert des Ozeans sinkt (schwarzer Pfeil). Dadurch wird wahrscheinlich die Stickstofffixierung durch Diazatrophen (grauer Pfeil) gefördert, die H+-Ionen nutzen, um Stickstoff in bioverfügbare Formen wie Ammoniak (NH3) und Ammoniumionen (NH+4) umzuwandeln. Wenn jedoch der pH-Wert sinkt und mehr Ammoniak in Ammoniumionen umgewandelt wird (grauer Pfeil), findet weniger Oxidation von Ammoniak zu Nitrit (NO-
2), was insgesamt zu einem Rückgang der Nitrifikation und Denitrifikation führt (schwarze Pfeile). Dies wiederum würde zu einer weiteren Anhäufung von gebundenem Stickstoff im Ozean führen, mit der möglichen Folge einer Eutrophierung. Graue Pfeile stehen für eine Zunahme, schwarze Pfeile für eine Abnahme des entsprechenden Prozesses. ⓘ
Menschliche Einflüsse auf den Stickstoffkreislauf


Durch den extensiven Anbau von Hülsenfrüchten (insbesondere Soja, Luzerne und Klee), den zunehmenden Einsatz des Haber-Bosch-Verfahrens bei der Herstellung von chemischen Düngemitteln und die Verschmutzung durch Kraftfahrzeuge und Industrieanlagen hat der Mensch den jährlichen Transfer von Stickstoff in biologisch verfügbare Formen mehr als verdoppelt. Darüber hinaus hat der Mensch in erheblichem Maße zum Transfer von Stickstoffspurengasen von der Erde in die Atmosphäre und vom Land in aquatische Systeme beigetragen. Die vom Menschen verursachten Veränderungen des globalen Stickstoffkreislaufs sind in den Industrieländern und in Asien am stärksten, wo die Emissionen von Kraftfahrzeugen und die industrielle Landwirtschaft am größten sind. ⓘ
Die Erzeugung von reaktivem Stickstoff hat sich im letzten Jahrhundert aufgrund der weltweiten Industrialisierung mehr als verzehnfacht. Diese Form des Stickstoffs durchläuft die Biosphäre in einer Kaskade über verschiedene Mechanismen und akkumuliert sich, da die Entstehungsrate größer ist als die Denitrifikationsrate. ⓘ
Distickstoffoxid (N2O) ist in der Atmosphäre durch Düngung in der Landwirtschaft, Verbrennung von Biomasse, Vieh- und Futtermittelanlagen und industrielle Quellen angestiegen. N2O hat schädliche Auswirkungen in der Stratosphäre, wo es abgebaut wird und als Katalysator für die Zerstörung des atmosphärischen Ozons wirkt. Lachgas ist auch ein Treibhausgas und trägt derzeit nach Kohlendioxid und Methan am drittgrößten zur globalen Erwärmung bei. Obwohl es in der Atmosphäre nicht so häufig vorkommt wie Kohlendioxid, ist es bei gleicher Masse in seiner Fähigkeit, den Planeten zu erwärmen, fast 300 Mal stärker. ⓘ
Der Anteil von Ammoniak (NH3) in der Atmosphäre hat sich durch menschliche Aktivitäten verdreifacht. Es ist ein Reaktant in der Atmosphäre, wo es als Aerosol wirkt, die Luftqualität verschlechtert und sich an Wassertröpfchen anlagert, was schließlich zu Salpetersäure (HNO3) führt, die sauren Regen erzeugt. Ammoniak und Salpetersäure in der Atmosphäre schädigen auch die Atemwege. ⓘ
Die sehr hohe Temperatur von Blitzen erzeugt natürlich geringe Mengen an NOx, NH3 und HNO3, aber die Hochtemperaturverbrennung hat zu einem 6- oder 7-fachen Anstieg des NOx-Flusses in die Atmosphäre beigetragen. Die NOx-Produktion ist eine Funktion der Verbrennungstemperatur - je höher die Temperatur, desto mehr NOx wird produziert. Die Verbrennung fossiler Brennstoffe trägt in erster Linie dazu bei, aber auch Biokraftstoffe und sogar die Verbrennung von Wasserstoff. Allerdings kann die Menge an Wasserstoff, die direkt in die Verbrennungskammern von Verbrennungsmotoren eingespritzt wird, gesteuert werden, um die höheren Verbrennungstemperaturen, die NOx erzeugen, zu vermeiden. ⓘ
Ammoniak und Stickoxide verändern aktiv die Atmosphärenchemie. Sie sind Vorläufer der troposphärischen Ozonproduktion (untere Atmosphäre), die zu Smog und saurem Regen beiträgt, Pflanzen schädigt und den Stickstoffeintrag in Ökosysteme erhöht. Ökosystemprozesse können sich durch Stickstoffdüngung verbessern, aber der anthropogene Eintrag kann auch zu einer Stickstoffsättigung führen, die die Produktivität schwächt und die Gesundheit von Pflanzen, Tieren, Fischen und Menschen schädigen kann. ⓘ
Ein Rückgang der biologischen Vielfalt kann auch die Folge sein, wenn durch eine höhere Stickstoffverfügbarkeit stickstoffbedürftige Gräser zunehmen, was zu einer Verschlechterung der stickstoffarmen, artenreichen Heidelandschaft führt. ⓘ
Die Umsetzungen im Stickstoff-Kreislauf bewegen jährlich insgesamt 250-300 Mio. t Stickstoff, was aber nur ein Millionstel des Stickstoffs in der Atmosphäre ausmacht. Die erheblichen Emissionen von gesundheitsgefährdenden Stickoxiden als Nebenprodukte von Verbrennungen (Kraftfahrzeuge) und die Emissionen von Ammoniak aus Düngemittelproduktion und Tierhaltung können zu Umweltproblemen führen. Die verschiedenen N-O- und N-H-Verbindungen können durch Stickstoffdeposition eine Eutrophierung (Überdüngung) von Böden und Gewässern bewirken. Durch Nitratauswaschung aus überdüngten Böden wird das Grundwasser belastet. Darüber hinaus wirken Stickoxide als Säurebildner („Saurer Regen“). ⓘ
Folgen der menschlichen Veränderung des Stickstoffkreislaufs

In Deutschland werden jährlich im Mittel 20 bis 40 Kilogramm Stickstoff je Hektar über den Luftweg als Stickstoffdeposition eingetragen; zu etwa gleichen Teilen in reduzierter und oxidierter Form. Dieses Überangebot an Stickstoff ist eine Hauptgefährdung der Biodiversität, da an Stickstoffmangel angepasste Arten durch nitrophile Arten verdrängt werden. Über 70 Prozent der in Deutschland auf der Roten Liste stehenden Gefäßpflanzen sind Stickstoff-Mangelanzeiger. Hinzu kommt der Eintrag durch Stickstoffdünger in der Landwirtschaft. ⓘ
Am 28. April 2016 hat die EU-Kommission eine seit Jahren vorbereitete Klage gegen Deutschland wegen der Nicht-Einhaltung der Nitrat-Richtlinie an den Europäischen Gerichtshof übermittelt. Seit Jahren werden in Deutschland die Grenzwerte für Nitrat in Gewässern überschritten. Nach Einschätzung der EU-Kommission unternimmt die Bundesregierung dagegen nicht genug. Die 2016 diskutierte Düngeverordnung gilt als Indiz dafür. ⓘ
Auswirkungen auf natürliche Systeme
Zunehmende Stickstoffeinträge haben nachweislich eine Reihe von negativen Auswirkungen auf terrestrische und aquatische Ökosysteme. Stickstoffgase und -aerosole können für bestimmte Pflanzenarten direkt toxisch sein und die oberirdische Physiologie und das Wachstum von Pflanzen in der Nähe großer punktueller Stickstoffverschmutzungsquellen beeinträchtigen. Es kann auch zu Veränderungen bei den Pflanzenarten kommen, da die Anhäufung von Stickstoffverbindungen deren Verfügbarkeit in einem bestimmten Ökosystem erhöht, wodurch sich schließlich die Artenzusammensetzung, die Pflanzenvielfalt und der Stickstoffkreislauf verändern. Ammoniak und Ammonium - zwei reduzierte Formen des Stickstoffs - können im Laufe der Zeit aufgrund einer erhöhten Toxizität für empfindliche Pflanzenarten schädlich sein, insbesondere für solche, die an Nitrat als Stickstoffquelle gewöhnt sind, was zu einer schlechten Entwicklung ihrer Wurzeln und Triebe führt. Erhöhte Stickstoffeinträge führen auch zu einer Versauerung des Bodens, wodurch die Auslaugung von Basenkationen im Boden und die Menge an Aluminium und anderen potenziell toxischen Metallen zunimmt, während gleichzeitig die Nitrifikation abnimmt und die pflanzliche Streu zunimmt. Aufgrund der anhaltenden Veränderungen, die durch hohe Stickstoffeinträge verursacht werden, kann die Anfälligkeit eines Lebensraums für ökologischen Stress und Störungen - wie Schädlinge und Krankheitserreger - zunehmen, wodurch er weniger widerstandsfähig gegenüber Situationen wird, die ansonsten kaum Auswirkungen auf seine langfristige Vitalität hätten. ⓘ
Weitere Risiken, die sich aus der erhöhten Verfügbarkeit von anorganischem Stickstoff in aquatischen Ökosystemen ergeben, sind die Versauerung des Wassers, die Eutrophierung von Süß- und Salzwassersystemen und die Toxizität für Tiere, einschließlich des Menschen. Eutrophierung führt häufig zu einem niedrigeren Gehalt an gelöstem Sauerstoff in der Wassersäule, einschließlich hypoxischer und anoxischer Bedingungen, die zum Tod der Wasserfauna führen können. Relativ sessile Benthosorganismen oder Bodenlebewesen sind aufgrund ihrer mangelnden Mobilität besonders gefährdet, obwohl große Fischsterben keine Seltenheit sind. Die toten Zonen im Meer nahe der Mündung des Mississippi im Golf von Mexiko sind ein bekanntes Beispiel für eine durch Algenblüten verursachte Hypoxie. Die New Yorker Adirondack-Seen, die Catskills, die Hudson Highlands, das Rensselaer Plateau und Teile von Long Island zeigen die Auswirkungen von Salpetersäureregen, der zum Absterben von Fischen und vielen anderen aquatischen Arten führt. ⓘ
Ammoniak (NH3) ist hochgradig fischgiftig, und die aus Kläranlagen eingeleitete Ammoniakmenge muss genau überwacht werden. Um Fischsterben zu verhindern, ist eine Nitrifikation durch Belüftung vor der Einleitung oft wünschenswert. Die Ausbringung auf dem Land kann eine attraktive Alternative zur Belüftung sein. ⓘ
Auswirkungen auf die menschliche Gesundheit: Nitratanreicherung im Trinkwasser
Die Freisetzung von Nr (reaktivem Stickstoff) durch menschliche Aktivitäten kann zu einer Anreicherung von Nitraten in der natürlichen Wasserumgebung führen, was schädliche Auswirkungen auf die menschliche Gesundheit haben kann. Der übermäßige Einsatz von Stickstoffdünger in der Landwirtschaft ist eine der Hauptursachen für die Nitratverschmutzung des Grund- und Oberflächenwassers. Aufgrund seiner hohen Löslichkeit und geringen Rückhaltefähigkeit im Boden kann Nitrat leicht aus dem Unterboden in das Grundwasser gelangen und so eine Nitratverschmutzung verursachen. Einige andere punktuelle Quellen für die Nitratverschmutzung des Grundwassers stammen aus der Viehfütterung, der Verunreinigung durch Tiere und Menschen sowie aus kommunalen und industriellen Abfällen. Da das Grundwasser häufig als primäre Wasserversorgung für die Haushalte dient, kann die Nitratverschmutzung bei der Trinkwassergewinnung vom Grundwasser auf das Oberflächenwasser und das Trinkwasser übergehen, insbesondere bei der Wasserversorgung kleiner Gemeinden, wo schlecht reguliertes und unhygienisches Wasser verwendet wird. ⓘ
Die WHO-Norm für Trinkwasser liegt bei 50 mg NO-3 L-1 für eine kurzfristige Belastung und bei 3 mg NO-3 L-1 für chronische Auswirkungen. Sobald es in den menschlichen Körper gelangt, kann Nitrat mit organischen Verbindungen durch Nitrosierungsreaktionen im Magen reagieren und Nitrosamine und Nitrosamide bilden, die an einigen Krebsarten beteiligt sind (z. B. Mund- und Magenkrebs). ⓘ
Auswirkungen auf die menschliche Gesundheit: Luftqualität
Menschliche Aktivitäten haben auch den globalen Stickstoffkreislauf durch die Produktion von stickstoffhaltigen Gasen dramatisch verändert, was mit der globalen atmosphärischen Stickstoffverschmutzung einhergeht. Es gibt mehrere Quellen für reaktiven Stickstoff (Nr) in der Atmosphäre. Landwirtschaftliche Quellen von reaktivem Stickstoff können atmosphärische Emissionen von Ammoniak (NH3), Stickoxiden (NOx) und Distickstoffoxid (N2O) erzeugen. Verbrennungsprozesse in der Energieerzeugung, im Verkehr und in der Industrie können durch die Emission von NOx, einem unbeabsichtigten Abfallprodukt, ebenfalls zur Bildung von neuem reaktivem Stickstoff führen. Wenn diese reaktiven Stickstoffe in die untere Atmosphäre freigesetzt werden, können sie zur Bildung von Smog, Feinstaub und Aerosolen führen, die alle wesentlich zu den gesundheitsschädigenden Auswirkungen der Luftverschmutzung auf den Menschen beitragen. In der Atmosphäre kann NO2 zu Salpetersäure (HNO3) oxidiert werden und mit NH3 zu Ammoniumnitrat reagieren, das die Bildung von besonderem Nitrat begünstigt. Außerdem kann NH3 mit anderen sauren Gasen (Schwefel- und Salzsäure) reagieren und ammoniumhaltige Partikel bilden, die die Vorläufer der sekundären organischen Aerosolpartikel im photochemischen Smog sind. ⓘ
Schritte des Stickstoffkreislaufes
Nitrifikation
In einem zweistufigen, aerob verlaufenden Prozess können zwei Gruppen von Bakterien, Nitritbakterien (z. B. Nitrosomonas) und Nitratbakterien (z. B. Nitrobacter), unter Energiegewinn Ammoniak über die Zwischenstufe Nitrit zu Nitrat oxidieren:
Ammonifikation
Durch Primärproduzenten sowie Primär- und Sekundärkonsumenten (s. Nahrungskette) wird ständig organisches Material in Form stickstoffhaltiger Exkremente oder abgestorbener Materie produziert. Den darin enthaltenen Stickstoff können Destruenten (Zersetzer) wie Pilze und Bakterien) als Ammoniak (NH3) bzw. als Ammonium-Ionen (NH4+) freisetzen. Diese stehen dann dem Ökosystem als anorganische Mineralstoffe zur Verfügung und können von autotrophen Organismen (Pflanzen u. a.) verwertet werden. ⓘ