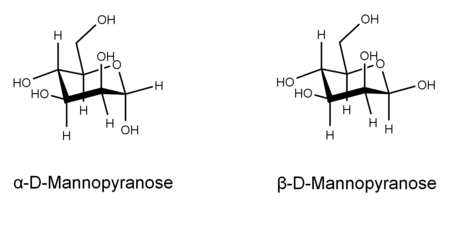Mannose
| Strukturformel ⓘ | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||
| Fischer-Projektion, offenkettige Darstellung | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Mannose | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C6H12O6 | ||||||||||||
| Kurzbeschreibung |
farb- und geruchloses, kristallines Pulver | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 180,16 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Dichte |
1,54 g·cm−3 (D-Mannose) | ||||||||||||
| Schmelzpunkt |
| ||||||||||||
| Löslichkeit |
| ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Mannose, in biochemischer Darstellung häufig mit Man abgekürzt, ist ein Epimer der Glucose, genauer gesagt ein C2-Epimer. Als D-Mannose ist es eine natürliche Hexose und Baustein zahlreicher pflanzlicher Polysaccharide (Mannane). Im Organismus ist es hauptsächlich Bestandteil von Membranen. Bezogen auf Saccharose hat eine 10%ige Lösung eine Süßkraft von 59 %. ⓘ
Der Name ist abgeleitet von Mannit, näheres zur Etymologie findet sich im entsprechenden Artikel. ⓘ
Wenn in diesem Text oder in der wissenschaftlichen Literatur „Mannose“ ohne weiteren Namenszusatz (Präfix) erwähnt wird, ist D-Mannose gemeint. Die (unnatürliche) L-Mannose ist synthetisch zugänglich und besitzt nur untergeordnete Bedeutung. ⓘ
 D-Mannopyranose
| |
 Fischer-Projektionen
| |
| Bezeichner | |
|---|---|
| ChEMBL | |
| ChemSpider |
|
IUPHAR/BPS
|
|
| MeSH | Mannose |
PubChem CID
|
|
| UNII | |
| Eigenschaften | |
Chemische Formel
|
C6H12O6 |
| Molare Masse | 180.156 g-mol-1 |
Magnetische Suszeptibilität (χ)
|
-102,90-10-6 cm3/mol |
Wenn nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
Mannose ist ein Zuckermonomer aus der Aldohexose-Reihe der Kohlenhydrate. Es handelt sich um ein C-2-Epimer der Glucose. Mannose spielt im menschlichen Stoffwechsel eine wichtige Rolle, insbesondere bei der Glykosylierung bestimmter Proteine. Mehrere angeborene Störungen der Glykosylierung werden mit Mutationen in Enzymen in Verbindung gebracht, die am Mannosestoffwechsel beteiligt sind. ⓘ
Mannose ist kein essenzieller Nährstoff; sie kann im menschlichen Körper aus Glukose hergestellt oder in Glukose umgewandelt werden. Mannose liefert 2-5 kcal/g. Sie wird teilweise mit dem Urin ausgeschieden. ⓘ
Verhalten in wässriger Lösung
In wässriger Lösung kommt es teilweise zu einem intramolekularen Ringschluss, sodass sich ein Gleichgewicht zwischen der Aldehydform und den beiden Ringformen (Furanose-Form und Pyranose-Form) einstellt, wobei die Mannose dann fast ausschließlich in der Pyranoseform vorliegt:
ⓘD-Mannose – Schreibweisen Keilstrichformel Haworth-Schreibweise 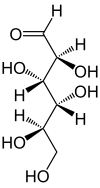

α-D-Mannofuranose
<1 %
β-D-Mannofuranose
<1 %
α-D-Mannopyranose
67 %
β-D-Mannopyranose
33 %Sesselkonformation
Mannose besteht im Allgemeinen aus zwei unterschiedlich großen Ringen, der Pyranose (sechsgliedrig) und der Furanose (fünfgliedrig). Jeder Ringschluss kann entweder eine Alpha- oder Beta-Konfiguration an der anomeren Position aufweisen. Die Chemikalie unterliegt einer schnellen Isomerisierung zwischen diesen vier Formen. ⓘ
Stoffwechsel

Während man annimmt, dass ein Großteil der für die Glykosylierung verwendeten Mannose aus Glukose stammt, wird in kultivierten Hepatomzellen (Krebszellen aus der Leber) der Großteil der Mannose für die Glykoproteinbiosynthese aus extrazellulärer Mannose und nicht aus Glukose gewonnen. Viele der in der Leber produzierten Glykoproteine werden in den Blutkreislauf ausgeschieden, so dass die mit der Nahrung aufgenommene Mannose im ganzen Körper verteilt wird. ⓘ
Mannose ist in zahlreichen Glykokonjugaten enthalten, einschließlich der N-gebundenen Glykosylierung von Proteinen. Auch C-Mannosylierung ist reichlich vorhanden und kann in kollagenartigen Regionen gefunden werden. ⓘ
Bei der Verdauung vieler Polysaccharide und Glykoproteine entsteht Mannose, die durch Hexokinase phosphoryliert wird, um Mannose-6-Phosphat zu erzeugen. Mannose-6-phosphat wird durch das Enzym Phosphomannose-Isomerase in Fructose-6-phosphat umgewandelt und gelangt dann in den glykolytischen Stoffwechselweg oder wird durch den glukoneogenen Stoffwechselweg der Hepatozyten in Glucose-6-phosphat umgewandelt. ⓘ
Mannose ist ein dominierendes Monosaccharid bei der N-gebundenen Glykosylierung, einer posttranslationalen Modifikation von Proteinen. Sie wird durch den En-bloc-Transfer von Glc3Man9GlcNAc2 auf naszierende Glykoproteine im endoplasmatischen Retikulum in einer kotranslationalen Weise eingeleitet, wenn das Protein durch das Transportsystem gelangt. Glukose wird an vollständig gefalteten Proteinen hydrolysiert, und die Mannoseeinheiten werden von Mannosidasen im ER und in den Golgi-Gefäßen hydrolysiert. Reife menschliche Glykoproteine enthalten in der Regel nur drei Mannosereste, die nacheinander durch GlcNAc, Galaktose und Sialinsäure modifiziert werden. Dies ist wichtig, da das angeborene Immunsystem von Säugetieren darauf ausgerichtet ist, freiliegende Mannosereste zu erkennen. Diese Aktivität ist auf das Vorkommen von Mannoseresten in Form von Mannanen auf der Oberfläche von Hefen zurückzuführen. Das humane Immundefizienzvirus weist aufgrund der engen Anhäufung von Glykanen in seinem viralen Spike eine beträchtliche Menge an Mannoseresten auf. Diese Mannosereste sind das Ziel für breit neutralisierende Antikörper. ⓘ
Biotechnologie
In Hefe produzierte rekombinante Proteine können einer Mannoseaddition unterliegen, die sich von der in Säugetierzellen verwendeten unterscheidet. Dieser Unterschied zwischen rekombinanten Proteinen und solchen, die normalerweise in Säugetierorganismen produziert werden, kann die Wirksamkeit von Impfstoffen beeinflussen. ⓘ
Bildung
Mannose kann durch die Oxidation von Mannitol gebildet werden. ⓘ
Sie kann auch durch die Lobry-de Bruyn-van Ekenstein-Transformation aus Glucose gebildet werden. ⓘ
Etymologie
Mannose" und Mannitol" haben ihren Ursprung im Manna, das in der Bibel als die Nahrung der Israeliten während ihrer Reise in die Region Sinai beschrieben wird. Mehrere Bäume und Sträucher können eine als Manna bezeichnete Substanz produzieren, wie z. B. der "Manna-Baum" (Fraxinus ornus), aus dessen Absonderungen Mannitol ursprünglich isoliert wurde. ⓘ
Verwendungen
Mannose (D-Mannose) wird als Nahrungsergänzungsmittel, verpackt als "D-Mannose", zur Vorbeugung wiederkehrender Harnwegsinfektionen verwendet. Obwohl bis zum Jahr 2022 nur wenige Studien durchgeführt wurden, scheint die Einnahme von Mannose Infektionen ebenso gut zu verhindern wie vorbeugende Antibiotika, und das bei minimalen Nebenwirkungen. ⓘ
Aufbau
Mannose unterscheidet sich von Glucose durch die Umkehrung des chiralen C-2-Zentrums. Mannose zeigt eine Falten in der Ringform der Lösung. Diese einfache Änderung führt zu der drastisch unterschiedlichen Biochemie der beiden Hexosen. Diese Veränderung hat auch auf die anderen Aldohexosen die gleiche Wirkung. ⓘ
Mannose-PTS-Permease

Das PEP-abhängige zuckertransportierende Phosphotransferase-System transportiert und phosphoryliert gleichzeitig seine Zuckersubstrate. Die Mannose-XYZ-Permease ist ein Mitglied dieser Familie. Diese besondere Methode wird von Bakterien für die Aufnahme von Zuckern verwendet, insbesondere von exogenen Hexosen im Fall von Mannose XYZ, um die Phosphatester in das Zellzytoplasma freizusetzen und den Stoffwechsel hauptsächlich über den Weg der Glykolyse vorzubereiten. Der MANXYZ-Transporterkomplex ist auch an der Infektion von E. coli durch den Bakteriophagen Lambda beteiligt, wobei die Untereinheiten ManY und ManZ für eine ordnungsgemäße Infektion durch den Lambda-Phagen ausreichen. MANXYZ verfügt über vier Domänen in drei Polypeptidketten: ManX, ManY und ManZ. Die Untereinheit ManX bildet ein Homodimer, das auf der zytoplasmatischen Seite der Membran lokalisiert ist. ManX enthält zwei Domänen IIA und IIB, die durch ein Scharnierpeptid verbunden sind, wobei jede Domäne eine Phosphorylierungsstelle enthält und der Phosphoryltransfer zwischen beiden Untereinheiten stattfindet. ManX kann membrangebunden sein oder nicht. Bei den Untereinheiten ManY und ManNZ handelt es sich um hydrophobe integrale Membranproteine mit sechs und einem transmembranen alpha-helikalen Spanner(n). Die Phosphorylgruppe von PEP wird über Enzym 1, den Histidin-Proteinphosphat-Träger, auf den importierten Zucker übertragen und dann auf die Untereinheiten ManX, ManY und ManZ des ManXYZ-Transportkomplexes, der den eintretenden Hexosezucker phosphoryliert und ein Hexose-6-Phosphat bildet. ⓘ
Eigenschaften
GDP-Mannose
Eine Besonderheit der Mannose ist, dass ihre Aktivierung nicht über Uridintriphosphat (UTP), sondern über Guanosintriphosphat (GTP) erfolgt. Hierzu wird zuerst Mannose-6-phosphat zu Mannose-1-phosphat umgewandelt, welches dann weiter zur GDP-Mannose reagiert. Die Reaktionsfolge ist hierbei dieselbe wie bei der Reaktion von Glucose zu UDP-Glucose und bei der Glycogensynthese. ⓘ
Toxizität für Insekten
Während Mannose für den Menschen nahezu ungiftig ist, besitzt diese für verschiedene Hautflügler wie Bienen (zu denen auch die Hummeln gehören) und die Gemeine Wespe Vespa vulgaris eine hohe Toxizität. Bei Bienen wurde eine Letale Dosis von 0,4–0,5 mg ermittelt. Die Giftwirkung beruht auf der Ähnlichkeit der Mannose zu Glucose, die zu einer kompetitiven Hemmung verschiedener Enzyme führt. ⓘ
Verwendung in der Medizin
Laut zweier Studien kann D-Mannose zur Prophylaxe von Blasenentzündungen eingesetzt werden. Andere Publikationen zweifeln diese Aussage jedoch an. ⓘ