Rost
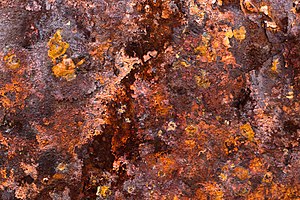
| Stähle ⓘ |
|---|
 |
| Phasen |
|
| Gefüge |
|
| Klassen |
|
| Andere Eisenwerkstoffe |
|
Rost ist ein Eisenoxid, ein meist rötlich-braunes Oxid, das durch die Reaktion von Eisen und Sauerstoff in katalytischer Gegenwart von Wasser oder Luftfeuchtigkeit entsteht. Rost besteht aus wasserhaltigen Eisen(III)-Oxiden (Fe2O3-nH2O) und Eisen(III)-Oxid-Hydroxid (FeO(OH), Fe(OH)3) und ist typischerweise mit der Korrosion von Roheisen verbunden. ⓘ
Wenn genügend Zeit vergeht, kann sich jede Eisenmasse in Gegenwart von Wasser und Sauerstoff schließlich vollständig in Rost umwandeln. Oberflächenrost ist in der Regel schuppig und brüchig und bietet dem darunter liegenden Eisen keinen passiven Schutz, anders als die Bildung von Patina auf Kupferoberflächen. Rost ist der allgemeine Begriff für die Korrosion von elementarem Eisen und seinen Legierungen wie Stahl. Viele andere Metalle unterliegen einer ähnlichen Korrosion, aber die dabei entstehenden Oxide werden im Allgemeinen nicht als "Rost" bezeichnet. ⓘ
Es gibt verschiedene Formen von Rost, die sowohl visuell als auch durch Spektroskopie unterschieden werden können und sich unter unterschiedlichen Umständen bilden. Andere Formen von Rost sind das Ergebnis von Reaktionen zwischen Eisen und Chlorid in einer sauerstoffarmen Umgebung. Ein Beispiel ist der in Unterwasserbetonpfeilern verwendete Bewehrungsstahl, der Grünrost bildet. Obwohl das Rosten im Allgemeinen ein negativer Aspekt von Eisen ist, führt eine besondere Form des Rostens, der so genannte stabile Rost, dazu, dass das Objekt eine dünne Rostschicht auf der Oberseite aufweist. Bei niedriger relativer Luftfeuchtigkeit schützt diese "stabile" Schicht das darunter liegende Eisen, jedoch nicht in dem Maße wie andere Oxide, z. B. Aluminiumoxid auf Aluminium. ⓘ



Als Rost bezeichnet man das Korrosionsprodukt, das aus Eisen oder Stahl durch Oxidation mit Sauerstoff in Gegenwart von Wasser entsteht. Rost ist porös und schützt nicht vor weiterer Zersetzung, anders als die Oxidschicht anderer metallischer Werkstoffe wie bei Chrom, Aluminium oder Zink oder beim nur oberflächlich verrosteten Cortenstahl. Anhand dieser Eigenschaften werden die Metalle in die Gruppen Eisenmetalle (rosten) und Nichteisenmetalle (rosten nicht) unterschieden. ⓘ
Chemische Reaktionen



Rost ist eine allgemeine Bezeichnung für einen Komplex aus Eisenoxiden und -hydroxiden, der entsteht, wenn Eisen oder einige eisenhaltige Legierungen über einen längeren Zeitraum hinweg Sauerstoff und Feuchtigkeit ausgesetzt sind. Im Laufe der Zeit verbindet sich der Sauerstoff mit dem Metall und bildet neue Verbindungen, die allgemein als Rost bezeichnet werden. Obwohl Rost im Allgemeinen als "Oxidation" bezeichnet wird, ist dieser Begriff viel allgemeiner und beschreibt eine Vielzahl von Prozessen, bei denen es im Rahmen einer Reaktion zum Verlust von Elektronen oder zu einer Erhöhung der Oxidationsstufe kommt. Bei den bekanntesten dieser Reaktionen ist Sauerstoff beteiligt, daher der Name "Oxidation". Die Begriffe "Rost" und "rosten" bezeichnen nur die Oxidation von Eisen und die dabei entstehenden Produkte. Es gibt viele andere Oxidationsreaktionen, an denen kein Eisen beteiligt ist und die keinen Rost erzeugen. Aber nur Eisen oder eisenhaltige Legierungen können rosten. Andere Metalle können jedoch auf ähnliche Weise korrodieren. ⓘ
Der Hauptkatalysator für den Rostprozess ist Wasser. Eisen- oder Stahlstrukturen scheinen zwar fest zu sein, aber Wassermoleküle können in die mikroskopisch kleinen Gruben und Risse in jedem freiliegenden Metall eindringen. Die in den Wassermolekülen enthaltenen Wasserstoffatome können sich mit anderen Elementen zu Säuren verbinden, die schließlich dazu führen, dass mehr Metall freigelegt wird. Wenn Chloridionen vorhanden sind, wie es bei Salzwasser der Fall ist, wird die Korrosion wahrscheinlich noch schneller voranschreiten. In der Zwischenzeit verbinden sich die Sauerstoffatome mit Metallatomen und bilden die zerstörerische Oxidverbindung. Wenn sich die Atome verbinden, schwächen sie das Metall und machen die Struktur spröde und brüchig. ⓘ
Oxidation von Eisen
Wenn Eisen mit Wasser und Sauerstoff in Berührung kommt, rostet es. Bei Vorhandensein von Salz, z. B. in Meerwasser oder Salzsprühnebel, rostet das Eisen aufgrund chemischer Reaktionen schneller. Von reinem Wasser oder trockenem Sauerstoff wird Eisenmetall relativ wenig angegriffen. Wie bei anderen Metallen, z. B. Aluminium, schützt eine fest haftende Oxidschicht, eine Passivierungsschicht, das massive Eisen vor weiterer Oxidation. Die Umwandlung der passivierenden Eisenoxidschicht in Rost erfolgt durch die kombinierte Wirkung von zwei Stoffen, in der Regel Sauerstoff und Wasser. ⓘ
Andere zersetzende Lösungen sind Schwefeldioxid in Wasser und Kohlendioxid in Wasser. Unter diesen korrosiven Bedingungen bilden sich Eisenhydroxide. Im Gegensatz zu Eisenoxiden haften die Hydroxide nicht an der Metallmasse. Wenn sie sich bilden und von der Oberfläche abplatzen, wird frisches Eisen freigelegt, und der Korrosionsprozess setzt sich fort, bis entweder das gesamte Eisen verbraucht ist oder der gesamte Sauerstoff, das Wasser, das Kohlendioxid oder das Schwefeldioxid im System entfernt oder verbraucht sind. ⓘ
Wenn Eisen rostet, nehmen die Oxide mehr Volumen ein als das ursprüngliche Metall; diese Ausdehnung kann enorme Kräfte erzeugen, die die aus Eisen gefertigten Strukturen beschädigen. Weitere Einzelheiten finden Sie unter Wirtschaftlicher Effekt. ⓘ
Assoziierte Reaktionen
Das Rosten von Eisen ist ein elektrochemischer Prozess, der mit der Übertragung von Elektronen von Eisen auf Sauerstoff beginnt. Das Eisen ist das Reduktionsmittel (gibt Elektronen ab), während der Sauerstoff das Oxidationsmittel ist (nimmt Elektronen auf). Die Korrosionsgeschwindigkeit wird durch Wasser beeinflusst und durch Elektrolyte beschleunigt, wie die Auswirkungen von Streusalz auf die Korrosion von Automobilen zeigen. Die wichtigste Reaktion ist die Reduktion von Sauerstoff:
- O2 + 4 e- + 2 H2O → 4 OH-
Da er Hydroxidionen bildet, wird dieser Prozess durch die Anwesenheit von Säure stark beeinträchtigt. Ebenso wird die Korrosion der meisten Metalle durch Sauerstoff bei niedrigem pH-Wert beschleunigt. Die Bereitstellung der Elektronen für die obige Reaktion ist die Oxidation von Eisen, die wie folgt beschrieben werden kann:
- Fe → Fe2+ + 2 e- ⓘ
Die folgende Redoxreaktion findet ebenfalls in Gegenwart von Wasser statt und ist entscheidend für die Bildung von Rost:
- 4 Fe2+ + O2 → 4 Fe3+ + 2 O2- ⓘ
Darüber hinaus beeinflussen die folgenden mehrstufigen Säure-Base-Reaktionen den Verlauf der Rostbildung:
- Fe2+ + 2 H2O ⇌ Fe(OH)2 + 2 H+
- Fe3+ + 3 H2O ⇌ Fe(OH)3 + 3 H+ ⓘ
sowie die folgenden Dehydratisierungsgleichgewichte:
Aus den obigen Gleichungen ist auch ersichtlich, dass die Korrosionsprodukte von der Verfügbarkeit von Wasser und Sauerstoff abhängen. Bei begrenztem gelöstem Sauerstoff werden eisen(II)-haltige Stoffe begünstigt, darunter FeO und schwarzer lodestone oder Magnetit (Fe3O4). Hohe Sauerstoffkonzentrationen begünstigen eisenhaltige Materialien mit den Nennformeln Fe(OH)3-xOx⁄2. Die Art des Rostes ändert sich mit der Zeit, was die langsamen Reaktionsgeschwindigkeiten von Feststoffen widerspiegelt. ⓘ
Darüber hinaus werden diese komplexen Prozesse durch das Vorhandensein anderer Ionen wie Ca2+ beeinflusst, die als Elektrolyte dienen und die Rostbildung beschleunigen oder sich mit den Eisenhydroxiden und -oxiden verbinden, um eine Vielzahl von Ca-, Fe-, O- und OH-Arten auszufällen. ⓘ
Der Beginn der Rostbildung kann auch im Labor mit Hilfe einer Ferroxyl-Indikatorlösung nachgewiesen werden. Die Lösung weist sowohl Fe2+-Ionen als auch Hydroxyl-Ionen nach. Die Bildung von Fe2+-Ionen und Hydroxyl-Ionen wird durch blaue bzw. rosa Flecken angezeigt. ⓘ
Vorbeugung
Aufgrund der weiten Verbreitung und Bedeutung von Eisen- und Stahlerzeugnissen ist die Vorbeugung oder Verlangsamung von Rost die Grundlage wichtiger wirtschaftlicher Aktivitäten in einer Reihe von Spezialtechnologien. Hier wird ein kurzer Überblick über die Methoden gegeben; ausführliche Informationen finden Sie in den Artikeln, auf die mit Querverweisen verwiesen wird. ⓘ
Da Rost luft- und wasserdurchlässig ist, korrodiert das innere metallische Eisen unter einer Rostschicht weiter. Zur Vermeidung von Rost sind daher Beschichtungen erforderlich, die die Rostbildung verhindern. ⓘ
Rostbeständige Legierungen
Rostfreier Stahl bildet eine Passivierungsschicht aus Chrom(III)-oxid. Ein ähnliches Passivierungsverhalten zeigen Magnesium, Titan, Zink, Zinkoxide, Aluminium, Polyanilin und andere elektroaktive leitfähige Polymere. ⓘ
Spezielle "witterungsbeständige Stahllegierungen" wie Cor-Ten rosten viel langsamer als normal, weil der Rost in einer Schutzschicht an der Metalloberfläche haftet. Bei Konstruktionen aus diesem Material müssen Maßnahmen getroffen werden, die den schlimmsten Fall vermeiden, da das Material auch unter nahezu idealen Bedingungen langsam weiterrostet. ⓘ
Verzinkung

Bei der Galvanisierung wird auf das zu schützende Objekt eine Schicht aus metallischem Zink aufgetragen, entweder durch Feuerverzinken oder durch Galvanisieren. Zink wird traditionell verwendet, weil es billig ist, gut auf Stahl haftet und im Falle einer Beschädigung der Zinkschicht einen kathodischen Schutz der Stahloberfläche bietet. In korrosiveren Umgebungen (z. B. Salzwasser) wird die Kadmiumbeschichtung bevorzugt. Die Verzinkung versagt oft an Nähten, Löchern und Verbindungen, wo die Beschichtung Lücken aufweist. In diesen Fällen bietet die Beschichtung immer noch einen teilweisen kathodischen Schutz für Eisen, indem sie als galvanische Anode wirkt und selbst korrodiert, anstatt das darunter liegende geschützte Metall zu schützen. Die schützende Zinkschicht wird dabei verbraucht, so dass die Verzinkung nur für einen begrenzten Zeitraum Schutz bietet. ⓘ
Modernere Beschichtungen fügen der Beschichtung Aluminium als Zink-Aluminium hinzu; das Aluminium wandert und deckt Kratzer ab, so dass der Schutz länger anhält. Diese Ansätze beruhen darauf, dass die Aluminium- und Zinkoxide eine einmal zerkratzte Oberfläche schützen und nicht wie bei herkömmlichen galvanischen Überzügen als Opferanode oxidieren. In einigen Fällen, z. B. in sehr aggressiven Umgebungen oder bei langer Lebensdauer, werden sowohl Zink als auch eine Beschichtung aufgetragen, um einen besseren Korrosionsschutz zu gewährleisten. ⓘ
Die typische Verzinkung von Stahlerzeugnissen, die der normalen täglichen Bewitterung im Freien ausgesetzt sind, besteht aus einer feuerverzinkten 85-µm-Beschichtung. Unter normalen Witterungsbedingungen verschlechtert sich dieser Überzug mit einer Rate von 1 µm pro Jahr, so dass der Schutz etwa 85 Jahre lang erhalten bleibt. ⓘ
Kathodischer Schutz
Der kathodische Schutz ist eine Technik zur Verhinderung von Korrosion an eingegrabenen oder eingetauchten Strukturen durch Zuführung einer elektrischen Ladung, die die elektrochemische Reaktion unterdrückt. Bei richtiger Anwendung kann die Korrosion vollständig gestoppt werden. In seiner einfachsten Form wird er durch das Anbringen einer Opferanode erreicht, wodurch das Eisen oder der Stahl zur Kathode in der gebildeten Zelle wird. Die Opferanode muss aus einem Material bestehen, dessen Elektrodenpotential negativer ist als das des Eisens oder Stahls, in der Regel Zink, Aluminium oder Magnesium. Die Opferanode wird mit der Zeit korrodieren und ihre Schutzwirkung aufgeben, wenn sie nicht rechtzeitig ersetzt wird. ⓘ
Der kathodische Schutz kann auch durch Anlegen eines elektrischen Stroms erfolgen. Dies wird dann als ICCP (Impressed Current Cathodic Protection) bezeichnet. ⓘ
Beschichtungen und Anstriche

Die Rostbildung lässt sich mit Beschichtungen wie Farbe, Lack, Firnis oder Wachsbändern eindämmen, die das Eisen von der Umgebung isolieren. Bei großen Konstruktionen mit geschlossenen Kastenprofilen, wie z. B. bei Schiffen und modernen Autos, wird häufig ein Produkt auf Wachsbasis (technisch gesehen ein Slush-Öl") in diese Profile gespritzt. Solche Behandlungen enthalten in der Regel auch Rostschutzmittel. Die Bedeckung von Stahl mit Beton kann aufgrund des alkalischen pH-Werts an der Schnittstelle zwischen Stahl und Beton einen gewissen Schutz für den Stahl bieten. Das Rosten von Stahl in Beton kann jedoch immer noch ein Problem darstellen, da sich ausbreitender Rost den Beton von innen heraus aufbrechen kann. ⓘ
Ein ähnliches Beispiel ist die Verwendung von Eisenklammern zur Verbindung von Marmorblöcken bei der Restaurierung des Parthenon in Athen, Griechenland, im Jahr 1898, die jedoch durch das Rosten und Aufquellen des ungeschützten Eisens den Marmor stark beschädigte. Die griechischen Baumeister der Antike hatten beim Bau ein ähnliches Befestigungssystem für die Marmorblöcke verwendet, allerdings gossen sie zusätzlich geschmolzenes Blei über die Eisenverbindungen, um sie vor seismischen Erschütterungen und Korrosion zu schützen. Diese Methode war bei dem 2500 Jahre alten Bauwerk erfolgreich, doch in weniger als einem Jahrhundert drohten die groben Reparaturen einzustürzen. ⓘ

Wenn nur ein vorübergehender Schutz für die Lagerung oder den Transport erforderlich ist, kann eine dünne Schicht Öl, Fett oder eine spezielle Mischung wie Cosmoline auf eine Eisenoberfläche aufgetragen werden. Solche Behandlungen werden häufig verwendet, wenn ein Stahlschiff, ein Auto oder eine andere Ausrüstung für eine langfristige Lagerung "eingemottet" wird. ⓘ
Es gibt spezielle Schmiermittelmischungen gegen Festfressen, die auf Metallgewinde und andere präzisionsbearbeitete Oberflächen aufgetragen werden, um sie vor Rost zu schützen. Diese Mischungen enthalten in der Regel Fett, das mit Kupfer-, Zink- oder Aluminiumpulver und anderen geschützten Bestandteilen vermischt ist. ⓘ
Bläuen
Das Bläuen ist eine Technik, die kleinen Stahlteilen, wie z. B. Schusswaffen, einen begrenzten Schutz vor Rost bieten kann; um erfolgreich zu sein, wird ein wasserverdrängendes Öl auf den gebläuten Stahl und anderen Stahl gerieben. ⓘ
Inhibitoren
Korrosionsinhibitoren, wie z. B. Gasphaseninhibitoren oder flüchtige Inhibitoren, können verwendet werden, um Korrosion in geschlossenen Systemen zu verhindern. Sie sind nicht wirksam, wenn die Luftzirkulation sie zerstreut und frischen Sauerstoff und Feuchtigkeit einbringt. ⓘ
Kontrolle der Luftfeuchtigkeit
Rost kann vermieden werden, indem die Feuchtigkeit in der Atmosphäre kontrolliert wird. Ein Beispiel hierfür ist die Verwendung von Kieselgelpaketen zur Kontrolle der Luftfeuchtigkeit in Geräten, die auf dem Seeweg transportiert werden. ⓘ
Behandlung
Rostentfernung von kleinen Eisen- oder Stahlgegenständen durch Elektrolyse kann in einer Heimwerkstatt mit einfachen Mitteln durchgeführt werden, z. B. mit einem Plastikeimer, der mit einem Elektrolyt gefüllt ist, der aus in Leitungswasser aufgelöstem Waschsoda besteht, einem senkrecht in der Lösung aufgehängten Bewehrungsstab, der als Anode dient, ein weiteres, quer über die Oberseite des Eimers gelegtes Stück Betonstahl, das als Stütze für die Aufhängung des Gegenstands dient, Ballenpressdraht zum Aufhängen des Gegenstands in der Lösung am waagerechten Betonstahl und ein Batterieladegerät als Stromquelle, bei dem der Pluspol an die Anode und der Minuspol an den zu behandelnden Gegenstand geklemmt wird, der zur Kathode wird. ⓘ
Rost kann mit handelsüblichen Produkten behandelt werden, die als Rostumwandler bekannt sind und Gerbsäure oder Phosphorsäure enthalten, die sich mit dem Rost verbindet; er kann mit organischen Säuren wie Zitronensäure und Essig oder der stärkeren Salzsäure entfernt werden; oder er kann mit Chelatbildnern, wie sie in einigen handelsüblichen Formulierungen enthalten sind, oder sogar mit einer Melasselösung entfernt werden. ⓘ
Wirtschaftliche Auswirkungen

Rost ist mit der Zersetzung von Werkzeugen und Konstruktionen aus Eisen verbunden. Da Rost ein viel größeres Volumen hat als die ursprüngliche Eisenmasse, kann seine Anhäufung auch zum Versagen führen, indem er benachbarte Teile auseinander drückt - ein Phänomen, das manchmal als "Rostpackung" bezeichnet wird. Dieses Phänomen war die Ursache für den Einsturz der Mianus-Brücke im Jahr 1983, als die Lager von innen rosteten und eine Ecke der Fahrbahnplatte von ihrem Träger abdrückten. ⓘ
Rost war ein wichtiger Faktor bei der Silver Bridge-Katastrophe von 1967 in West Virginia, als eine Hängebrücke aus Stahl in weniger als einer Minute zusammenbrach und 46 Fahrer und Passagiere auf der Brücke ums Leben kamen. Die Kinzua-Brücke in Pennsylvania wurde 2003 von einem Tornado zum Einsturz gebracht, was vor allem darauf zurückzuführen war, dass die zentralen Grundbolzen, die das Bauwerk am Boden hielten, weggerostet waren und die Brücke nur noch durch die Schwerkraft verankert war. ⓘ
Auch Stahlbeton ist anfällig für Rostschäden. Der Innendruck, der durch die sich ausbreitende Korrosion des betonummantelten Stahls und Eisens verursacht wird, kann zum Abplatzen des Betons führen, was schwere strukturelle Probleme verursacht. Dies ist eine der häufigsten Versagensarten bei Brücken und Gebäuden aus Stahlbeton. ⓘ
- Durch Rost verursachte strukturelle Mängel
Die eingestürzte Silver Bridge, von der Ohio-Seite aus gesehen
Verrostete und entsteinte Streben der 70 Jahre alten Nandu River Iron Bridge ⓘ
Kulturelle Symbolik
Rost ist eine gängige Metapher für den langsamen Verfall aufgrund von Vernachlässigung, da er robustes Eisen- und Stahlmetall allmählich in ein weiches, bröckelndes Pulver verwandelt. Ein großer Teil des industrialisierten Mittleren Westens und Nordostens der USA, der einst von Stahlgießereien, der Automobilindustrie und anderen Herstellern dominiert wurde, hat harte wirtschaftliche Einschnitte erlebt, die der Region den Beinamen "Rust Belt" eingebracht haben. ⓘ
In Musik, Literatur und Kunst wird Rost mit Bildern von verblasstem Ruhm, Vernachlässigung, Verfall und Ruin assoziiert. ⓘ
Elektrochemisches Modell der Rostbildung

Die Rostbildung (Korrosion) an Eisen beginnt durch den Angriff
- einer Säure (Säurekorrosion) oder
- von Sauerstoff und Wasser (Sauerstoffkorrosion)
auf die Metalloberfläche. ⓘ
Beschleunigende Faktoren bei der Rostbildung
Wenn Eisen mit einem anderen Metall in Berührung kommt, entsteht an der Kontaktstelle ein Lokalelement, das zur Korrosion des unedleren Metalls führt. Der Rostvorgang wird zudem durch die Anwesenheit von Salzen beschleunigt, da diese die Leitfähigkeit des Wassers erhöhen. Die Wanderung der Ionen im Wasser ist wichtig für den Korrosionsprozess, andernfalls wäre der Stromkreis unterbrochen und die Korrosion käme sehr schnell zum Erliegen (vgl. Salzbrücke in einer normalen elektrochemischen Zelle). ⓘ
Entrostung

Stark gerostete Metalle können durch Bürsten oder Schleifen von Rost befreit werden. Eine der wirkungsvollsten Methoden für die Entrostung ist das Strahlen mit Sand oder ähnlichen Materialien, die frei von Kieselsäure sind. Diese Methode wird in der Technik vor einem Anstrich überwiegend angewendet. Ist die Sandstrahlmethode nicht ausreichend, kann auch der pneumatische Nadelentroster zum Einsatz kommen. Die vollständige Entfernung von Rost bis auf das blanke Metall ist eine der Voraussetzungen, dass ein korrosionsbeständiger Anstrich erreicht werden kann. ⓘ
Leichter Rost lässt sich auch mit einer schwachen Säure abwaschen. Geeignet ist beispielsweise verdünnte Phosphorsäure. Damit die Säure das Metall nicht angreift, muss sie danach mit viel Wasser abgespült werden. Das Metall muss gründlich getrocknet und vor weiterer Korrosion geschützt werden. Phosphorsäure dient auch als Rostumwandler und wird in verschiedenen Mischungen für die Instandsetzung etwa von Autos eingesetzt. ⓘ
Bei all diesen Methoden zur Entrostung wird der Rost entfernt, der rostige Abtrag geht verloren. ⓘ
Korrosionsschutz
Aus dem Modell lassen sich drei Strategien für den Korrosionsschutz ableiten: ⓘ
Fernhalten von Feuchtigkeit
Da Wasser als Elektrolyt in der Reaktion zur Rostentwicklung wirkt, ist das Trockenhalten eine gute Gegenstrategie. So gibt es beispielsweise in Gegenden mit geringer Luftfeuchtigkeit praktisch keine Rostschäden an Autos. ⓘ
Pipelinerohre und auch die Stahlblechwickel um Bleikabel (bis etwa 1970 für Telefon und Elektrizität) wurden mit bitumengefüllten Jutematten bzw. -streifen belegt, um Benetzung mit Wasser im Erdreich zu verhindern. Noch heute werden die besonders korrosionsgefährdeten Stellen, wo Ampel- oder Leuchtenmasten oder auch Erdungsstangen etwa den Gehsteig durchdringen, mit bituminöser, fetter oder betonierter Umhüllung versehen. ⓘ
Eine weitere Möglichkeit sind Schutzschichten aus Fett, Lack, Chrom oder Metallauflagen (Metallische Überzüge), die das Eisen von der Umgebung abschirmen (Feuerverzinken, Weißblech). Sobald diese Schutzschicht zerstört wird, beginnt der Rostungsprozess. ⓘ
Nichtrostender Stahl ist eine Eisenlegierung mit einem Chromanteil von mehr als 12 % und wird durch die Chromoxidschicht vor Oxidation geschützt. ⓘ
Abbau der Potenzialdifferenz in Lokalelementen
Beispiel 1: Feuerverzinkung schützt Eisen nachhaltig vor Rostbefall. Kommt es zu einer Schädigung der Beschichtung, bilden Zink und Eisen bei Zutritt von Wasser ein Lokalelement (ähnlich einer Batterie). Zink als das unedlere Metall korrodiert und bewahrt das Eisen vor Oxidation. In den meisten Zinkstaubfarben („Zinkspray“) kann das Zink dagegen nicht galvanisch wirken, da es vom Bindemittel isoliert wird. Nur Zinkstaubfarben mit elektrisch leitendem Bindemittel oder Zinkstaubfarben auf Epoxidharz-Basis mit geeigneter Pigment-Volumen-Konzentration (PVK), bei der sich die Zinkteilchen berühren, schützen gut vor Korrosion. ⓘ
Bei einer Beschichtung mit einem edleren Metall (zum Beispiel Zinn bei Weißblech) tritt der umgekehrte Fall ein. Das Eisen rostet, möglicherweise verdeckt von der Schutzschicht (siehe Bild der Getränkedose). Die Anwesenheit eines edleren Metalls fördert sogar die Oxidation. Das Lokalelement aus Eisen und dem edleren Metall verhindert die schützende negative Aufladung des Eisens (siehe oben). ⓘ
Beispiel 2: Eisenrohre werden elektrisch mit einer sogenannten Opferanode aus einem unedleren Metall verbunden. Wie im ersten Beispiel wird Eisen auf Kosten der Opferanode geschützt, sofern beide über einen Elektrolyten, zum Beispiel feuchtes Erdreich, im Kontakt stehen. ⓘ
Beispiel 3: Statt einer Opferanode schützt auch eine elektrisch leitende Elektrode (zum Beispiel Graphit), wenn sie über eine externe Gleichspannungsquelle auf einem positiven Potenzial relativ zum Eisen gehalten wird. Dies nennt man dann kathodischen Korrosionsschutz, der bei Pipelines und im Brückenbau eingesetzt wird. ⓘ



