Bilirubin

| |

| |
| Bezeichnungen | |
|---|---|
| IUPAC-Bezeichnung
3,3′-(2,17-Diethenyl-3,7,13,18-tetramethyl-1,19-dioxo-10,19,21,22,23,24-hexahydro-1H-biline-8,12-diyl)dipropanoic acid
| |
| Bevorzugter IUPAC-Name
3,3′-([12(2)Z,6(72)Z]-13,74-Diethenyl-14,33,54,73-tetramethyl-15,75-dioxo-11,15,71,75-tetrahydro-31H,51H-1,7(2),3,5(2,5)-tetrapyrrolaheptaphane-12(2),6(72)-diene-34,53-diyl)dipropanoic acid | |
| Andere Bezeichnungen
Bilirubin IXα
| |
| Bezeichner | |
3D-Modell (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
IUPHAR/BPS
|
|
PubChem CID
|
|
| UNII | |
Ausklappen
InChI | |
Ausklappen
SMILES | |
| Eigenschaften | |
Chemische Formel
|
C33H36N4O6 |
| Molekulare Masse | 584,673 g-mol-1 |
| Dichte | 1,31 g-cm-3 |
| Schmelzpunkt | 235°C |
Wenn nicht anders angegeben, beziehen sich die Daten auf Materialien in ihrem Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
Bilirubin (BR) (lateinisch für "rote Galle") ist eine rot-orangefarbene Verbindung, die bei Wirbeltieren im normalen Katabolismusweg des Häm-Abbaus entsteht. Dieser Abbau ist ein notwendiger Prozess bei der Beseitigung von Abfallprodukten, die bei der Zerstörung gealterter oder abnormaler roter Blutkörperchen entstehen, durch den Körper. Im ersten Schritt der Bilirubin-Synthese wird das Häm-Molekül aus dem Hämoglobin-Molekül herausgelöst. Anschließend durchläuft das Häm verschiedene Prozesse des Porphyrinabbaus, die je nach Körperregion, in der der Abbau stattfindet, unterschiedlich sind. So unterscheiden sich beispielsweise die im Urin ausgeschiedenen Moleküle von denen im Stuhl. Die Herstellung von Biliverdin aus Häm ist der erste große Schritt im Katabolismusweg, nach dem das Enzym Biliverdin-Reduktase den zweiten Schritt durchführt, indem es Bilirubin aus Biliverdin herstellt. ⓘ
Letztendlich wird Bilirubin im Körper abgebaut, und seine Metaboliten werden über die Galle und den Urin ausgeschieden; erhöhte Werte können auf bestimmte Krankheiten hinweisen. Es ist verantwortlich für die gelbe Farbe von heilenden Blutergüssen und die gelbe Verfärbung bei Gelbsucht. Seine Abbauprodukte, wie z. B. Stercobilin, verursachen die braune Farbe des Stuhls. Ein anderes Abbauprodukt, Urobilin, ist der Hauptbestandteil der strohgelben Farbe des Urins. ⓘ
Obwohl Bilirubin normalerweise eher in Tieren als in Pflanzen vorkommt, ist zumindest eine Pflanzenart, Strelitzia nicolai, dafür bekannt, dass sie das Pigment enthält. ⓘ
| Strukturformel ⓘ | |||||||
|---|---|---|---|---|---|---|---|
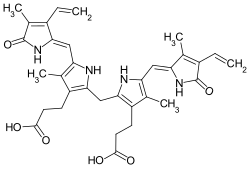
| |||||||
| Allgemeines | |||||||
| Name | Bilirubin | ||||||
| Andere Namen |
| ||||||
| Summenformel | C33H36N4O6 | ||||||
| Kurzbeschreibung |
roter Feststoff | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 584,66 g·mol−1 | ||||||
| Aggregatzustand |
fest | ||||||
| Löslichkeit |
| ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Das Bilirubin (lateinisch bilis „Galle“ und ruber „rot“) ist ein gelbes Abbauprodukt des Häm-Anteils des roten Blutfarbstoffes Hämoglobin und damit ein Gallenfarbstoff. Das Pigment kommt in der Natur nicht nur in Tieren, sondern auch in Pflanzen vor; 2009 wurde es erstmals im Samen von Baum-Strelitzien nachgewiesen. Bilirubin wurde erstmals 1942 durch Hans Fischer erfolgreich synthetisiert. ⓘ
Isomere
Die quantitativ vorherrschende Form entsteht durch Aufspaltung des Häm-Rings in der IX-α Position und wird deshalb als (Z,Z)-Bilirubin IX-α bezeichnet. Es liegen jedoch auch andere Isomere vor, die durch Aufspaltung des Häm-Rings in der β-, γ- oder δ-Position generiert werden. Bilirubin IX-α ist bei physiologischem pH-Wert nahezu wasserunlöslich, da seine Carboxy- und Aminogruppen durch intramolekulare Wasserstoffbrücken fixiert sind. Für den Transport in der Zirkulation ist es deshalb nicht-kovalent an Albumin gebunden. Durch die intramolekularen Wasserstoffbrücken entsteht zudem die wannenförmige räumliche Struktur des Bilrubins. Die β-, γ- oder δ-Isomere können keine Wasserstoffbrücken ausbilden. Sie sind daher besser wasserlöslich und können renal ausgeschieden werden. Weitere Isomere, z. B. Bilirubin III-α und Bilirubin XIII-α, kommen zwar im Plasma nicht vor, können jedoch in Standardpräparationen in größeren Mengen vorhanden sein. ⓘ
Die Fototherapie, bei der mit sichtbarem Licht im Wellenlängenbereich 420–470 nm bestrahlt wird, ist heute die Standardtherapie für mittelschwere Hyperbilirubinämien bei Neugeborenen. Neben Fotooxidationsprodukten, d. h. Bruchstücken des Moleküls, entstehen dabei durch eine cis-trans-Isomerisierung (Z→E) zwei neue Fraktionen: das Stereoisomer (4Z,15E)-Bilirubin IX-α und in geringerem Umfang das (4E,15Z)-Cyclobilirubin IX-α. Durch das Umklappen einer Doppelbindung wird einer der äußeren Ringe des Moleküls so gedreht, dass die Ausbildung von Wasserstoffbrücken nicht mehr möglich ist. Die Moleküle sind deshalb polarer und besser wasserlöslich und werden in der Hauptsache ohne Konjugation über Leber und Galle ausgeschieden. ⓘ
Bilirubin besteht aus einem offenkettigen Tetrapyrrol. Es wird durch oxidative Spaltung eines Porphyrins im Häm gebildet, wodurch Biliverdin entsteht. Biliverdin wird zu Bilirubin reduziert. Nach Konjugation mit Glucuronsäure wird Bilirubin ausgeschieden. ⓘ
Bilirubin ähnelt strukturell dem Pigment Phycobilin, das von bestimmten Algen zum Einfangen von Lichtenergie verwendet wird, und dem Pigment Phytochrom, das von Pflanzen zur Wahrnehmung von Licht verwendet wird. Alle diese Pigmente enthalten eine offene Kette aus vier Pyrrolringen. ⓘ
Wie bei diesen anderen Pigmenten isomerisieren einige der Doppelbindungen in Bilirubin, wenn es dem Licht ausgesetzt wird. Diese Isomerisierung ist für die Phototherapie von Neugeborenen mit Gelbsucht von Bedeutung: Die E,Z-Isomere des Bilirubins, die sich bei Lichteinwirkung bilden, sind besser löslich als das unbeleuchtete Z,Z-Isomer, da die Möglichkeit einer intramolekularen Wasserstoffbrückenbindung wegfällt. Die erhöhte Löslichkeit ermöglicht die Ausscheidung von nicht konjugiertem Bilirubin über die Galle. ⓘ
In einigen Lehrbüchern und Forschungsartikeln wird das falsche geometrische Isomer von Bilirubin angegeben. Das natürlich vorkommende Isomer ist das Z,Z-Isomer. ⓘ
Funktion
Bilirubin entsteht durch die Aktivität der Biliverdin-Reduktase an Biliverdin, einem grünen tetrapyrrolischen Gallenfarbstoff, der ebenfalls ein Produkt des Häm-Katabolismus ist. Wenn Bilirubin oxidiert wird, verwandelt es sich wieder in Biliverdin. Dieser Zyklus und die nachgewiesene starke antioxidative Wirkung von Bilirubin haben zu der Hypothese geführt, dass die wichtigste physiologische Funktion von Bilirubin die eines zellulären Antioxidans ist. In Übereinstimmung damit deuten Tierstudien darauf hin, dass die Eliminierung von Bilirubin zu endogenem oxidativem Stress führt. Die antioxidative Wirkung von Bilirubin könnte im Gehirn besonders wichtig sein, wo es Exzitotoxizität und den Tod von Neuronen verhindert, indem es Superoxid während der N-Methyl-D-Asparaginsäure-Neurotransmission abfängt. ⓘ
Stoffwechsel

Gesamtbilirubin = direktes Bilirubin + indirektes Bilirubin ⓘ
Eine Erhöhung sowohl der Alanin-Aminotransferase (ALT) als auch des Bilirubins deutet eher auf eine schwerwiegende Leberschädigung hin als eine Erhöhung der ALT allein, wie es im Hy'schen Gesetz postuliert wird, das den Zusammenhang zwischen den Labortestergebnissen und arzneimittelinduzierten Leberschäden verdeutlicht ⓘ
Indirekt (unkonjugiert)
Die Messung von unkonjugiertem Bilirubin (UCB) wird durch die Messung von indirektem Bilirubin unterschätzt, da unkonjugiertes Bilirubin (ohne/kaum Glucuronidierung) mit Diazosulfanilsäure zu Azobilirubin reagiert, das als direktes Bilirubin gemessen wird. ⓘ
Direkt
Direktes Bilirubin = Konjugiertes Bilirubin + Delta-Bilirubin ⓘ
Konjugiertes
In der Leber wird Bilirubin durch das Enzym Glucuronyltransferase mit Glucuronsäure konjugiert, zunächst zu Bilirubinglucuronid und dann zu Bilirubindiglucuronid, wodurch es wasserlöslich wird: Die konjugierte Version ist die Hauptform des Bilirubins in der "direkten" Bilirubinfraktion. Ein Großteil davon gelangt in die Galle und damit in den Dünndarm. Obwohl der größte Teil der Gallensäure im terminalen Ileum resorbiert wird, um am enterohepatischen Kreislauf teilzunehmen, wird konjugiertes Bilirubin nicht resorbiert und gelangt stattdessen in den Dickdarm. ⓘ
Dort dekonjugieren und metabolisieren Kolonbakterien das Bilirubin in farbloses Urobilinogen, das zu Urobilin und Stercobilin oxidiert werden kann. Urobilin wird über die Nieren ausgeschieden und verleiht dem Urin seine gelbe Farbe, während Stercobilin mit dem Kot ausgeschieden wird und dem Stuhl seine charakteristische braune Farbe verleiht. Eine Spur (~1%) des Urobilinogens wird in den enterohepatischen Kreislauf resorbiert und in der Galle wieder ausgeschieden. ⓘ
Die Halbwertszeit von konjugiertem Bilirubin ist kürzer als die von Delta-Bilirubin. ⓘ
Delta-Bilirubin
Obwohl die Begriffe direktes und indirektes Bilirubin gleichbedeutend mit konjugiertem und unkonjugiertem Bilirubin verwendet werden, ist dies quantitativ nicht korrekt, denn die direkte Fraktion umfasst sowohl konjugiertes Bilirubin als auch δ-Bilirubin. ⓘ
Delta-Bilirubin ist Albumin-gebundenes konjugiertes Bilirubin. Mit anderen Worten, Delta-Bilirubin ist die Art von Bilirubin, die kovalent an Albumin gebunden ist und im Serum erscheint, wenn die hepatische Ausscheidung von konjugiertem Bilirubin bei Patienten mit hepatobiliären Erkrankungen beeinträchtigt ist. Außerdem neigt das direkte Bilirubin dazu, den Gehalt an konjugiertem Bilirubin zu überschätzen, da unkonjugiertes Bilirubin mit Diazosulfanilsäure reagiert hat, was zu erhöhten Azobilirubinwerten (und erhöhtem direkten Bilirubin) führt. ⓘ
δ-Bilirubin = Gesamtbilirubin - (unkonjugiertes Bilirubin + konjugiertes Bilirubin) ⓘ
Halbwertszeit
Die Halbwertszeit von Delta-Bilirubin entspricht der von Albumin, da ersteres an letzteres gebunden ist und 2-3 Wochen ergibt. ⓘ
Ein ungebundenes Bilirubin hat eine Halbwertszeit von 2 bis 4 Stunden. ⓘ
Urin
Unter normalen Umständen wird, wenn überhaupt, nur eine sehr geringe Menge an Urobilinogen mit dem Urin ausgeschieden. Wenn die Leberfunktion beeinträchtigt oder der Abfluss der Galle blockiert ist, tritt ein Teil des konjugierten Bilirubins aus den Hepatozyten aus und gelangt in den Urin, der dadurch dunkel bernsteinfarben wird. Bei Erkrankungen, die mit einer hämolytischen Anämie einhergehen, werden jedoch vermehrt rote Blutkörperchen abgebaut, was zu einem Anstieg der Menge an unkonjugiertem Bilirubin im Blut führt. Da das unkonjugierte Bilirubin nicht wasserlöslich ist, ist kein Anstieg des Bilirubins im Urin zu beobachten. Da es kein Problem mit der Leber oder dem Gallensystem gibt, durchläuft dieses überschüssige unkonjugierte Bilirubin alle normalen Verarbeitungsmechanismen (z. B. Konjugation, Ausscheidung in der Galle, Metabolisierung zu Urobilinogen, Rückresorption) und zeigt sich als Anstieg des Urobilinogens im Urin. Dieser Unterschied zwischen erhöhtem Bilirubin im Urin und erhöhtem Urobilinogen im Urin hilft bei der Unterscheidung zwischen verschiedenen Störungen in diesen Systemen. ⓘ
Toxizität
Der Wert des ungebundenen Bilirubins (Bf) kann zur Vorhersage des Risikos einer neurologischen Entwicklungsstörung bei Säuglingen herangezogen werden. Eine unkonjugierte Hyperbilirubinämie bei einem Neugeborenen kann zu einer Anhäufung von Bilirubin in bestimmten Hirnregionen (insbesondere in den Basalkernen) führen, was irreversible Schäden in diesen Bereichen zur Folge hat, die sich in verschiedenen neurologischen Defiziten, Krampfanfällen, abnormen Reflexen und Augenbewegungen äußern. Diese Art der neurologischen Schädigung wird als Kernikterus bezeichnet. Das Spektrum der klinischen Auswirkungen wird als Bilirubin-Enzephalopathie bezeichnet. Die Neurotoxizität der neonatalen Hyperbilirubinämie tritt auf, weil die Blut-Hirn-Schranke noch nicht vollständig ausgebildet ist und Bilirubin ungehindert in das Interstitium des Gehirns eindringen kann, während höher entwickelte Individuen mit erhöhtem Bilirubin im Blut geschützt sind. Abgesehen von bestimmten chronischen Erkrankungen, die zu einer Hyperbilirubinämie führen können, sind Neugeborene im Allgemeinen einem erhöhten Risiko ausgesetzt, da ihnen die Darmbakterien fehlen, die den Abbau und die Ausscheidung von konjugiertem Bilirubin im Stuhl erleichtern (dies ist weitgehend der Grund, warum der Stuhl eines Neugeborenen blasser ist als der eines Erwachsenen). Stattdessen wird das konjugierte Bilirubin durch das Enzym β-Glucuronidase wieder in die unkonjugierte Form umgewandelt (im Darm befindet sich dieses Enzym im Bürstensaum der Darmschleimhautzellen) und ein großer Teil wird über den enterohepatischen Kreislauf resorbiert. Darüber hinaus weisen neuere Studien darauf hin, dass hohe Gesamtbilirubinwerte unabhängig von Geschlecht und Alter eine Ursache für Gallensteine sind. ⓘ
Gesundheitliche Vorteile
Wenn keine Lebererkrankung vorliegt, sind hohe Gesamtbilirubinwerte mit verschiedenen gesundheitlichen Vorteilen verbunden. Studien haben auch gezeigt, dass der Serumbilirubinspiegel (SBR) in umgekehrtem Verhältnis zum Risiko für bestimmte Herzerkrankungen steht. Während die schlechte Löslichkeit und die potenzielle Toxizität von Bilirubin seine potenziellen medizinischen Anwendungen einschränken, wird derzeit erforscht, ob in Seidenfibrin-Nanopartikeln eingekapseltes Bilirubin die Symptome von Erkrankungen wie akuter Pankreatitis lindern kann. Darüber hinaus wurden in jüngster Zeit Entdeckungen gemacht, die Bilirubin und sein ε-Polylysin-Bilirubin-Konjugat (PLL-BR) mit einer effizienteren Insulinmedikation in Verbindung bringen. Es scheint, dass Bilirubin während der Inseltransplantation schützende Eigenschaften aufweist, wenn die Medikamente über den Blutkreislauf zugeführt werden. ⓘ
Blutuntersuchungen
Bilirubin wird durch Licht abgebaut. Blutentnahmeröhrchen, die Blut oder (insbesondere) Serum enthalten, das für Bilirubin-Tests verwendet werden soll, sollten vor Licht geschützt werden. Bei Erwachsenen wird das Blut normalerweise mit einer Nadel aus einer Armvene entnommen. Bei Neugeborenen wird das Blut häufig mit einem Fersenstich entnommen, einer Technik, bei der mit einer kleinen, scharfen Klinge die Haut an der Ferse des Säuglings aufgeschnitten und einige Tropfen Blut in ein kleines Röhrchen aufgefangen werden. In einigen Gesundheitseinrichtungen steht eine nicht-invasive Technologie zur Verfügung, bei der Bilirubin mit einem auf der Haut platzierten Instrument gemessen wird (transkutanes Bilirubin-Messgerät). ⓘ
Bilirubin (im Blut) kommt in zwei Formen vor:
| Abb. | Bezeichnung(en) | Wasserlöslich | Reaktion ⓘ |
| "BC" | "Konjugiertes Bilirubin" | Ja (gebunden an Glucuronsäure) | Reagiert schnell, wenn Farbstoffe (Diazoreagenz) zur Blutprobe hinzugefügt werden, um Azobilirubin zu erzeugen "Direktes Bilirubin" |
| "BU" | "Unkonjugiertes Bilirubin" | Keine | Reagiert langsamer, ergibt immer noch Azobilirubin, Ethanol lässt alles Bilirubin sofort reagieren, dann: indirektes Bilirubin = Gesamtbilirubin - direktes Bilirubin |
Hinweis: Konjugiertes Bilirubin wird oft fälschlicherweise als "direktes Bilirubin" und unkonjugiertes Bilirubin fälschlicherweise als "indirektes Bilirubin" bezeichnet. Direkte und indirekte Bezeichnungen beziehen sich ausschließlich auf die Art und Weise, wie die Verbindungen in Lösung gemessen oder nachgewiesen werden. Direktes Bilirubin ist jede Form von Bilirubin, die wasserlöslich ist und in Lösung mit den Testreagenzien reagieren kann. Direktes Bilirubin besteht oft größtenteils aus konjugiertem Bilirubin, aber ein Teil des unkonjugierten Bilirubins (bis zu 25 %) kann immer noch Teil der "direkten" Bilirubinfraktion sein. Ebenso ist nicht alles konjugierte Bilirubin in Lösung für eine Reaktion oder einen Nachweis leicht verfügbar (z. B. wenn es mit sich selbst Wasserstoffbrückenbindungen eingeht) und würde daher nicht in die direkte Bilirubinfraktion einbezogen werden. ⓘ
Das Gesamtbilirubin (TBIL) misst sowohl BU als auch BC. Gesamtbilirubin-Tests arbeiten mit Tensiden und Beschleunigern (wie Koffein), um alle verschiedenen Bilirubinformen in Lösung zu bringen, wo sie mit den Testreagenzien reagieren können. Der Gesamtbilirubinspiegel und der direkte Bilirubinspiegel können im Blut gemessen werden, aber das indirekte Bilirubin wird aus dem Gesamtbilirubin und dem direkten Bilirubin berechnet. ⓘ
Indirektes Bilirubin ist fettlöslich und direktes Bilirubin ist wasserlöslich. ⓘ
Messmethoden
Ursprünglich wurde die Van-den-Bergh-Reaktion für eine qualitative Schätzung des Bilirubins verwendet. ⓘ
Dieser Test wird in den meisten medizinischen Labors routinemäßig durchgeführt und kann mit einer Vielzahl von Methoden gemessen werden. ⓘ
Das Gesamtbilirubin wird heute häufig mit der 2,5-Dichlorphenyldiazonium-Methode (DPD) gemessen, und das direkte Bilirubin wird häufig mit der Methode von Jendrassik und Grof bestimmt. ⓘ
Blutspiegel
Der im Körper festgestellte Bilirubinspiegel spiegelt das Gleichgewicht zwischen Produktion und Ausscheidung wider. Es wird empfohlen, bei der Interpretation von Bluttestergebnissen immer den Referenzbereich des Labors zu verwenden, das den Test durchgeführt hat. Die SI-Einheiten sind μmol/L. Typische Bereiche für Erwachsene sind:
- 0-0,3 mg/dl - direkter (konjugierter) Bilirubinspiegel
- 0,1-1,2 mg/dl - Gesamtbilirubinspiegel im Serum ⓘ
| μmol/l = Mikromol/Liter | mg/dl = Milligramm/Deziliter ⓘ | |
| Gesamtbilirubin | <21 | <1.23 |
| direktes Bilirubin | 1.0–5.1 | 0–0.3, 0.1–0.3, 0.1–0.4 |
Hyperbilirubinämie
Hyperbilirubinämie ist ein überdurchschnittlich hoher Bilirubinspiegel im Blut. Bei Erwachsenen ist dies jeder Wert über 170 μmol/l und bei Neugeborenen 340 μmol/l und kritische 425 μmol/l. ⓘ
Leichte Erhöhungen des Bilirubinspiegels können verursacht werden durch:
- Hämolyse oder vermehrter Abbau von roten Blutkörperchen
- Gilbert-Syndrom - eine genetisch bedingte Störung des Bilirubinstoffwechsels, die zu einer leichten Gelbsucht führen kann und bei etwa 5 % der Bevölkerung auftritt
- Rotor-Syndrom: Gelbsucht ohne Juckreiz, mit Anstieg des Bilirubins im Serum des Patienten, hauptsächlich vom konjugierten Typ ⓘ
Ein mäßiger Anstieg des Bilirubins kann verursacht werden durch:
- Arzneimittel (insbesondere Antipsychotika, einige Sexualhormone und eine Vielzahl anderer Arzneimittel)
- Sulfonamide sind bei Säuglingen unter 2 Monaten kontraindiziert (Ausnahme bei Verwendung mit Pyrimethamin zur Behandlung von Toxoplasmose), da sie das unkonjugierte Bilirubin erhöhen und zu Kernikterus führen.
- Medikamente wie Proteaseinhibitoren wie Indinavir können ebenfalls Störungen des Bilirubinstoffwechsels verursachen, da sie das UGT1A1-Enzym kompetitiv hemmen.
- Hepatitis (die Werte können mäßig oder hoch sein)
- Chemotherapie
- Gallengangstriktur (gutartig oder bösartig) ⓘ
Sehr hohe Bilirubinwerte können verursacht werden durch:
- Neugeborenen-Hyperbilirubinämie, bei der die Leber des Neugeborenen nicht in der Lage ist, das Bilirubin richtig zu verarbeiten, was zu Gelbsucht führt
- Ungewöhnlich große Gallengangsobstruktion, z. B. Stein im Hauptgallengang, Tumor, der den Hauptgallengang blockiert usw.
- Schweres Leberversagen mit Zirrhose (z. B. primär biliäre Zirrhose)
- Crigler-Najjar-Syndrom
- Dubin-Johnson-Syndrom
- Choledocholithiasis (chronisch oder akut). ⓘ
Eine Zirrhose kann je nach den genauen Merkmalen der Zirrhose normale, mäßig hohe oder hohe Bilirubinwerte verursachen. ⓘ
Zur weiteren Abklärung der Ursachen von Gelbsucht oder erhöhtem Bilirubin ist es in der Regel einfacher, andere Leberfunktionstests (insbesondere die Enzyme Alanin-Transaminase, Aspartat-Transaminase, Gamma-Glutamyl-Transpeptidase, alkalische Phosphatase), Blutbilduntersuchungen (Hämolyse usw.) oder Hinweise auf infektiöse Hepatitis (z. B. Hepatitis A, B, C, Delta, E usw.) zu untersuchen. ⓘ
Gelbsucht
Hämoglobin sorgt dafür, dass der Sauerstoff, den Ihr Körper erhält, über die Blutgefäße zu allen Körpergeweben transportiert wird. Im Laufe der Zeit, wenn die roten Blutkörperchen erneuert werden müssen, wird das Hämoglobin in der Milz in zwei Teile zerlegt: die Häm-Gruppe, die aus Eisen und Galle besteht, und die Proteinfraktion. Während Eiweiß und Eisen zur Erneuerung der roten Blutkörperchen verwendet werden, lagern sich die Pigmente, die die rote Farbe des Blutes ausmachen, in der Galle ab und bilden Bilirubin. Gelbsucht führt zu erhöhten Bilirubinwerten, die wiederum elastinreiches Gewebe negativ beeinflussen. Gelbsucht kann sich in der Sklera der Augen bei Werten von etwa 2 bis 3 mg/dl (34 bis 51 μmol/l) und in der Haut bei höheren Werten bemerkbar machen. ⓘ
Je nachdem, ob das Bilirubin frei oder an Glucuronsäure konjugiert ist, wird die Gelbsucht in konjugierte Gelbsucht oder nicht konjugierte Gelbsucht unterteilt. ⓘ
Urinuntersuchungen
Auch das Bilirubin im Urin kann klinisch bedeutsam sein. Bilirubin ist bei gesunden Menschen normalerweise nicht im Urin nachweisbar. Wenn der Blutspiegel von konjugiertem Bilirubin erhöht ist, z. B. aufgrund einer Lebererkrankung, wird überschüssiges konjugiertes Bilirubin mit dem Urin ausgeschieden, was auf einen pathologischen Prozess hinweist. Unkonjugiertes Bilirubin ist nicht wasserlöslich und wird daher nicht über den Urin ausgeschieden. Die Untersuchung des Urins sowohl auf Bilirubin als auch auf Urobilinogen kann helfen, eine obstruktive Lebererkrankung von anderen Ursachen der Gelbsucht zu unterscheiden. ⓘ
Geschichte
In der Antike diskutierte Hippokrates die Gallenpigmente in zwei der vier Körpersäfte im Zusammenhang mit einer Beziehung zwischen gelber und schwarzer Galle. Hippokrates besuchte Demokrit in Abdera, der als Experte für Melagkholy, die "schwarze Galle", angesehen wurde. ⓘ
Einschlägige Unterlagen tauchten 1827 auf, als M. Louis Jacques Thénard die Gallenwege eines verendeten Elefanten in einem Pariser Zoo untersuchte. Er stellte fest, dass die erweiterten Gallengänge mit gelbem Magma gefüllt waren, das er isolierte und das sich als unlöslich in Wasser erwies. Bei der Behandlung des gelben Pigments mit Salzsäure entstand eine starke grüne Farbe. Thenard vermutete, dass das grüne Pigment durch Verunreinigungen aus dem Gallenschleim verursacht wurde. ⓘ
Leopold Gmelin experimentierte 1826 mit Salpetersäure, um das Redoxverhalten bei der Umwandlung von Bilirubin in Biliverdin festzustellen, obwohl die Nomenklatur zu dieser Zeit noch nicht existierte. Der Begriff Biliverdin wurde 1840 von Jöns Jacob Berzelius geprägt, obwohl er "Bilifulvin" (gelb/rot) gegenüber "Bilirubin" (rot) bevorzugte. Der Begriff "Bilirubin" setzte sich vermutlich aufgrund der Arbeiten von Staedeler durch, der 1864 Bilirubin aus Rindergallensteinen kristallisierte. ⓘ
Rudolf Virchow erkannte 1847, dass Hämatoidin mit Bilirubin identisch ist. Es wird nicht immer von Hämatoidin unterschieden, das in einem modernen Wörterbuch als gleichbedeutend mit Bilirubin definiert wird, in einem anderen jedoch als "scheinbar chemisch identisch mit Bilirubin, aber mit einem anderen Ursprungsort, der lokal im Gewebe aus Hämoglobin gebildet wird, insbesondere unter Bedingungen einer reduzierten Sauerstoffspannung". Die synonyme Identität von Bilirubin und Hämatoidin wurde 1923 von Fischer und Steinmetz mittels analytischer Kristallographie bestätigt. ⓘ
In den 1930er Jahren wurden von Hans Fischer, Plieninger und anderen bedeutende Fortschritte bei der Isolierung und Synthese von Bilirubin beschrieben, und im selben Jahrzehnt wurden auch bahnbrechende Arbeiten zur endogenen Bildung von Bilirubin aus Häm durchgeführt. Das Suffix IXα basiert teilweise auf einem von Fischer entwickelten System, das bedeutet, dass die Ausgangsverbindung des Bilins das an der Alpha-Methin-Brücke gespaltene Protoporphyrin IX war (siehe Nomenklatur von Protoporphyrin IX). ⓘ
Die Ursprünge der physiologischen Aktivität von Bilirubin wurden 1891 von Ernst Stadelmann beschrieben, der die Biotransformation von infundiertem Hämoglobin in Bilirubin beobachtet haben könnte, möglicherweise inspiriert durch Ivan Tarkhanovs Arbeiten von 1874. Georg Barkan schlug 1932 vor, dass die Quelle des endogenen Bilirubins das Hämoglobin sein könnte. Plieninger und Fischer wiesen 1942 einen enzymatischen oxidativen Verlust der Alpha-Methin-Brücke von Häm nach, der zu einer Bis-Lactam-Struktur führte. Es ist allgemein anerkannt, dass Irving London 1950 als Erster die endogene Bildung von Bilirubin aus Hämoglobin nachwies, und Sjostrand zeigte zwischen 1949 und 1952, dass beim Hämoglobinabbau Kohlenmonoxid entsteht. Die Biotransformation von 14C-markiertem Protoporphyrin zu Bilirubin wurde 1966 von Cecil Watson nachgewiesen. Rudi Schmid und Tenhunen entdeckten 1968 die Häm-Oxygenase, das verantwortliche Enzym. Zuvor hatte Nakajima 1963 eine lösliche "Häm-Alpha-Methnyl-Oxygeanse" beschrieben, die sich später als nicht-enzymatischer Weg herausstellte, wie die Bildung eines 1,2-Dioxetan-Zwischenprodukts an der Methinbrücke, das zur Freisetzung von Kohlenmonoxid und zur Bildung von Biliverdin führt. ⓘ
Bemerkenswerte Persönlichkeiten
- Claudio Tiribelli, italienischer Hepatologe, Studien über Bilirubin ⓘ
