Herzfrequenzvariabilität
Als Herzfrequenzvariabilität (englisch heart rate variability, HRV) wird die natürliche Variation der Zeit zwischen zwei aufeinanderfolgenden Herzschlägen bezeichnet. Bei gesunden erwachsenen Menschen beträgt diese Variation in Ruhe ca. eine Zehntelsekunde. Die Herzfrequenzvariabilität ist ein Indikator für die Fähigkeit eines Organismus (Mensch, Säugetier), die Herzfrequenz den körperlichen und mentalen Anforderungen anzupassen. Maße für die Herzfrequenzvariabilität lassen sich statistisch im Zeitbereich als Streumaße (Mittelwert, Standardabweichung, Varianz) oder spektral im Frequenzbereich (low frequency, high frequency) ableiten; eine dritte Möglichkeit bieten nicht-lineare Methoden (z. B. Poincaré-Abbildung, Fluktuationsanalyse). ⓘ
Über autonome physiologische Regulationswege passt ein gesunder Organismus die Herzschlagrate beständig momentanen Erfordernissen an. Körperliche Beanspruchung oder psychische Belastung hat deswegen in der Regel eine Erhöhung der Herzfrequenz zur Folge, die bei Entlastung und Entspannung normalerweise wieder zurückgeht. Dabei zeigt sich eine höhere Anpassungsfähigkeit an Belastungen in einer größeren Variabilität der Herzfrequenz. Unter chronischer Stressbelastung ist beides dagegen wegen der beständig hohen Anspannung, die dafür typisch ist, mehr oder weniger eingeschränkt und infolgedessen reduziert. ⓘ

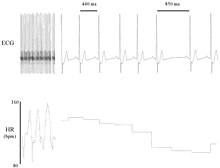
Andere verwendete Begriffe sind: "Zykluslängenvariabilität", "R-R-Variabilität" (wobei R ein Punkt ist, der dem Scheitelpunkt des QRS-Komplexes der EKG-Welle entspricht, und RR das Intervall zwischen aufeinanderfolgenden Rs ist) und "Herzperiodenvariabilität". ⓘ
Zu den Methoden zur Erkennung von Schlägen gehören: EKG, Blutdruck, Ballistokardiogramme, und das von einem Photoplethysmographen (PPG) abgeleitete Pulswellensignal. Das EKG gilt als der Goldstandard für die Messung der HRV, da es die elektrische Aktivität des Herzens direkt widerspiegelt. ⓘ
Klinische Bedeutung
Eine verringerte HRV ist nachweislich ein Prädiktor für die Mortalität nach einem Myokardinfarkt, obwohl andere Untersuchungen gezeigt haben, dass die für das Überleben nach einem akuten Myokardinfarkt relevanten Informationen in der HRV vollständig in der mittleren Herzfrequenz enthalten sind. Eine Reihe anderer Ergebnisse und Zustände können ebenfalls mit einer veränderten (in der Regel niedrigeren) HRV in Verbindung gebracht werden, darunter kongestive Herzinsuffizienz, diabetische Neuropathie, Depression nach einer Herztransplantation, Anfälligkeit für SIDS und schlechtes Überleben bei Frühgeborenen sowie der Schweregrad der Müdigkeit bei chronischem Müdigkeitssyndrom. ⓘ
Psychologische und soziale Aspekte
Im Bereich der Psychophysiologie besteht ein Interesse an der HRV. So steht die HRV beispielsweise im Zusammenhang mit emotionaler Erregung. Es wurde festgestellt, dass die Hochfrequenzaktivität (HF) unter akutem Zeitdruck, emotionaler Belastung und erhöhtem Angstzustand abnimmt, was vermutlich mit konzentrierter Aufmerksamkeit und motorischer Hemmung zusammenhängt. Es hat sich gezeigt, dass die HRV bei Personen, die angeben, sich mehr Sorgen zu machen, reduziert ist. Bei Personen mit posttraumatischer Belastungsstörung (PTSD) ist die HRV und ihre HF-Komponente (siehe unten) reduziert, während die niederfrequente Komponente (LF) erhöht ist. Darüber hinaus zeigten PTSD-Patienten keine LF- oder HF-Reaktivität bei der Erinnerung an ein traumatisches Ereignis. ⓘ
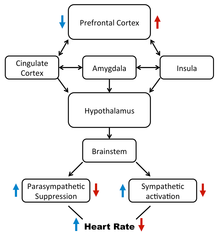
Die neuroviscerale Integration ist ein Modell der HRV, das das zentrale autonome Netzwerk als Entscheidungsträger der kognitiven, verhaltensbezogenen und physiologischen Regulierung in Bezug auf ein Kontinuum von Emotionen betrachtet. Das Modell der neurovisceralen Integration beschreibt, wie der präfrontale Kortex die Aktivität in limbischen Strukturen reguliert, die die Aktivität des parasympathischen Nervensystems (PSNS) unterdrücken und die Schaltkreise des sympathischen Nervensystems (SNS) aktivieren. Schwankungen im Output dieser beiden Zweige des autonomen Systems erzeugen die HRV, und die Aktivität im präfrontalen Kortex kann daher die HRV modulieren. ⓘ
Die HRV ist das Maß für die inkonsistenten Abstände zwischen den einzelnen Herzschlägen und wird als Index für verschiedene Aspekte der Psychologie verwendet. Es wird berichtet, dass die HRV ein Index für den Einfluss des parasympathischen und des sympathischen Nervensystems ist. Verschiedene Aspekte der Psychologie stellen das Gleichgewicht zwischen diesen beiden Einflüssen dar. Eine hohe HRV zeigt zum Beispiel eine gute Emotionsregulierung, Entscheidungsfindung und Aufmerksamkeit, während eine niedrige HRV das Gegenteil widerspiegelt. Das parasympathische Nervensystem wirkt auf die Senkung der Herzfrequenz hin, während das SNS auf die Erhöhung der Herzfrequenz hinwirkt, und dies ist wichtig, weil es sich auf die verschiedenen oben genannten psychologischen Zustände bezieht. Zum Beispiel kann jemand mit einer hohen HRV eine erhöhte parasympathische Aktivität widerspiegeln, während jemand mit einer niedrigen HRV eine erhöhte sympathische Aktivität widerspiegeln kann. ⓘ
Emotionen ergeben sich aus der Zeit und den Auswirkungen einer Situation auf eine Person. Die Fähigkeit, Emotionen zu regulieren, ist wesentlich für das soziale Umfeld und das Wohlbefinden. Die HRV hat einen Einblick in die physiologischen Komponenten gegeben, die mit der Emotionsregulierung verbunden sind. Es hat sich gezeigt, dass die HRV die Emotionsregulation auf zwei verschiedenen Ebenen widerspiegelt: in Ruhe und während der Ausführung einer Aufgabe. Forschungsergebnisse deuten darauf hin, dass eine Person mit einer höheren HRV im Ruhezustand angemessenere emotionale Reaktionen zeigen kann als eine Person mit einer niedrigen HRV im Ruhezustand. Empirische Untersuchungen haben ergeben, dass die HRV bei Personen mit einer höheren HRV im Ruhezustand eine bessere emotionale Regulierung widerspiegeln kann, insbesondere bei negativen Emotionen. Bei der Bewältigung einer Aufgabe verändert sich die HRV, insbesondere wenn Menschen ihre Emotionen regulieren müssen. Am wichtigsten ist, dass individuelle Unterschiede mit der Fähigkeit zur Emotionsregulierung zusammenhängen. Nicht nur die Emotionsregulation ist notwendig, sondern auch die Aufmerksamkeit. ⓘ
Frühere Forschungen haben ergeben, dass ein großer Teil der Aufmerksamkeitsregulierung auf die standardmäßigen inhibitorischen Eigenschaften des präfrontalen Kortex zurückzuführen ist. Top-down-Prozesse des präfrontalen Kortex sorgen für parasympathische Einflüsse, und wenn diese Einflüsse aus irgendeinem Grund aktiv sind, kann die Aufmerksamkeit leiden. Forscher haben zum Beispiel vorgeschlagen, dass die HRV die Aufmerksamkeit indizieren kann. So fand eine Forschergruppe heraus, dass Gruppen mit hoher Angst und niedriger HRV eine schlechte Aufmerksamkeit aufweisen. In Übereinstimmung mit dieser Forschung wurde auch festgestellt, dass eine erhöhte Aufmerksamkeit mit einer hohen HRV und einer erhöhten Aktivität des Vagusnervs verbunden ist. Die Aktivität des Vagusnervs spiegelt die physiologische Modulation des parasympathischen und sympathischen Nervensystems wider. Die Aktivität hinter dem präfrontalen Kortex und dem parasympathischen und sympathischen Nervensystem kann die Herzaktivität beeinflussen. Allerdings sind nicht alle Menschen in gleicher Weise betroffen. Eine systematische Überprüfung der HRV und der kognitiven Funktion ergab, dass die HRV im Ruhezustand individuelle Unterschiede in der Aufmerksamkeitsleistung vorhersagen kann. Selbst bei psychologischen Konzepten wie der Aufmerksamkeit kann die HRV individuelle Unterschiede anzeigen. Darüber hinaus ist die HRV in der Lage, die Rolle von Aufmerksamkeit und Leistung zu indizieren, was eine hohe HRV als Biomarker für erhöhte Aufmerksamkeit und Leistung unterstützt. Sowohl Emotionen als auch Aufmerksamkeit können Aufschluss darüber geben, wie die HRV als Index für die Entscheidungsfindung verwendet wird. ⓘ
In mehreren Studien wurde festgestellt, dass die Entscheidungsfähigkeit durch die HRV indiziert wird. Frühere Forschungen haben ergeben, dass sowohl Emotionen als auch Aufmerksamkeit mit der Entscheidungsfindung zusammenhängen; so ist beispielsweise eine schlechte Entscheidungsfindung mit der Unfähigkeit verbunden, Emotionen und Aufmerksamkeit zu regulieren oder zu kontrollieren und umgekehrt. Die Entscheidungsfindung wird durch eine niedrigere HRV negativ und durch ein höheres Niveau der HRV positiv beeinflusst. Vor allem aber wurde festgestellt, dass die HRV im Ruhezustand ein signifikanter Prädiktor für kognitive Funktionen wie die Entscheidungsfindung ist. Es hat sich gezeigt, dass die HRV in Verbindung mit einem psychologischen Zustand, wie z. B. Angst, zu schlechten Entscheidungen führt. So fand eine Forschergruppe heraus, dass eine niedrige HRV ein Indikator für eine höhere Unsicherheit ist, die zu einer schlechten Entscheidungsfähigkeit führt, insbesondere bei Personen mit einem höheren Angstniveau. Die HRV wurde auch zur Bewertung der Entscheidungsfähigkeit in einem Hochrisikospiel verwendet und erwies sich als Index für eine höhere Sympathikusaktivierung (niedrigere HRV) bei Entscheidungen, die mit Risiken verbunden sind. Die HRV kann psychologische Konzepte, wie die oben genannten, indizieren, um den Bedarf an den Situationen, die Menschen erleben, zu bewerten. ⓘ
Die polyvagale Theorie ist eine weitere Möglichkeit, die Bahnen im autonomen Nervensystem zu beschreiben, die die HRV vermitteln. Die polyvagale Theorie hebt drei ordinale Hauptprozesse hervor: die inaktive Reaktion auf eine Umweltbedrohung, die aktive Reaktion auf eine Umweltbedrohung und die Fluktuation zwischen der Verbindung und der Unterbrechung der Verbindung zu einer Umweltbedrohung. Wie andere Theorien zerlegt auch diese die Herzfrequenzvariabilität anhand von Frequenzbereichseigenschaften. Sie legt jedoch mehr Gewicht auf die respiratorische Sinusarrhythmie und ihre Übertragung durch einen hypothetischen neuronalen Pfad, der sich von anderen Komponenten der HRV unterscheidet. Es gibt anatomische und physiologische Beweise für eine polyvagale Steuerung des Herzens. ⓘ
Veränderung
Die Variation des Schlag-zu-Schlag-Intervalls ist ein physiologisches Phänomen. Der SA-Knoten erhält mehrere verschiedene Eingänge, und die momentane Herzfrequenz oder das RR-Intervall und seine Variation sind das Ergebnis dieser Eingänge. ⓘ
Die wichtigsten Inputs sind das sympathische und das parasympathische Nervensystem (PSNS) sowie humorale Faktoren. Die Atmung führt zu Wellen in der Herzfrequenz, die in erster Linie über das PSNS vermittelt werden, und es wird angenommen, dass die Verzögerung in der Barorezeptor-Rückkopplungsschleife zu 10-Sekunden-Wellen in der Herzfrequenz führen kann (in Verbindung mit den Mayer-Wellen des Blutdrucks), aber dies bleibt umstritten. ⓘ
Faktoren, die den Input beeinflussen, sind der Baroreflex, die Thermoregulation, Hormone, der Schlaf-Wach-Rhythmus, Mahlzeiten, körperliche Aktivität und Stress. ⓘ
Eine verringerte PSNS-Aktivität oder eine erhöhte SNS-Aktivität führt zu einer verringerten HRV. Insbesondere die hochfrequente (HF) Aktivität (0,15 bis 0,40 Hz) wurde mit der PSNS-Aktivität in Verbindung gebracht. Aktivität in diesem Bereich wird mit der respiratorischen Sinusarrhythmie (RSA) in Verbindung gebracht, einer vagal vermittelten Modulation der Herzfrequenz, bei der diese während der Inspiration ansteigt und während der Exspiration abfällt. Über die physiologischen Einflüsse der niederfrequenten (LF) Aktivität (0,04 bis 0,15 Hz) ist weniger bekannt. Früher ging man davon aus, dass sie die Aktivität des SNS widerspiegelt, heute ist man sich weitgehend einig, dass sie eine Mischung aus SNS und PSNS widerspiegelt. ⓘ
Phänomene
Es gibt zwei Hauptfluktuationen:
- Respiratorische Arrhythmie (oder respiratorische Sinusarrhythmie). Diese Herzfrequenzschwankung ist mit der Atmung verbunden und folgt der Atemfrequenz über eine Reihe von Frequenzen.
- Niederfrequente Oszillationen. Diese Herzfrequenzschwankungen stehen in Zusammenhang mit den Mayer-Wellen (Traube-Hering-Mayer-Wellen) des Blutdrucks und haben in der Regel eine Frequenz von 0,1 Hz oder einen Zeitraum von 10 Sekunden. ⓘ
Artefakt
Fehler bei der Lokalisierung des momentanen Herzschlags führen zu Fehlern bei der Berechnung der HRV. Die HRV ist sehr empfindlich gegenüber Artefakten, und selbst Fehler bei nur 2 % der Daten führen zu unerwünschten Verzerrungen bei den HRV-Berechnungen. Um genaue Ergebnisse zu gewährleisten, ist es daher entscheidend, Artefakte und RR-Fehler vor der Durchführung von HRV-Analysen angemessen zu behandeln. ⓘ
Ein robustes Management von Artefakten, einschließlich der Identifizierung, Interpolation und des Ausschlusses von RWellen, erfordert ein hohes Maß an Sorgfalt und Präzision. Dies kann bei großen Studien mit über lange Zeiträume aufgezeichneten Daten sehr zeitaufwändig sein. Softwarepakete können die Benutzer mit einer Vielzahl von robusten und getesteten Artefaktmanagement-Tools unterstützen. Diese Softwareprogramme bieten auch einige automatische Funktionen, aber es ist wichtig, dass ein Mensch jede automatische Artefaktverwaltung überprüft und entsprechend bearbeitet. ⓘ
Analyse
Die am weitesten verbreiteten Methoden lassen sich in Zeit- und Frequenzbereich gruppieren. Eine gemeinsame europäische und amerikanische Arbeitsgruppe beschrieb 1996 Standards für HRV-Messungen. Es wurden weitere Methoden vorgeschlagen, wie z. B. nichtlineare Methoden. ⓘ
Methoden im Zeitbereich
Sie beruhen auf den Schlag-zu-Schlag- oder NN-Intervallen, die analysiert werden, um Variablen wie die folgenden zu erhalten
- SDNN, die Standardabweichung der NN-Intervalle. Sie wird häufig über einen Zeitraum von 24 Stunden berechnet. SDANN, die Standardabweichung der durchschnittlichen NN-Intervalle, berechnet über kurze Zeiträume, normalerweise 5 Minuten. SDANN ist daher ein Maß für Veränderungen der Herzfrequenz aufgrund von Zyklen, die länger als 5 Minuten dauern. SDNN spiegelt alle zyklischen Komponenten wider, die für die Variabilität im Aufzeichnungszeitraum verantwortlich sind, und stellt somit die Gesamtvariabilität dar.
- RMSSD ("root mean square of successive differences"), die Quadratwurzel aus dem Mittelwert der Quadrate der aufeinanderfolgenden Differenzen zwischen benachbarten NNs.
- SDSD ("standard deviation of successive differences"), die Standardabweichung der aufeinanderfolgenden Differenzen zwischen benachbarten NNs.
- NN50, die Anzahl der Paare aufeinanderfolgender NN, die sich um mehr als 50 ms unterscheiden.
- pNN50, der Anteil von NN50 geteilt durch die Gesamtzahl der NN.
- NN20, die Anzahl der Paare von aufeinanderfolgenden NN, die sich um mehr als 20 ms unterscheiden.
- pNN20, der Anteil von NN20 geteilt durch die Gesamtzahl der NNs.
- EBC ("estimated breath cycle", geschätzter Atemzyklus), der Bereich (max-min) innerhalb eines beweglichen Fensters einer bestimmten Zeitdauer innerhalb des Untersuchungszeitraums. Die Fenster können sich selbst überlappen oder strikt getrennte (aufeinanderfolgende) Fenster sein. Die EBC wird häufig in Datenerfassungsszenarien bereitgestellt, bei denen die HRV-Rückmeldung in Echtzeit ein primäres Ziel ist. Es hat sich gezeigt, dass die aus dem PPG abgeleitete EBC über sequenzielle und überlappende 10- und 16-Sekunden-Fenster hoch mit der SDNN korreliert. ⓘ
Geometrische Methoden
Die Reihe der NN-Intervalle kann auch in ein geometrisches Muster umgewandelt werden, wie zum Beispiel: Geometrische Maße HRV Dreiecksindex: Integral der Dichteverteilung / Maximum der Dichteverteilung Maximum HRV-Dreiecksindex = Anzahl aller NN-Intervalle / maximale Anzahl. Abhängig von der Länge des Bin -> Angabe der Bin-Größe+ relativ unempfindlich gegenüber der analytischen Qualität der Serie von NN-Intervallen - Notwendigkeit einer angemessenen Anzahl von NN-Intervallen, um das geometrische Muster zu erzeugen (in der Praxis 20 min bis 24 h)- nicht geeignet, um kurzfristige Veränderungen der HRV zu bewerten
- die Stichprobendichteverteilung der NN-Intervalldauern;
- die Stichprobendichteverteilung der Differenzen zwischen benachbarten NN-Intervallen;
- ein Streudiagramm jedes NN- (oder RR-) Intervalls mit dem unmittelbar vorangegangenen NN- (oder RR-) Intervall - auch "Poincare-Plot" oder (offenbar irrtümlich) "Lorenz-Plot" genannt;
und so weiter. Es wird dann eine einfache Formel verwendet, die die Variabilität auf der Grundlage der geometrischen und/oder grafischen Eigenschaften des resultierenden Musters beurteilt. ⓘ
Methoden im Frequenzbereich
Bei Frequenzbereichsmethoden werden Frequenzbänder zugewiesen und dann die Anzahl der NN-Intervalle gezählt, die in jedes Band passen. Die Bänder sind in der Regel hochfrequent (HF) von 0,15 bis 0,4 Hz, niederfrequent (LF) von 0,04 bis 0,15 Hz und sehr niederfrequent (VLF) von 0,0033 bis 0,04 Hz. ⓘ
Für die Analyse stehen mehrere Methoden zur Verfügung. Die Leistungsspektraldichte (PSD) liefert mit Hilfe parametrischer oder nichtparametrischer Methoden grundlegende Informationen über die Leistungsverteilung über die Frequenzen. Eine der am häufigsten verwendeten PSD-Methoden ist die diskrete Fourier-Transformation. Die Methoden zur Berechnung der PSD lassen sich allgemein in nichtparametrische und parametrische Methoden einteilen. In den meisten Fällen liefern beide Methoden vergleichbare Ergebnisse. Die Vorteile der nichtparametrischen Methoden sind (1) die Einfachheit des verwendeten Algorithmus (in den meisten Fällen die schnelle Fourier-Transformation [FFT]) und (2) die hohe Verarbeitungsgeschwindigkeit. Die Vorteile parametrischer Methoden sind (1) glattere Spektralkomponenten, die unabhängig von vorgewählten Frequenzbändern unterschieden werden können, (2) eine einfache Nachbearbeitung des Spektrums mit einer automatischen Berechnung der nieder- und hochfrequenten Leistungskomponenten mit einer einfachen Identifizierung der zentralen Frequenz jeder Komponente und (3) eine genaue Schätzung der PSD selbst bei einer kleinen Anzahl von Abtastwerten, bei denen das Signal stationär bleiben soll. Der grundlegende Nachteil parametrischer Methoden besteht darin, dass die Eignung des gewählten Modells und seine Komplexität (d. h. die Ordnung des Modells) überprüft werden müssen. ⓘ
Neben den klassischen FFT-basierten Methoden zur Berechnung der Frequenzparameter ist das Lomb-Scargle-Periodogramm eine geeignetere Methode zur Schätzung der PSD. Die Analyse hat gezeigt, dass das LS-Periodogramm eine genauere Schätzung der PSD als FFT-Methoden für typische RR-Daten liefern kann. Da es sich bei den RR-Daten um ungleichmäßig abgetastete Daten handelt, besteht ein weiterer Vorteil der LS-Methode darin, dass sie im Gegensatz zu FFT-basierten Methoden verwendet werden kann, ohne dass die RR-Daten neu abgetastet und detrendiert werden müssen. ⓘ
Um Artefakte zu vermeiden, die bei der Berechnung der Leistung eines Signals entstehen, das eine einzelne hochintensive Spitze enthält (z. B. verursacht durch einen arrhythmischen Herzschlag), wurde alternativ das Konzept der "momentanen Amplitude" eingeführt, das auf der Hilbert-Transformation der RR-Daten basiert. ⓘ
Ein neu verwendeter HRV-Index, der von den Wavelet-Entropiemaßen abhängt, ist eine alternative Wahl. Die Wavelet-Entropiemaße werden nach einem in der Literatur beschriebenen dreistufigen Verfahren berechnet. Zunächst wird der Wavelet-Paket-Algorithmus unter Verwendung der Daubechies-4-Funktion (DB4) als Mutter-Wavelet mit einer Skala von 7 implementiert. Sobald die Wavelet-Koeffizienten erhalten sind, wird die Energie für jeden Koeffizienten wie in der Literatur beschrieben berechnet. Nach der Berechnung der normalisierten Werte der Wavelet-Energien, die die relative Wavelet-Energie (oder die Wahrscheinlichkeitsverteilung) darstellen, werden die Wavelet-Entropien anhand der von Shannon gegebenen Definition der Entropie ermittelt. ⓘ
Nichtlineare Methoden
Angesichts der Komplexität der Mechanismen, die die Herzfrequenz regulieren, kann man davon ausgehen, dass die Anwendung der HRV-Analyse auf der Grundlage von Methoden der nichtlinearen Dynamik wertvolle Informationen liefern wird. Obwohl ein chaotisches Verhalten angenommen wurde, haben genauere Tests gezeigt, dass die Herzfrequenzvariabilität nicht als niedrigdimensionaler chaotischer Prozess beschrieben werden kann. Es hat sich jedoch gezeigt, dass die Anwendung von chaotischen Globalwerten auf die HRV den Diabetesstatus vorhersagen kann. Die am häufigsten verwendete nichtlineare Methode zur Analyse der Herzfrequenzvariabilität ist das Poincaré-Diagramm. Jeder Datenpunkt stellt ein Paar aufeinanderfolgender Schläge dar, die x-Achse ist das aktuelle RR-Intervall, die y-Achse ist das vorherige RR-Intervall. Die HRV wird quantifiziert, indem mathematisch definierte geometrische Formen an die Daten angepasst werden. Weitere Methoden sind die Korrelationsdimension, die symbolische Dynamik, die nichtlineare Vorhersagbarkeit, die punktweise Korrelationsdimension, die approximative Entropie, die Probenentropie, die Multiskalen-Entropie-Analyse, die Probenasymmetrie und die Speicherlänge (basierend auf der inversen statistischen Analyse). Es ist auch möglich, Langzeitkorrelationen geometrisch darzustellen. ⓘ
Langfristige Korrelationen
Es wurde festgestellt, dass Sequenzen von RR-Intervallen Langzeitkorrelationen aufweisen. Ein Schwachpunkt dieser Analysen ist jedoch das Fehlen von Anpassungsstatistiken, d. h. es werden Werte abgeleitet, die möglicherweise keine ausreichende statistische Strenge aufweisen. In verschiedenen Schlafstadien wurden unterschiedliche Arten von Korrelationen festgestellt. ⓘ
Dauer und Umstände der EKG-Aufzeichnung
Bei der Untersuchung von Kurzzeitaufzeichnungen werden Zeitbereichsmethoden den Frequenzbereichsmethoden vorgezogen. Dies ist darauf zurückzuführen, dass die Aufzeichnung mindestens das Zehnfache der Wellenlänge der niedrigsten interessierenden Frequenzgrenze betragen sollte. So ist für die Bewertung der HF-Komponenten der HRV eine Aufzeichnung von etwa 1 Minute erforderlich (d. h. eine untere Grenze von 0,15 Hz entspricht einem Zyklus von 6,6 Sekunden, so dass für 10 Zyklen ~60 Sekunden benötigt werden), während für die Untersuchung der NF-Komponente (mit einer unteren Grenze von 0,04 Hz) mehr als 4 Minuten erforderlich sind. ⓘ
Obwohl Zeitbereichsmethoden, insbesondere die SDNN- und RMSSD-Methoden, zur Untersuchung von Aufzeichnungen mit langer Dauer verwendet werden können, besteht ein wesentlicher Teil der Langzeitvariabilität aus Tag-Nacht-Unterschieden. Daher sollten Langzeitaufzeichnungen, die mit Zeitbereichsmethoden analysiert werden, mindestens 18 Stunden an analysierbaren EKG-Daten enthalten, die die gesamte Nacht umfassen. ⓘ
Physiologische Korrelate der HRV-Komponenten
Autonome Einflüsse auf die Herzfrequenz
Obwohl die Automatik des Herzens verschiedenen Schrittmachergeweben eigen ist, unterliegen Herzfrequenz und -rhythmus weitgehend der Kontrolle durch das autonome Nervensystem. Der parasympathische Einfluss auf die Herzfrequenz wird über die Freisetzung von Acetylcholin durch den Vagusnerv vermittelt. Muskarinische Acetylcholinrezeptoren reagieren auf diese Freisetzung hauptsächlich mit einer Erhöhung der K+-Leitfähigkeit der Zellmembran. Acetylcholin hemmt auch den durch Hyperpolarisation aktivierten "Schrittmacher"-Strom. Die "Ik-Decay"-Hypothese besagt, dass die Schrittmacherdepolarisation aus einer langsamen Deaktivierung des verzögerten Gleichrichterstroms Ik resultiert, der aufgrund eines zeitunabhängigen Hintergrund-Einwärtsstroms eine diastolische Depolarisation verursacht. Die Hypothese der "If-Aktivierung" besagt hingegen, dass If nach der Beendigung des Aktionspotenzials einen langsam aktivierenden Einwärtsstrom liefert, der gegenüber dem abklingenden Ik vorherrscht und somit eine langsame diastolische Depolarisation auslöst. ⓘ
Der sympathische Einfluss auf die Herzfrequenz wird durch die Freisetzung von Epinephrin und Norepinephrin vermittelt. Die Aktivierung von β-adrenergen Rezeptoren führt zu einer cAMP-vermittelten Phosphorylierung von Membranproteinen und zu einem Anstieg von ICaL und in If zu einer Beschleunigung der langsamen diastolischen Depolarisation. ⓘ
Unter Ruhebedingungen überwiegt der vagale Tonus, und die Schwankungen der Herzperiode sind weitgehend von der vagalen Modulation abhängig. Die vagale und die sympathische Aktivität interagieren ständig. Da der Sinusknoten reich an Acetylcholinesterase ist, ist die Wirkung eines vagalen Impulses nur von kurzer Dauer, da das Acetylcholin schnell hydrolysiert wird. Die parasympathischen Einflüsse übertreffen die sympathischen Wirkungen wahrscheinlich durch zwei unabhängige Mechanismen: eine cholinergisch induzierte Verringerung von Noradrenalin, das als Reaktion auf die sympathische Aktivität freigesetzt wird, und eine cholinerge Abschwächung der Reaktion auf einen adrenergen Stimulus. ⓘ
Komponenten
Die Schwankungen des RR-Intervalls im Ruhezustand stellen Schlag-zu-Schlag-Schwankungen der kardialen autonomen Inputs dar. Die efferente vagale (parasympathische) Aktivität trägt jedoch wesentlich zur HF-Komponente bei, wie klinische und experimentelle Beobachtungen von autonomen Manövern wie elektrischer vagaler Stimulation, Muskarinrezeptorblockade und Vagotomie zeigen. Problematischer ist die Interpretation der NF-Komponente, die von einigen als Marker für die sympathische Modulation angesehen wurde (insbesondere, wenn sie in normalisierten Einheiten ausgedrückt wird), von der aber inzwischen bekannt ist, dass sie sowohl sympathische als auch vagale Einflüsse umfasst. So geht beispielsweise bei einer sympathischen Aktivierung die resultierende Tachykardie in der Regel mit einer deutlichen Verringerung der Gesamtleistung einher, während bei einer vagalen Aktivierung das Gegenteil der Fall ist. Die Spektralkomponenten ändern sich also in die gleiche Richtung und lassen nicht darauf schließen, dass die LF die sympathischen Effekte getreu widerspiegelt. ⓘ
Die HRV misst die Schwankungen der autonomen Eingänge zum Herzen und nicht das mittlere Niveau der autonomen Eingänge. Daher können sowohl ein Entzug als auch ein sättigendes hohes Niveau des autonomen Inputs für das Herz zu einer verminderten HRV führen. ⓘ
Veränderungen im Zusammenhang mit bestimmten biologischen Zuständen und Pathologien
Eine Verringerung der HRV wurde bei verschiedenen kardiovaskulären und nicht kardiovaskulären Erkrankungen festgestellt. ⓘ
Myokardinfarkt
Eine erniedrigte HRV nach einem Myokardinfarkt kann auf eine Abnahme der auf das Herz gerichteten vagalen Aktivität zurückzuführen sein. Die HRV von Patienten, die einen akuten Herzinfarkt überlebt haben, zeigt eine Verringerung der Gesamtleistung und der individuellen Leistung der spektralen Komponenten. Das Vorhandensein einer veränderten neuronalen Steuerung spiegelt sich auch in einer Abstumpfung der Tag-Nacht-Schwankungen des RR-Intervalls wider. Bei Post-MI-Patienten mit einer sehr gedrückten HRV ist der größte Teil der Restenergie im VLF-Frequenzbereich unter 0,03 Hz verteilt, mit nur geringen atmungsbezogenen Schwankungen. ⓘ
Diabetische Neuropathie
Bei der mit Diabetes mellitus assoziierten Neuropathie, die durch eine Veränderung der kleinen Nervenfasern gekennzeichnet ist, scheint eine Verringerung der Zeitbereichsparameter der HRV nicht nur einen negativen prognostischen Wert zu haben, sondern auch der klinischen Ausprägung der autonomen Neuropathie vorauszugehen. Bei Diabetikern ohne Hinweise auf eine autonome Neuropathie wurde ebenfalls eine Verringerung der absoluten Leistung von LF und HF unter kontrollierten Bedingungen festgestellt. In ähnlicher Weise können Diabetiker anhand der Verringerung der HRV von normalen Kontrollpersonen unterschieden werden. ⓘ
Herztransplantation
Bei Patienten mit einer kürzlich erfolgten Herztransplantation wurde eine stark reduzierte HRV ohne eindeutige Spektralkomponenten festgestellt. Das Auftreten von diskreten Spektralkomponenten bei einigen wenigen Patienten wird als Ausdruck einer kardialen Reinnervation angesehen. Diese Reinnervation kann bereits 1 bis 2 Jahre nach der Transplantation auftreten, und es wird angenommen, dass sie einen sympathischen Ursprung hat. Darüber hinaus deutet eine Korrelation zwischen der Atemfrequenz und der HF-Komponente der HRV, die bei einigen transplantierten Patienten beobachtet wurde, darauf hin, dass ein nicht-neuraler Mechanismus eine atmungsbezogene rhythmische Oszillation erzeugen kann. ⓘ
Myokardiale Dysfunktion
Bei Patienten mit Herzinsuffizienz wurde durchweg eine reduzierte HRV beobachtet. Bei diesem Zustand, der durch Anzeichen einer sympathischen Aktivierung wie schnellere Herzfrequenzen und hohe Konzentrationen zirkulierender Katecholamine gekennzeichnet ist, wurde ein Zusammenhang zwischen Veränderungen der HRV und dem Ausmaß der linksventrikulären Dysfunktion festgestellt. Während die Verringerung der HRV im Zeitbereich parallel zum Schweregrad der Erkrankung zu verlaufen schien, scheint die Beziehung zwischen den Spektralkomponenten und den Indizes der ventrikulären Dysfunktion komplexer zu sein. Insbesondere konnte bei den meisten Patienten mit einem sehr fortgeschrittenen Krankheitsstadium und einer drastischen Verringerung der HRV trotz der klinischen Anzeichen einer sympathischen Aktivierung keine NF-Komponente nachgewiesen werden. Dies zeigt, dass die NF, wie bereits erwähnt, den kardialen Sympathikustonus möglicherweise nicht genau widerspiegelt. ⓘ
Leberzirrhose
Leberzirrhose ist mit einer verminderten HRV verbunden. Eine verminderte HRV bei Patienten mit Zirrhose hat einen prognostischen Wert und sagt die Sterblichkeit voraus. Ein Verlust der HRV wird auch mit höheren proinflammatorischen Zytokinspiegeln im Plasma und einer beeinträchtigten neurokognitiven Funktion bei dieser Patientengruppe in Verbindung gebracht. ⓘ
Sepsis
Da die Herzratenvariabilität ihren Ursprung in der Funktion des vegetativen Nervensystems hat, lassen sich prinzipiell Krankheiten erkennen, bei denen es darüber zu Auswirkungen auf den Herzschlag kommt. Dabei sind Erkrankungen zu unterscheiden, die direkt das autonome Nervensystem schädigen, und Krankheiten, die sich etwa über dauerhaft erhöhte Stoffwechselbeanspruchungen indirekt auf das autonome Nervensystem auswirken. ⓘ
Ein Beispiel für die erste Gruppe von Krankheiten ist die diabetische Neuropathie, eines aus der zweiten Gruppe die koronare Herzkrankheit. Auch psychische Erkrankungen können über eine Erhöhung des Katecholaminspiegels und die Sympathikusaktivierung erkennbare Folgen auf die Herzaktivität haben; die Herzfrequenzvariabilität kann daher auch im Bereich der Neuropsychiatrie zu diagnostischen Zwecken herangezogen werden. ⓘ
Weitere Erkrankungen mit Veränderungen der Herzratenvariabilität sind:
- Asphyxie bei Neugeborenen
- plötzlicher Herztod nach Herzinfarkt (als prädiktiver Wert)
- Asthma
- Traumapatienten, als prädiktiver Wert für die Mortalität, unabhängig von Mechanismus, Ort oder Schwere der Verletzung.
- Sepsis, schon vor klinischer Diagnosestellung der Sepsis beginnt die HRV abzufallen. ⓘ
Tetraplegie
Bei Patienten mit chronischen vollständigen Läsionen des hohen zervikalen Rückenmarks sind die efferenten vagalen Nervenbahnen, die zum Sinusknoten führen, intakt. Dennoch kann bei einigen Tetraplegikern eine NF-Komponente in der HRV und den arteriellen Druckschwankungen nachgewiesen werden. Somit stellt die NF-Komponente der HRV bei Patienten ohne intakte sympathische Eingänge zum Herzen eine vagale Modulation dar. ⓘ
Plötzlicher Herztod
Bei Opfern des plötzlichen Herztods wurde eine niedrigere HRV festgestellt als bei gesunden Personen. Die HRV kann bereits vor der Entwicklung des plötzlichen Herztods gesenkt sein, was die Frage aufwirft, ob eine veränderte autonome Funktion bei der Entwicklung der elektrischen Instabilität eine Rolle spielt. Die HRV ist auch bei Überlebenden von SCD erniedrigt, die ein hohes Risiko für weitere Anfälle haben. ⓘ
Krebs
Laut einer systematischen Überprüfung veröffentlichter Studien korreliert die HRV mit dem Krankheitsverlauf und dem Ergebnis von Krebspatienten. Patienten in den frühen Krebsstadien haben eine signifikant höhere HRV als Patienten in den späteren Krebsstadien, was darauf hindeutet, dass der Schweregrad der Erkrankung die HRV beeinflusst. Bei den verschiedenen Krebsarten sind unterschiedliche HRV-Spannen zu beobachten. ⓘ
Schwangerschaft
HRV-Veränderungen treten sowohl bei gesunden Schwangerschaften als auch bei Schwangerschaften mit Schwangerschaftsdiabetes auf, wozu auch niedrigere HRV-Mittelwerte gehören. ⓘ
Stimmungsschwankungen und Angstzustände
Niedrige RMSSD-Werte, von denen man annimmt, dass sie den Vagustonus repräsentieren, wurden mit schweren Depressionen in Verbindung gebracht. Eine niedrigere SDNN und eine erhöhte LF/HF wurden bei Patienten mit bipolarer Störung festgestellt, insbesondere bei solchen, die aufgrund der größeren Anzahl von Episoden, der Krankheitsdauer und des Vorliegens einer Psychose als schwerwiegendere Erkrankung eingestuft wurden. Bei Patienten mit PTBS war auch die HF, ein Maß für den Vagustonus, niedriger. ⓘ
Modifikationen durch spezifische Interventionen
Interventionen, die die HRV verbessern, können vor kardialer Mortalität und plötzlichem Herztod schützen. Die Gründe für eine Veränderung der HRV sind zwar stichhaltig, bergen aber auch die Gefahr, dass sie zu der ungerechtfertigten Annahme führen, dass eine Veränderung der HRV direkt zu einem Schutz des Herzens führt, was möglicherweise nicht der Fall ist. Trotz des wachsenden Konsenses, dass eine Erhöhung der vagalen Aktivität vorteilhaft sein kann, ist noch nicht bekannt, wie stark die vagale Aktivität (oder die HRV als Marker) ansteigen muss, um einen angemessenen Schutz zu bieten. ⓘ
β-adrenerge Blockade
Die Daten über die Wirkung von β-Blockern auf die HRV bei Patienten nach einem Herzinfarkt sind erstaunlich spärlich. Trotz der Beobachtung statistisch signifikanter Anstiege sind die tatsächlichen Veränderungen sehr bescheiden. Bei bewussten Hunden nach MI verändern β-Blocker die HRV nicht. Die unerwartete Beobachtung, dass eine β-Blockade vor einem Herzinfarkt die HRV nur bei den Tieren erhöht, die nach einem Herzinfarkt ein geringes Risiko für tödliche Arrhythmien haben, könnte neue Ansätze für eine Risikostratifizierung nach einem Herzinfarkt nahelegen. ⓘ
Antiarrhythmische Medikamente
Für mehrere Antiarrhythmika liegen Daten vor. Flecainid und Propafenon, nicht aber Amiodaron, verringerten bei Patienten mit chronischen ventrikulären Arrhythmien die HRV im Zeitbereich. In einer anderen Studie reduzierte Propafenon die HRV und verringerte die NF wesentlich stärker als die HF. Eine größere Studie bestätigte, dass Flecainid, aber auch Encainid und Moricizin die HRV bei Patienten nach Herzinfarkt verringerten, fand aber keine Korrelation zwischen der Veränderung der HRV und der Mortalität während der Nachbeobachtung. Somit können einige Antiarrhythmika, die mit einer erhöhten Sterblichkeit assoziiert sind, die HRV senken. Es ist jedoch nicht bekannt, ob diese Veränderungen der HRV eine direkte prognostische Bedeutung haben. ⓘ
Scopolamin
Niedrig dosierte Muskarinrezeptorblocker wie Atropin und Scopolamin können eine paradoxe Verstärkung der vagalen Wirkungen auf das Herz bewirken, wie ein Rückgang der Herzfrequenz vermuten lässt. Darüber hinaus können Scopolamin und niedrig dosiertes Atropin die HRV deutlich erhöhen. Obwohl die Verlangsamung der Herzfrequenz proportional zur (niedrigen) Atropin-Dosis ist, variiert der Anstieg der HRV stark zwischen und innerhalb von Personen. Dies deutet darauf hin, dass die HRV selbst für die vagale Aktivität des Herzens ein begrenzter Marker sein kann. ⓘ
Thrombolyse
Bei 95 Patienten mit akutem Herzinfarkt wurde die Wirkung der Thrombolyse auf die HRV (gemessen anhand von pNN50) untersucht. Die HRV war 90 Minuten nach der Thrombolyse bei den Patienten höher, bei denen die infarktnahe Arterie durchgängig war. Dieser Unterschied wurde jedoch nicht mehr deutlich, wenn die gesamten 24 Stunden analysiert wurden. ⓘ
Bewegungstraining
Bewegungstraining kann die kardiovaskuläre Sterblichkeit und den plötzlichen Herztod verringern. Es wird angenommen, dass regelmäßiges Bewegungstraining auch die autonome Kontrolle des Herzens verändert. Personen, die regelmäßig Sport treiben, haben eine "Trainingsbradykardie" (d. h. eine niedrige Ruheherzfrequenz) und weisen im Allgemeinen eine höhere HRV auf als Personen, die sich nicht bewegen. ⓘ
Biofeedback
In den letzten Jahrzehnten wurden verschiedene Biofeedback-Techniken und -Geräte entwickelt, um die Variabilität der Herzfrequenz zu messen. Dabei wurde besonderes Gewicht auf die Messung der Koppelung von Herz und Atmung gelegt, um so den Grad der Kohärenz bzw. Synchronisation von Herzrhythmus und Atemfrequenz bestimmen zu können. ⓘ
Synchronisation und chaotischer Verlauf von Atemrhythmus und Herzfrequenz sind bei diesen Biofeedback-Verfahren bildlich oder akustisch darstellbar. Die Messung des Pulses erfolgt dabei mit Hilfe eines Brustgurtes oder eines Ohrclips, wobei die Daten dabei auf spezielle Weise ausgewertet werden. ⓘ
Festgestellt wurde, dass bei so komplexen Reaktionen wie Liebe oder Dankbarkeit, die mit der emotionalen Reaktion der Freude verbunden sind, eine messbare Synchronisation der Rhythmen von Herz und Atmung (Respiratorische Sinusarrhythmie) erfolgt. Diese Balance zwischen Atmung und Herzschlag verschwindet jedoch bei Reaktionen wie Hetze („Stress“), Ärger oder Angst, die mit vermehrter Ausschüttung von Stresshormonen einhergehen. Einige Studien sowie Übersichtsarbeiten und Metaanalysen weisen darauf hin, dass die Herzfrequenzvariabilität psychisch Kranker niedriger ist als psychisch gesunden Personen. ⓘ
Von den USA ausgehend werden in den letzten Jahren zunehmend Forschungen unternommen um festzustellen, inwieweit Kohärenz von Herz und Atmung trainierbar ist, und welche Therapieerfolge mit unterschiedlichen Settings erreicht werden können. Dabei werden Biofeedback-Techniken eingesetzt und in verschiedenen Variationen das emotionale Erleben der Trainees zusätzlich oder alternativ gezielt zu beeinflussen gesucht. Dabei werden spezielle musikalische Kompositionen eingesetzt, Atemtechniken, Achtsamkeitsübungen, Tranceinduktionen oder gelenkte Imaginationen mit Konzentration auf Herz und Atmung in Verbindung mit der Aktivierung besonders positiver, etwa liebevoller Reaktionen. ⓘ
Das HRV-Biofeedback wird als Coaching-Methode oder komplementärmedizinische Methode schon länger in der verhaltenstherapeutisch orientierten Psychotherapie genutzt. Nach Studien in den USA sind dadurch Depressionen, Herzerkrankungen, Asthma, Angststörungen und Schlaflosigkeit günstig beeinflussbar. Die Verbesserung der Kohärenz von Atmung und Herz kann auch beim Abbau von Anspannungen helfen, bei der Bewältigung von Stress und Angst, und dazu beitragen, im Alltag gelassener zu reagieren. ⓘ
HRV-Biofeedback wird seit einiger Zeit in der betrieblichen Gesundheitsförderung eingesetzt. ⓘ
Laut einer 2017 veröffentlichten Studie kann HRV-Biofeedback auch angewandt werden, um die Leistungsfähigkeit von Sportlern zu verbessern. Die Autoren erwähnen aber auch den Bedarf an weiteren Studien. ⓘ
Auch bei Patienten, die an Atemnot, Müdigkeit oder Ödemen und zusätzlich unter Ängsten und Depressionen litten, half ein sechswöchiges Herzfrequenzvariabilitäts-Training. Allerdings hatte sich die Herzfrequenzvariabilität nicht verändert. ⓘ
Blasinstrumente
Eine Studie, die die physiologischen Auswirkungen des Spielens von indianischen Flöten untersuchte, fand einen signifikanten Anstieg der HRV sowohl beim Spielen von Flöten mit niedrigen als auch mit hohen Tönen. ⓘ
Normalwerte von Standardmaßen
Obwohl es keine allgemein akzeptierten Standardwerte für die HRV gibt, die für klinische Zwecke verwendet werden können, haben mehrere Studien Normalwerte für verschiedene Bevölkerungsgruppen gemessen und berichtet:
| Zeitbereichsanalyse | Spektralanalyse ⓘ | |||||
|---|---|---|---|---|---|---|
| Variable | Einheiten | Normalwerte (Mittelwert±SD) | Variable | Einheiten | Normalwerte (Mittelwert±SD) | |
| IBI | ms | 926±90 | LF | ms2 | 519±291 | |
| SDNN | ms | 50±16 | HF | ms2 | 657±777 | |
| RMSSD | ms | 42±15 | LF | nu | 52±10 | |
| HF | nu | 40±10 | ||||
| LF/HF-Verhältnis | 2.8±2.6 | |||||
Anfänge und aktueller Stand der HRV-Forschung
Bereits im 3. Jahrhundert nach Christus erkannte der chinesische Arzt Wang Shu-he (auch Wang Shu-ho oder Wang Hsi), dass ein variabler Herzschlag ein Zeichen für Gesundheit ist. Er dokumentierte dies in seinen Schriften Mai Ching (The Knowledge of Pulse Diagnosis). Da es keine Messinstrumente wie beispielsweise Stethoskop oder EKG gab, musste der Arzt sich sehr sensibel auf die Erfassung des Zusammenspiels der Körpersignale eines Patienten einstellen, um eine Krankheit daraus diagnostizieren zu können. Dass Wang Shu-he die Variabilität des Pulsschlags nicht zur Prognose verwendet hat, ist in "Von Spechten, Regentropfen und Herzschlägen … (s.u.)" nachzulesen. ⓘ
Aktuell existiert ein breites Forschungsspektrum zur Herzfrequenzvariabilität, das vorwiegend auf drei Bereiche konzentriert ist:
- Klinischer Bereich: Risikostratifizierung und Gesundheitsprognose mit Parametern der HRV
- Rehabilitative Medizin: klassische und nichtlineare HRV-Methoden für die Prognose- und Leistungsobjektivierung
- Stressmedizin und Psychophysiologie: HRV-Biofeedback ⓘ
Zur Leistungsdiagnostik und Belastungssteuerung wurden im Bereich der Sport- und Trainingswissenschaften neue Methoden entwickelt. ⓘ
Definition
Der Abstand zwischen zwei Herzschlägen wird meistens definiert als die Zeit zwischen dem Beginn zweier Kontraktionen der Herzkammern. Dieser Beginn der Kammerkontraktion erscheint im Elektrokardiogramm (EKG) als so genannte R-Zacke. Der Abstand zwischen zwei R-Zacken wird daher als RR-Intervall bezeichnet (Es wird auch von NN-Intervallen gesprochen: a) um eine Verwechslung mit der Blutdruckangabe RR (nach Riva-Rocci) zu vermeiden und b) um R-Zacken zu kennzeichnen, die einer regulären, also vom Sinusknoten ausgehenden Herzerregung entstammen – im Gegensatz z. B. zu supraventrikulären und ventrikulären Extrasystolen). Das RR-Intervall lässt sich als Kehrwert in die Herzfrequenz umrechnen (60 BPM ~ 1000 ms: 60 Beats per minute ~ 1000 Millisekunden RR-Abstand). Die RR-Intervalle sind im Regelfall nicht gleich lang, sondern unterliegen Schwankungen. Die Quantifizierung dieser Schwankungen bezeichnet man als Herzfrequenz- oder Herzratenvariabilität (HRV). ⓘ
Physiologie der Herzratenvariabilität
Ein Herzschlag wird beim gesunden Individuum durch einen Impuls des Sinusknotens als zentralem Taktgeber des autonomen Erregungssystems des Herzens ausgelöst. Dieses steht seinerseits unter dem Einfluss des übergeordneten vegetativen Nervensystems, wobei über den Sympathikus ein aktivierender Einfluss ausgeübt wird, der u. a. eine Erhöhung der Herzfrequenz zur Folge hat. Körperliche und psychische Belastungen gehen mit einer Steigerung der Aktivität des Sympathikus einher, während parallel dazu Körperfunktionen reduziert werden, die vom Vagus reguliert werden, wie etwa die Verdauung. Grob vereinfachend kann man sagen, dass der Sympathikus die Teilsysteme (Kreislauf, Muskulatur, Zucker) für Angriff und Flucht aktiviert, der Vagus im Gegenzug die hierfür erforderlichen Ressourcen aufbauen hilft, wenn sich der Mensch in einem entspannten Ruhezustand befindet. Äußere Einflüsse (Reize), psychische Vorgänge (Gedanken) oder mechanische Abläufe (Atmung) greifen dabei komplex ineinander, können sich dabei aber je nach eigenem Gewicht auch unterschiedlich auf den Herzschlag auswirken. ⓘ
Messverfahren


Das EKG ist nach wie vor zentrales Diagnoseverfahren in der Kardiologie. Aus ihm lässt sich eine sog. Zeitreihe der RR-Intervalle bestimmen. Die Schwankung dieser Zeitreihe lässt sich mit Hilfe verschiedener Verfahren hinsichtlich ihrer Stärke, Zeitskala oder innerer Muster quantifizieren. Im Vergleich zum normalen Elektrokardiogramm, bei dem die Kurvenform diagnostische Bedeutung hat, steht bei der Messung der Herzratenvariabilität die zeitliche Auflösung der RR-Abstände im Vordergrund. ⓘ
Eine einfache statistische Größe zur Bestimmung der Streuung ist die Standardabweichung der RR-Intervalle. Man unterscheidet heute drei Bereiche (Domänen), die zur Analyse der Herzfrequenzvariabilität genutzt werden:
- Zeitbereich (z. B. Standardabweichung der RR-Intervalle)
- Frequenzbereich (z. B. Spektrum der Herzfrequenzvariabilität)
- nichtlinearer Bereich (z. B. Poincaré-Abbildungen). ⓘ
Hinsichtlich ihrer Zeitskala lassen sich die Schwankungen der Herzfrequenz durch Verfahren der Spektralanalyse näher charakterisieren. In jüngerer Zeit werden auch komplexe empirische Parameter, wie z. B. die fraktale Dimension herangezogen. ⓘ
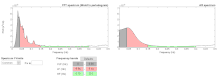
Die Spektralanalyse ist ein sehr genaues Verfahren zur Feststellung der Frequenzanteile, aus denen sich die Variabilität der Herzfrequenz zusammensetzt. Sie gibt beispielsweise Auskunft über die Kopplung von Atmung und Herzschlag (also deren Kohärenz) im entspannten Zustand. Sind Atmung und Herzschlag gut gekoppelt, ergibt die Spektralanalyse einen eindeutigen Peak (Spitzenwert). Das betreffende Mess-Spektrum wird in der HRV-Forschung in drei Frequenzbänder aufgeteilt, VLF (very low frequency), LF (low frequency, mitunter auch als MF (middle frequency) bezeichnet) und HF (high frequency), teilweise zuzüglich eines vierten Frequenzbandes: ULF (ultra low frequency). Diese Frequenzen repräsentieren
- HF, 0,15 – 0,4 Hz: Respiratorische Sinusarrhythmie
- LF, 0,04 – 0,15 Hz: Oszillationen des Baroreflexes
- VLF: peripher-zentrale Thermoregulation
(vgl.) ⓘ
Die respiratorische Sinusarrhythmie – und damit die HF – werden gemeinhin als Marker parasympathischer Aktivität angesehen. Es wurde und wird teilweise postuliert, die LF sei das sympathische Gegenstück zur HF und der Quotient LF/HF somit ein geeigneter Marker für die autonome Balance zwischen Sympathikus und Parasympathikus. Mittlerweile ist dies hinreichend widerlegt, dennoch wird LF/HF weiterhin in aktuellen Publikationen als Kennwert sympathovagaler Balance aufgeführt. ⓘ
Eine weitere Darstellungsform der Herzratenvariabilität ist das Histogramm. In einem Verlaufsdiagramm einer Biofeedback-Messung wird gezählt, wie viele der Herzschläge in eine bestimmte Klasse fallen. Bei größerer HRV verteilen sich die Herzschläge gleichmäßig über möglichst viele Klassen. Unter starker Belastung verschiebt sich die vegetative Balance und die HRV schränkt sich auf wenige Klassen ein. ⓘ
Zahlreiche Studien benutzen Poincaré- oder Lorenz-Plot zur Analyse der HRV mittels zwei- oder mehrdimensionaler Punktwolkendarstellungen. Bekannt sind verschiedene Bezeichnungen für die Darstellung sukzessiver RR-Abstände: Poincaré-, Lorenz-, Recurrence- und Scatter-Plot sowie Return Maps. Bei dieser Darstellung bezieht sich jeder folgende Datenpunkt auf den vorhergehenden, wobei im einfachsten Fall einer zweidimensionalen Darstellung die RR-Zeitreihe auf sich selbst abgebildet wird. ⓘ
Zur Vermeidung von Fehleinschätzungen der Bedeutung verschiedener Parameter der HRV wurden von Task Force of the European Society of Cardiology und The North American Society of Pacing and Electrophysiology Richtlinien festgelegt zur Durchführung und Interpretation von HRV-Analysen. ⓘ
HRV-gesteuertes Training im Spitzensport
Im Spitzensport wird in zunehmendem Maße die Trainingsbelastung mit HRV kontrolliert und gesteuert, um Überbelastungen zu vermeiden. So haben z. B. die vier neuseeländischen Ruderweltmeister 2015 ihr Training in den intensiven Phasen vor der Weltmeisterschaft mit HRV von Tag zu Tag periodisiert. Hierbei haben sie als Bezugsgröße den rMSSD (root mean square of successive differences = quadratischer Mittelwert der Differenzen aufeinanderfolgender R-R-Intervalle) herangezogen. Hierdurch kann rechnerisch die Wirkung einzelner Ausreißer minimiert werden. Da Ausdauersportler in der Regel bereits einen sehr niedrigen Ruhepuls haben, wird auch dem Einfluss des Parasympathikus Rechnung getragen. ⓘ