Natriumlaurylsulfat

| |
| |
| Bezeichnungen | |
|---|---|
| Bevorzugter IUPAC-Name
Natriumdodecylsulfat | |
| Andere Bezeichnungen
Natriummonododecylsulfat; Natriumlaurylsulfat; Natriummonolaurylsulfat; Natriumdodecansulfat; Natriumcocosulfat; Dodecylalkohol, Hydrogensulfat, Natriumsalz; n-Dodecylsulfat-Natrium; Schwefelsäuremonododecylester-Natriumsalz
| |
| Kennzeichnungsmittel | |
3D-Modell (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Arzneimittelbank | |
PubChem CID
|
|
| UNII | |
InChI
| |
SMILES
| |
| Eigenschaften | |
Chemische Formel
|
C12H25NaSO4 |
| Molare Masse | 288,372 g/mol |
| Erscheinungsbild | weißer oder cremefarbener Feststoff |
| Geruch | geruchlos |
| Dichte | 1,01 g/cm3 |
| Schmelzpunkt | 206 °C (403 °F; 479 K) |
| Oberflächenspannung: | |
CMC
|
8,2 mM bei 25 °C |
Brechungsindex (nD)
|
1.461 |
| Pharmakologie | |
ATC-Code
|
A06AG11 (WHO) |
| Gefahren | |
| Tödliche Dosis oder Konzentration (LD, LC): | |
LD50 (mittlere Dosis)
|
1288 mg/kg (Ratte, oral) |
| Verwandte Verbindungen | |
Andere Anionen
|
Natriumlaurethsulfat Natriummyrethsulfat |
Andere Kationen
|
Ammoniumlaurylsulfat Kaliumlaurylsulfat |
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa).
Infobox Referenzen
| |
Natriumdodecylsulfat (SDS) oder Natriumlaurylsulfat (SLS), manchmal auch Natriumlaurilsulfat geschrieben, ist eine organische Verbindung mit der Formel CH3(CH2)11OSO3Na. Es handelt sich um ein anionisches Tensid, das in vielen Reinigungs- und Hygieneprodukten verwendet wird. Diese Verbindung ist das Natriumsalz eines Organosulfats mit 12 Kohlenstoffatomen. Der Kohlenwasserstoffschwanz in Kombination mit einer polaren "Kopfgruppe" verleiht der Verbindung amphiphile Eigenschaften und macht sie somit zu einem nützlichen Reinigungsmittel. SDS ist auch Bestandteil von Mischungen, die aus preiswerten Kokosnuss- und Palmölen hergestellt werden. SDS ist ein häufiger Bestandteil vieler Haushaltsreinigungs-, Körperpflege-, Kosmetik-, Pharma- und Lebensmittelprodukte sowie industrieller und gewerblicher Reinigungs- und Produktformulierungen. ⓘ
| Strukturformel ⓘ | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
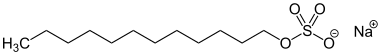
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Natriumlaurylsulfat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C12H25NaO4S | |||||||||||||||
| Kurzbeschreibung |
farbloser, geruchloser Feststoff | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 288,4 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
1,1 g·cm−3 bei 20 °C | |||||||||||||||
| Schmelzpunkt |
204–207 °C | |||||||||||||||
| Löslichkeit |
gut löslich in Wasser (150 g·l−1 bei 20 °C) | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten |
1290 mg·kg−1 (LD50, Ratte, oral) | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Natriumlaurylsulfat oder Natriumdodecylsulfat, auch SLS oder SDS (von englisch sodium lauryl sulfate und sodium dodecyl sulfate), ist ein anionisches Tensid, also eine waschaktive Substanz, das als Detergens Verwendung findet, z. B. in Reinigungsmitteln und Zahnpasta. ⓘ
Physikalisch-chemische Eigenschaften

Die kritische Mizellenkonzentration (CMC) in Wasser bei 25 °C beträgt 8,2 mM, und die Aggregationszahl bei dieser Konzentration wird üblicherweise mit etwa 62 angegeben. Der Mizellen-Ionisationsanteil (α) liegt bei etwa 0,3 (oder 30 %). ⓘ
Anwendungen
Reinigung und Hygiene
SDS wird hauptsächlich in Waschmitteln für zahlreiche Reinigungsanwendungen eingesetzt. Es ist ein hochwirksames Tensid und wird bei allen Aufgaben eingesetzt, die die Entfernung von öligen Flecken und Rückständen erfordern. So findet man es beispielsweise in höheren Konzentrationen in Industrieprodukten wie Motorentfettungsmitteln, Bodenreinigern und Außenreinigern für Autos. ⓘ
Es ist ein Bestandteil von Handseife, Zahnpasta, Shampoos, Rasierschaum und Schaumbädern, da es schaumbildend wirkt, oberflächenaktiv ist und zum Teil eine verdickende Wirkung hat. ⓘ
Lebensmittelzusatzstoff
Natriumdodecylsulfat, das auch unter dem Synonym Natriumlaurylsulfat (SLS) bekannt ist, gilt laut USFDA (21 CFR 172.822) als allgemein als sicher anerkannte Zutat für die Verwendung in Lebensmitteln (GRAS). Es wird als Emulgator und Aufschlaghilfe verwendet. Als Emulgator in oder mit Eiklar darf es nach dem United States Code of Federal Regulations nicht mehr als 1.000 parts per million (0,1 %) in festem Eiklar oder 125 parts per million (0,0125 %) in gefrorenem oder flüssigem Eiklar enthalten, und als Aufschlagmittel für die Zubereitung von Marshmallows darf es nicht mehr als 0,5 % des Gewichts der Gelatine enthalten. Es wird berichtet, dass SLS vorübergehend die Wahrnehmung von Süße vermindert. ⓘ
Anwendungen im Labor
Natriumlaurylsulfat diente früher in den meisten Shampoos und Duschgelen als reinigende Komponente. Heute ist es in diesen Anwendungen fast vollständig durch Natriumdodecylpoly(oxyethylen)sulfat (Natriumlaurethsulfat) ersetzt. Natriumlaurylsulfat wird als Emulgator in Salben und Lotionen sowie Reinigungsmitteln, vor allem in Handspülmitteln und flüssigen Waschmitteln verwendet. Die Behauptung, dass SLS in kosmetischen Produkten zu Haarausfall führen kann, ist nach aktueller Datenlage (2015) nicht wissenschaftlich belegt. ⓘ
Die intensive Anwendung als Denaturierungsmittel für Proteine ist ein Grund für die Bedeutung von Natriumlaurylsulfat in höheren Konzentrationen in der Biochemie und Biotechnologie. Die Wirkung auf Proteine basiert darauf, dass nichtkovalente Bindungen der Proteine unterbrochen und so deren Quartär- und Tertiärstruktur zerstört werden. Dabei bindet Natriumlaurylsulfat im Verhältnis von circa 1,4 Gramm SDS pro Gramm Protein. Durch die Eigenschaft, Mizellen auszubilden, sind Natriumlaurylsulfat-Protein-Lösungen nicht dialysierbar; eine Entfernung von Natriumlaurylsulfat ist durch Extraktionen mit organischen Lösungsmitteln möglich. ⓘ
In der biochemischen Analytik wird Natriumlaurylsulfat bei der Polyacrylamid-Gelelektrophorese (SDS-PAGE, von engl. Sodium Dodecyl Sulfate + Poly Acrylamid Gel Elektrophorese) verwendet. Da die meisten Proteine insgesamt fast neutral sind, behandelt man sie mit Laurylsulfat. Es denaturiert die Proteine nicht nur, sondern führt ihnen auch negative Ladungen zu. Somit wandern sie in der Elektrophorese zum positiven Pol. ⓘ
SDS wird in Reinigungsverfahren eingesetzt und wird üblicherweise als Komponente für die Lyse von Zellen bei der RNA-Extraktion und/oder DNA-Extraktion sowie für die Denaturierung von Proteinen zur Vorbereitung der Elektrophorese bei der SDS-PAGE-Technik verwendet. ⓘ
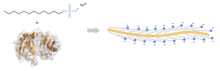
Bei der SDS-PAGE wirkt die Verbindung, indem sie die nicht-kovalenten Bindungen in den Proteinen aufbricht und sie somit denaturiert, d. h. die Proteinmoleküle verlieren ihre ursprüngliche Form und Gestalt. Durch die Bindung an die Proteine in einem Verhältnis von einem SDS-Molekül pro 2 Aminosäurereste verleiht das negativ geladene Detergens allen Proteinen eine ähnliche negative Nettoladung und damit ein ähnliches Verhältnis von Ladung zu Masse. Auf diese Weise kann der Unterschied in der Mobilität der Polypeptidketten im Gel allein auf ihre Länge zurückgeführt werden, im Gegensatz zu ihrer ursprünglichen Ladung und Form. Diese Trennung auf der Grundlage der Größe der Polypeptidkette vereinfacht die Analyse von Proteinmolekülen. ⓘ
Pharmazeutische Anwendungen
Natriumlaurylsulfat wird im pharmazeutischen Bereich häufig als ionischer Lösungsvermittler und Emulgator eingesetzt, der sich für Anwendungen in flüssigen Dispersionen, Lösungen, Emulsionen und Mikroemulsionen, Tabletten, Schäumen und halbfesten Stoffen wie Cremes, Lotionen und Gelen eignet. Außerdem trägt SLS zur Benetzbarkeit von Tabletten und zur Schmierung während der Herstellung bei. Markennamen für SLS in pharmazeutischer Qualität sind Kolliphor SLS und Kolliphor SLS Fine. ⓘ
Verschiedene Anwendungen
SLS wird in einer verbesserten Technik zur Präparation von Hirngewebe für die Untersuchung durch optische Mikroskopie verwendet. Diese Technik, die unter dem Namen CLARITY bekannt ist, wurde von Karl Deisseroth und seinen Mitarbeitern an der Stanford University entwickelt und umfasst die Infusion des Organs mit einer Acrylamidlösung, um die Makromoleküle des Organs (Proteine, Nukleinsäuren usw.) zu binden. ) zu binden, gefolgt von einer thermischen Polymerisation, um ein "Gehirn-Hydrogel" zu bilden (ein Netz, das über das gesamte Gewebe verteilt ist, um die Makromoleküle und andere Strukturen im Raum zu fixieren), und dann von einer Lipidentfernung mit SDS, um die Lichtstreuung bei minimalem Proteinverlust zu eliminieren, wodurch das Gewebe quasi transparent wird. ⓘ
Zusammen mit Natriumdodecylbenzolsulfonat und Triton X-100 werden wässrige SDS-Lösungen gerne zum Dispergieren oder Suspendieren von Nanoröhrchen, z. B. Kohlenstoffnanoröhrchen, verwendet. ⓘ
Nischenanwendungen
SLS wurde als potenziell wirksames topisches Mikrobizid zur intravaginalen Anwendung vorgeschlagen, um die Infektion durch verschiedene behüllte und unbehüllte Viren wie Herpes-simplex-Viren, HIV und das Semliki-Forest-Virus zu hemmen und möglicherweise zu verhindern. ⓘ
Flüssige Membranen, die aus SDS in Wasser gebildet werden, haben sich als ungewöhnliche Partikelabscheider erwiesen. Das Gerät wirkt wie ein umgekehrter Filter, der große Partikel durchlässt, während kleinere Partikel zurückgehalten werden. ⓘ
Herstellung
SDS wird synthetisiert, indem Laurylalkohol mit Schwefeltrioxid, Oleum oder Chlorschwefelsäure behandelt wird, um Laurylwasserstoffsulfat zu erzeugen. Laurylalkohol kann in reiner Form oder als Gemisch von Fettalkoholen verwendet werden. Die aus diesen Quellen hergestellten "SDS"-Produkte sind ein Gemisch aus verschiedenen Natriumalkylsulfaten, wobei SDS der Hauptbestandteil ist. Beispielsweise ist SDS zusammen mit anderen amphiphilen Stoffen mit hoher Kettenlänge ein Bestandteil, wenn es aus Kokosnussöl hergestellt wird, und ist als Natriumcocosulfat (SCS) bekannt. SDS ist im Handel in Pulver-, Pellet- und anderen Formen (die sich jeweils in der Auflösungsgeschwindigkeit unterscheiden) sowie in wässrigen Lösungen unterschiedlicher Konzentrationen erhältlich. ⓘ
Sicherheit
SDS ist nicht krebserregend. Wie alle Detergenzien entfernt Natriumlaurylsulfat Öle von der Haut und kann Haut- und Augenreizungen verursachen. Es hat sich gezeigt, dass es die Gesichtshaut von jungen Erwachsenen bei längerer und ständiger Exposition (mehr als eine Stunde) reizt. SDS kann Hautprobleme bei Personen mit chronischer Hautüberempfindlichkeit verschlimmern, wobei einige Personen stärker betroffen sind als andere. ⓘ
Orale Bedenken
Die niedrigen Kosten von SDS, die fehlende Auswirkung auf den Geschmack, die potenzielle Auswirkung auf flüchtige Schwefelverbindungen (VSC), die zu übelriechendem Atem beitragen, und die erwünschte Wirkung als Schaumbildner haben dazu geführt, dass SDS in Zahnpastaformulierungen verwendet wird. Eine Reihe kleiner Crossover-Studien (25-34 Patienten) haben die Wirksamkeit von SLS bei der Verringerung von VSCs und die damit verbundenen positiven Auswirkungen auf üblen Atemgeruch belegt, obwohl diese Studien im Allgemeinen auf technische Probleme bei der Kontrolle der Variablen des Studiendesigns zurückzuführen sind. Während primäre Quellen aus der Gruppe von Irma Rantanen an der Universität Turku, Finnland, zu dem Schluss kommen, dass SLS-haltige Pasten einen Einfluss auf Mundtrockenheit (Xerostomie) haben, kommt ein Cochrane-Review aus dem Jahr 2011 zu dem Schluss, dass es "keine überzeugenden Beweise dafür gibt, dass irgendeine topische Therapie wirksam ist, um das Symptom der Mundtrockenheit zu lindern." ⓘ
Auf der Grundlage mehrerer Studien wurden Sicherheitsbedenken hinsichtlich der Wirkung von Zahnpasta-SDS auf aphthöse Geschwüre (genauer gesagt, Mundgeschwüre oder "Krebsgeschwüre") geäußert, die gemeinhin als Krebsgeschwüre oder weiße Wunden bezeichnet werden. Nach Angaben des NHS ist SLS ein Grund zur Besorgnis bei Mundgeschwüren. Wie Lippert feststellt, enthalten 2013 "nur sehr wenige ... vermarktete Zahnpasten ein anderes Tensid als SLS [SDS]", und führende Hersteller formulieren ihre Produkte weiterhin mit SDS. ⓘ
Gewinnung und Darstellung
Natriumlaurylsulfat kann durch Veresterung von Dodecanol mit Schwefelsäure, Chlorsulfonsäure oder Schwefeltrioxid und nachfolgender Neutralisation gewonnen werden. Ebenso ist die Addition von Schwefelsäure an 1-Dodecen möglich. Da die verwendeten Ausgangsprodukte meist technische Fettalkohole sind, die zum Beispiel aus den entsprechenden Fetten bzw. Fettsäuren reduktiv gewonnen werden, enthalten die meisten Handelsprodukte neben Dodecyl- auch Tetradecyl- und Hexadecylketten in unterschiedlichen Anteilen. In technischen Merkblättern sind die entsprechenden Produkte (Stoffgemische) häufig mit dem Zusatz (C12-C16) gekennzeichnet. ⓘ
Nachweis
- Epton-Titration ⓘ


