Medizinprodukt



Ein Medizinprodukt ist jedes Gerät, das für medizinische Zwecke bestimmt ist. Die Verwendung eines Produkts zu medizinischen Zwecken birgt ein erhebliches Gefahrenpotenzial, und daher müssen Medizinprodukte mit hinreichender Sicherheit sicher und wirksam sein, bevor die Regulierungsbehörden die Vermarktung des Produkts in ihrem Land erlauben. Generell gilt: Je höher das mit dem Produkt verbundene Risiko ist, desto größer ist auch der Prüfaufwand für den Nachweis der Sicherheit und Wirksamkeit. Außerdem muss mit dem Risiko auch der potenzielle Nutzen für den Patienten zunehmen. ⓘ
Die Entdeckung dessen, was nach heutigen Maßstäben als Medizinprodukt gelten würde, reicht bis ca. 7000 v. Chr. in Belutschistan zurück, wo neolithische Zahnärzte Bohrer mit Feuersteinspitzen und Bogensehnen verwendeten. Untersuchungen der Archäologie und der römischen medizinischen Literatur zeigen auch, dass viele Arten von medizinischen Geräten in der Zeit des alten Roms weit verbreitet waren. In den Vereinigten Staaten wurden Medizinprodukte erst mit dem Federal Food, Drug, and Cosmetic Act (FD&C Act) von 1938 geregelt. Später, im Jahr 1976, wurde mit den Medical Device Amendments zum FD&C Act die Regulierung und Überwachung von Medizinprodukten, wie wir sie heute in den Vereinigten Staaten kennen, eingeführt. Die Regulierung von Medizinprodukten in Europa, wie wir sie heute kennen, trat 1993 mit der sogenannten Medizinprodukterichtlinie (MDD) in Kraft. Am 26. Mai 2017 wurde die MDD durch die Medical Device Regulation (MDR) ersetzt. ⓘ
Medizinprodukte unterscheiden sich sowohl in ihrem Verwendungszweck als auch in den Anwendungsgebieten. Die Beispiele reichen von einfachen, risikoarmen Produkten wie Zungenspateln, medizinischen Thermometern, Einweghandschuhen und Bettpfannen bis hin zu komplexen, risikoreichen Produkten, die implantiert werden und Leben erhalten. Ein Beispiel für Hochrisikogeräte sind Geräte mit eingebetteter Software wie Herzschrittmacher, die bei der Durchführung von medizinischen Tests, Implantaten und Prothesen helfen. Die Entwicklung medizinischer Geräte ist ein wichtiges Segment des Bereichs Biomedizintechnik. ⓘ
Der weltweite Markt für medizinische Geräte erreichte 2006 einen Wert von rund 209 Milliarden US-Dollar und wird für 2013 auf 220 bis 250 Milliarden US-Dollar geschätzt. Die Vereinigten Staaten kontrollieren ~40 % des Weltmarktes, gefolgt von Europa (25 %), Japan (15 %) und dem Rest der Welt (20 %). Obwohl Europa insgesamt einen größeren Anteil hat, ist Japan das Land mit dem zweitgrößten Marktanteil. Die größten Marktanteile in Europa (in der Reihenfolge der Marktanteilsgröße) haben Deutschland, Italien, Frankreich und das Vereinigte Königreich. Der Rest der Welt umfasst Regionen wie (in keiner bestimmten Reihenfolge) Australien, Kanada, China, Indien und Iran. In diesem Artikel wird erörtert, was ein Medizinprodukt in diesen verschiedenen Regionen ausmacht, und im gesamten Artikel werden diese Regionen in der Reihenfolge ihres Weltmarktanteils behandelt. ⓘ
Als Medizinprodukt werden unter anderem Apparate, Gegenstände, Stoffe und auch Software bezeichnet, die zu therapeutischen oder diagnostischen Zwecken für Menschen verwendet werden, wobei die bestimmungsgemäße Hauptwirkung im Unterschied zu Arzneimitteln primär nicht pharmakologisch, metabolisch oder immunologisch, sondern meist physikalisch oder physikochemisch erfolgt. Es gibt über 500.000 verschiedene Arten von Medizinprodukten und In-vitro-Diagnostika auf dem Europäischen Binnenmarkt (Stand 2017). ⓘ
Die Abgrenzung der Medizinprodukte zu Arzneimitteln ist bedeutsam, da Marktzugang und Verkehrsfähigkeit unterschiedlich geregelt sind. Die regulatorischen Voraussetzung zur Verkehrsfähigkeit unterscheiden sich grundlegend. ⓘ
Geschichte

Definition
Es ist schwierig, eine globale Definition für Medizinprodukte festzulegen, da es weltweit zahlreiche Regulierungsbehörden gibt, die die Vermarktung von Medizinprodukten überwachen. Obwohl diese Gremien oft zusammenarbeiten und die Definition im Allgemeinen diskutieren, gibt es feine Unterschiede im Wortlaut, die eine globale Harmonisierung der Definition eines Medizinprodukts verhindern, so dass die geeignete Definition eines Medizinprodukts von der Region abhängt. Oft dient ein Teil der Definition eines Medizinprodukts dazu, zwischen Medizinprodukten und Arzneimitteln zu unterscheiden, da die regulatorischen Anforderungen für beide unterschiedlich sind. In den Definitionen werden häufig auch In-vitro-Diagnostika als Unterklasse von Medizinprodukten anerkannt und Zubehör als Medizinprodukte festgelegt. ⓘ
Definitionen nach Region
Vereinigte Staaten (Food and Drug Administration)
Abschnitt 201(h) des Federal Food Drug & Cosmetic (FD&C) Act definiert ein Produkt als ein "Instrument, ein Apparat, eine Vorrichtung, ein Gerät, eine Maschine, eine Einrichtung, ein Implantat, ein In-vitro-Reagenz oder ein anderer ähnlicher oder verwandter Artikel, einschließlich eines Bauteils oder Zubehörs, das:
- in der offiziellen nationalen Arzneimittelliste (National Formulary) oder der Pharmakopöe der Vereinigten Staaten (United States Pharmacopoeia) oder einer Ergänzung dazu anerkannt sind
- zur Verwendung bei der Diagnose von Krankheiten oder anderen Zuständen oder zur Heilung, Linderung, Behandlung oder Vorbeugung von Krankheiten bei Menschen oder anderen Tieren bestimmt sind, oder
- die dazu bestimmt sind, die Struktur oder eine Funktion des Körpers von Menschen oder anderen Tieren zu beeinflussen, und
das seine primäre Zweckbestimmung nicht durch eine chemische Wirkung im oder auf den Körper des Menschen oder anderer Tiere erreicht und das zur Erreichung seiner primären Zweckbestimmung nicht vom Stoffwechsel abhängig ist. Der Begriff 'Gerät' umfasst keine Softwarefunktionen, die gemäß Abschnitt 520 Buchstabe o ausgeschlossen sind." ⓘ
Europäische Union
Nach Artikel 1 der Richtlinie 93/42/EWG des Rates ist ein "Medizinprodukt" jedes "Instrument, jeder Apparat, jede Vorrichtung, jede Software, jeder Stoff oder jeder sonstige Gegenstand, der/die einzeln oder in Verbindung miteinander verwendet wird, einschließlich der Software, die vom Hersteller speziell für diagnostische und/oder therapeutische Zwecke bestimmt und für die ordnungsgemäße Anwendung erforderlich ist, und der/die vom Hersteller zur Anwendung beim Menschen für folgende Zwecke bestimmt ist:
- Diagnose, Vorbeugung, Überwachung, Behandlung oder Linderung von Krankheiten,
- der Diagnose, Überwachung, Behandlung, Linderung oder Kompensation einer Verletzung oder Behinderung,
- Untersuchung, Ersatz oder Veränderung der Anatomie oder eines physiologischen Prozesses,
- Kontrolle der Empfängnis, ⓘ
und deren bestimmungsgemäße Hauptwirkung im oder am menschlichen Körper nicht durch pharmakologische, immunologische oder metabolische Mittel erreicht wird, die aber in ihrer Funktion durch solche Mittel unterstützt werden können." ⓘ
EU-Rechtsrahmen
Auf der Grundlage des neuen Konzepts wurden in den 1990er Jahren die Vorschriften für die Sicherheit und Leistung von Medizinprodukten in der EU harmonisiert. Das neue Konzept, das in einer Entschließung des Europäischen Rates vom Mai 1985 festgelegt wurde, stellt einen innovativen Weg der technischen Harmonisierung dar. Es zielt darauf ab, technische Handelshemmnisse zu beseitigen und die daraus resultierende Unsicherheit für die Wirtschaftsakteure zu beseitigen, um den freien Warenverkehr innerhalb der EU zu erleichtern. ⓘ
Der frühere grundlegende Rechtsrahmen bestand aus drei Richtlinien:
- der Richtlinie 90/385/EWG über aktive implantierbare medizinische Geräte
- Richtlinie 93/42/EWG über Medizinprodukte
- Richtlinie 98/79/EG über In-vitro-Diagnostika (bis 2022 wird die In-vitro-Diagnostika-Verordnung (IVDR) die derzeitige EU-Richtlinie über In-vitro-Diagnostika (98/79/EG) ersetzen). ⓘ
Sie zielen darauf ab, ein hohes Maß an Schutz der menschlichen Gesundheit und Sicherheit sowie das gute Funktionieren des Binnenmarktes zu gewährleisten. Diese drei Hauptrichtlinien wurden im Laufe der Zeit durch mehrere Änderungs- und Durchführungsrichtlinien ergänzt, darunter die letzte technische Überarbeitung durch die Richtlinie 2007/47 EG. ⓘ
Die Regierung eines jeden Mitgliedstaates muss eine für Medizinprodukte zuständige Behörde benennen. Die zuständige Behörde (CA) ist eine Stelle, die befugt ist, im Namen des Mitgliedstaates zu handeln, um sicherzustellen, dass die Regierung des Mitgliedstaates die Anforderungen der Richtlinien über Medizinprodukte in nationales Recht umsetzt und anwendet. Die zuständige Behörde untersteht dem Gesundheitsminister des Mitgliedstaates. Die zuständige Behörde eines Mitgliedstaates ist in keinem anderen Mitgliedstaat zuständig, tauscht aber Informationen aus und versucht, gemeinsame Standpunkte zu erreichen. ⓘ
Im Vereinigten Königreich fungiert beispielsweise die Medicines and Healthcare products Regulatory Agency (MHRA) als zuständige Behörde. In Italien ist es das Ministero Salute (Gesundheitsministerium). Medizinprodukte dürfen nicht mit Arzneimitteln verwechselt werden. In der EU müssen alle Medizinprodukte mit dem CE-Zeichen gekennzeichnet werden. Die Konformität eines Medizinprodukts mit mittlerem oder hohem Risiko mit den einschlägigen Vorschriften wird außerdem von einer externen Stelle, der Benannten Stelle, bewertet, bevor es in Verkehr gebracht werden kann. ⓘ
Im September 2012 schlug die Europäische Kommission neue Rechtsvorschriften vor, die die Sicherheit, Rückverfolgbarkeit und Transparenz verbessern sollen. Die Verordnung wurde im Jahr 2017 verabschiedet. ⓘ
Der künftige zentrale Rechtsrahmen besteht aus zwei Verordnungen, die die bisherigen drei Richtlinien ersetzen:
- Die Medizinprodukteverordnung (MDR (EU) 2017/745)
- Die Verordnung über In-vitro-Diagnostika (IVDR (EU) 2017/746) ⓘ
Japan .
Artikel 2, Absatz 4 des Pharmaceutical Affairs Law (PAL) definiert Medizinprodukte als "Instrumente und Apparate, die zur Diagnose, Heilung oder Vorbeugung von Krankheiten bei Menschen oder anderen Tieren bestimmt sind; die dazu bestimmt sind, die Struktur oder die Funktionen des Körpers von Menschen oder anderen Tieren zu beeinflussen." ⓘ
Rest der Welt
Kanada
Der Begriff Medizinprodukt wird im Food and Drugs Act wie folgt definiert: "Jeder Artikel, jedes Instrument, jeder Apparat oder jede Vorrichtung, einschließlich aller Komponenten, Teile oder Zubehörteile davon, der/die hergestellt, verkauft oder dargestellt wird zur Verwendung in: der Diagnose, Behandlung, Linderung oder Verhütung einer Krankheit, Störung oder eines anormalen körperlichen Zustands oder deren Symptome bei einem Menschen; der Wiederherstellung, Korrektur oder Veränderung einer Körperfunktion oder der Körperstruktur eines Menschen; der Diagnose einer Schwangerschaft bei einem Menschen; oder der Versorgung eines Menschen während der Schwangerschaft und bei und nach der Geburt eines Kindes, einschließlich der Versorgung des Kindes. Der Begriff umfasst auch ein Verhütungsmittel, nicht aber ein Arzneimittel". ⓘ
Der Begriff umfasst eine breite Palette von Gesundheits- oder Medizinprodukten, die zur Behandlung, Linderung, Diagnose oder Vorbeugung einer Krankheit oder eines anormalen körperlichen Zustands eingesetzt werden. Health Canada prüft Medizinprodukte auf ihre Sicherheit, Wirksamkeit und Qualität, bevor sie zum Verkauf in Kanada zugelassen werden. Gemäß dem Gesetz umfasst der Begriff Medizinprodukt keine Produkte, die für die Verwendung bei Tieren bestimmt sind. ⓘ
Nationale Ausnahmen
Im indischen Recht gibt es keine spezifische Definition des Begriffs "Medizinprodukte". Bestimmte Medizinprodukte sind jedoch nach dem Drugs & Cosmetics Act als DRUGS gemeldet. In Abschnitt 3 (b) (iv), der sich auf die Definition von "Arzneimitteln" bezieht, heißt es, dass "Geräte, die zur inneren oder äußeren Anwendung für die Diagnose, Behandlung, Linderung oder Verhütung von Krankheiten oder Störungen bei Menschen oder Tieren bestimmt sind", ebenfalls Arzneimittel sind. Ab April 2022 werden 14 Klassen von Produkten als Arzneimittel eingestuft. ⓘ
Jede nationale Gesetzgebung hat das Recht, zum Beispiel aus Sicherheitsgründen, bestimmte Medizinprodukte zu Arzneimitteln zu erklären (siehe auch Produktabgrenzung). Nicht möglich ist es dagegen, nur ein bestimmtes Medizinprodukt national anders als nach den EU-Richtlinien zu behandeln. ⓘ
In den meisten Ländern gelten Mundpflegemittel (Zahnpaste, Zahnbürste & Co) als Kosmetika, obgleich sie der Definition der Medizinprodukte entsprechen. ⓘ
Deutsche Ausnahmen
In-vivo-Diagnostika wie beispielsweise Kontrastmittel gelten nach dem deutschen Arzneimittelgesetz (AMG) als Arzneimittel. ⓘ
Zahnbürsten gelten nach deutschem Recht abweichend als Gegenstände des täglichen Bedarfs und nicht als Medizinprodukt. ⓘ
Österreichische Ausnahmen
Natürliche Heilvorkommen sowie auch daraus hergestellte Produkte gelten in Österreich nicht als Medizinprodukte. ⓘ
Ausnahmen in Schweden
Mundpflegemittel gelten in Schweden als Arzneimittel. ⓘ
Regulierung und Beaufsichtigung
Risikoklassifizierung
Die Aufsichtsbehörden unterscheiden verschiedene Klassen von Medizinprodukten auf der Grundlage ihres Schadenspotenzials bei unsachgemäßer Verwendung, der Komplexität der Konstruktion und ihrer Anwendungsmerkmale. Jedes Land oder jede Region definiert diese Kategorien auf unterschiedliche Weise. Die Behörden erkennen auch an, dass einige Produkte in Kombination mit Arzneimitteln angeboten werden, und bei der Regulierung dieser Kombinationsprodukte wird dieser Faktor berücksichtigt. ⓘ
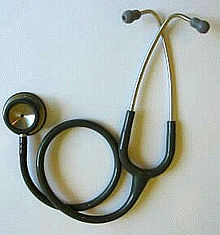
Die Einstufung von Medizinprodukten nach ihrem Risiko ist für die Sicherheit von Patienten und Personal unerlässlich und erleichtert gleichzeitig die Vermarktung von Medizinprodukten. Durch die Festlegung verschiedener Risikoklassifizierungen müssen Produkte mit geringerem Risiko, wie z. B. ein Stethoskop oder ein Zungenspatel, nicht denselben Prüfungen unterzogen werden wie Produkte mit höherem Risiko, wie z. B. ein künstlicher Herzschrittmacher. Die Festlegung einer Hierarchie der Risikoklassifizierung ermöglicht es den Regulierungsbehörden, bei der Überprüfung von Medizinprodukten flexibel vorzugehen. ⓘ
Klassifizierung nach Region
Vereinigte Staaten
Gemäß dem Food, Drug, and Cosmetic Act (Lebensmittel-, Arzneimittel- und Kosmetikgesetz) unterscheidet die U.S. Food and Drug Administration (FDA) drei Klassen von Medizinprodukten, die sich nach dem Grad der für die Gewährleistung von Sicherheit und Wirksamkeit erforderlichen Kontrollen richten.
- Klasse I
- Klasse II
- Klasse III ⓘ
| Geräteklasse | Risiko | FDA-Regulierungskontrolle | Beispiele ⓘ |
|---|---|---|---|
| Klasse I | Geringes Risiko | Allgemeine Kontrollen | Zunge, elektrische Zahnbürste, Pflaster, Krankenhausbetten |
| Klasse II | Mittleres Risiko | Allgemeine Kontrollen + Notifizierung vor dem Inverkehrbringen (510K) | Katheter, Kontaktlinsen, Schwangerschaftstestkits, |
| Klasse III | Hohes Risiko | Allgemeine Kontrollen + Spezielle Kontrollen (510K) + Genehmigung vor dem Inverkehrbringen (PMA) | Herzschrittmacher, Defibrillatoren, Implantatprothetik, Brustimplantate |
Die Klassifizierungsverfahren sind im Code of Federal Regulations, Titel 21, Teil 860 (gewöhnlich bekannt als 21 CFR 860) beschrieben. ⓘ
Produkte der Klasse I unterliegen der geringsten behördlichen Kontrolle und sind nicht dazu bestimmt, das Leben zu unterstützen oder zu erhalten oder wesentlich dazu beizutragen, Beeinträchtigungen der menschlichen Gesundheit zu verhindern, und sie dürfen kein unangemessenes Krankheits- oder Verletzungsrisiko darstellen. Beispiele für Produkte der Klasse I sind elastische Binden, Untersuchungshandschuhe und handgehaltene chirurgische Instrumente. ⓘ
Für Produkte der Klasse II gelten besondere Kennzeichnungsvorschriften, verbindliche Leistungsstandards und eine Überwachung nach dem Inverkehrbringen. Beispiele für Produkte der Klasse II sind Akupunkturnadeln, elektrische Rollstühle, Infusionspumpen, Luftreiniger, OP-Abdeckungen, stereotaktische Navigationssysteme und Operationsroboter. ⓘ
Bei Produkten der Klasse III handelt es sich in der Regel um Produkte, die das menschliche Leben unterstützen oder aufrechterhalten, die von wesentlicher Bedeutung für die Verhütung von Gesundheitsschäden sind oder die ein potenzielles, unangemessenes Krankheits- oder Verletzungsrisiko darstellen und eine Genehmigung vor dem Inverkehrbringen erfordern. Beispiele für Produkte der Klasse III sind implantierbare Herzschrittmacher, Pulsgeneratoren, HIV-Diagnosetests, automatische externe Defibrillatoren und enossale Implantate. ⓘ
Europäische Union (EU) und Europäische Freihandelsassoziation (EFTA)
Die Klassifizierung von Medizinprodukten in der Europäischen Union ist in Artikel IX der Richtlinie 93/42/EWG des Rates und in Anhang VIII der EU-Medizinprodukteverordnung festgelegt. Es gibt im Wesentlichen vier Klassen, die von geringem Risiko bis zu hohem Risiko reichen, die Klassen I, IIa, IIb und III (dies schließt In-vitro-Diagnostika einschließlich Software aus, die in vier Klassen fallen: von A (geringstes Risiko) bis D (höchstes Risiko)):
| Geräteklasse | Risiko | Beispiele ⓘ |
|---|---|---|
| Klasse I (Klasse I, Klasse Is, Klasse Im, Klasse Ir) | Geringes Risiko | Zunge, Rollstuhl, Brille |
| Klasse IIA | Mittleres Risiko | Hörgeräte, |
| Klasse IIB | Mittleres bis hohes Risiko | Beatmungsgeräte, Infusionspumpen |
| Klasse III | Hohes Risiko | Herzschrittmacher, Defibrillatoren, Implantatprothetik, Brustimplantate |
Produkte der Klasse I: Nicht-invasive, alltägliche Geräte oder Ausrüstungen. Produkte der Klasse I sind im Allgemeinen mit einem geringen Risiko behaftet und können Bandagen, Kompressionsstrümpfe oder Gehhilfen umfassen. Für solche Produkte muss der Hersteller lediglich ein technisches Dossier ausfüllen. ⓘ
Produkte der Klasse I: Bei Produkten der Klasse I handelt es sich in ähnlicher Weise um nicht-invasive Produkte, allerdings umfasst diese Untergruppe auch sterile Produkte. Beispiele für Produkte der Klasse I sind Stethoskope, Untersuchungshandschuhe, Kolostomiebeutel oder Sauerstoffmasken. Auch für diese Produkte ist ein technisches Dossier erforderlich, wobei zusätzlich ein Antrag bei einer europäischen benannten Stelle auf Zertifizierung der Herstellung in Verbindung mit Sterilitätsstandards gestellt werden muss. ⓘ
Produkte der Klasse Im: Dies bezieht sich hauptsächlich auf Messgeräte mit ähnlich geringem Risiko. Zu dieser Kategorie gehören: Thermometer, Tropfer und nicht-invasive Blutdruckmessgeräte. Auch hier muss der Hersteller ein technisches Dossier vorlegen und von einer europäischen benannten Stelle für die Herstellung in Übereinstimmung mit den messtechnischen Vorschriften zertifiziert sein. ⓘ
Produkte der Klasse IIa: Produkte der Klasse IIa stellen im Allgemeinen ein geringes bis mittleres Risiko dar und beziehen sich hauptsächlich auf Produkte, die kurzfristig im Körper installiert werden. Produkte der Klasse IIa sind Produkte, die nur zwischen 60 Minuten und 30 Tagen im Körper installiert sind. Beispiele hierfür sind Hörgeräte, Bluttransfusionsschläuche und Katheter. Zu den Anforderungen gehören technische Unterlagen und eine Konformitätsprüfung, die von einer europäischen benannten Stelle durchgeführt wird. ⓘ
Produkte der Klasse IIb: Produkte der Klasse IIb sind etwas komplexer als Produkte der Klasse IIa und bergen in der Regel ein mittleres bis hohes Risiko. Sie werden häufig für einen Zeitraum von 30 Tagen oder länger im Körper installiert. Beispiele hierfür sind Beatmungsgeräte und Überwachungsgeräte für die Intensivpflege. Der Weg zur Einhaltung der Vorschriften ist der gleiche wie bei Produkten der Klasse IIa, wobei zusätzlich eine Baumusterprüfung durch eine benannte Stelle erforderlich ist. ⓘ
Produkte der Klasse III: Bei Produkten der Klasse III handelt es sich ausschließlich um Produkte mit hohem Risiko. Beispiele hierfür sind Ballonkatheter, Herzklappenprothesen, Herzschrittmacher usw. Die Schritte bis zur Zulassung umfassen ein vollständiges Audit des Qualitätssicherungssystems sowie die Prüfung der Produktauslegung und des Produkts selbst durch eine europäische benannte Stelle. ⓘ
Die Zulassung von Medizinprodukten wird durch eine Konformitätserklärung gewährleistet. Diese Erklärung wird vom Hersteller selbst ausgestellt, muss aber bei Produkten der Klassen Is, Im, Ir, IIa, IIb oder III durch eine von einer benannten Stelle ausgestellte Konformitätsbescheinigung überprüft werden. Eine benannte Stelle ist eine öffentliche oder private Organisation, die akkreditiert wurde, um die Übereinstimmung des Produkts mit der europäischen Richtlinie zu validieren. Medizinprodukte der Klasse I (unter der Voraussetzung, dass sie nicht sterilisiert werden müssen oder keine Funktion messen) können durch reine Selbstzertifizierung vermarktet werden. ⓘ
Die europäische Klassifizierung hängt von Regeln ab, die die Dauer des Körperkontakts, den invasiven Charakter, die Verwendung einer Energiequelle, die Auswirkung auf den zentralen Kreislauf oder das Nervensystem, die diagnostische Wirkung oder die Beigabe eines Arzneimittels betreffen. Zertifizierte Medizinprodukte sollten auf der Verpackung, den Beipackzetteln usw. das CE-Zeichen tragen. Diese Verpackungen sollten auch harmonisierte Piktogramme und EN-genormte Logos aufweisen, um wesentliche Merkmale wie Gebrauchsanweisung, Verfallsdatum, Hersteller, steril, nicht wiederverwenden usw. anzugeben. ⓘ
Im November 2018 entschied das Bundesverwaltungsgericht der Schweiz, dass die App "Sympto", die zur Analyse des Menstruationszyklus einer Frau verwendet wird, ein Medizinprodukt ist, weil sie anhand persönlicher Daten ein Fruchtbarkeitsfenster für jede Frau berechnet. Der Hersteller, die Stiftung Sympto-Therm, argumentierte, dass es sich um ein didaktisches und nicht um ein medizinisches Verfahren handele. Das Gericht legte fest, dass eine App ein Medizinprodukt ist, wenn sie für einen der gesetzlich vorgesehenen medizinischen Zwecke verwendet werden soll und Gesundheitsinformationen durch Berechnungen oder Vergleiche erstellt oder verändert, die Informationen über einen einzelnen Patienten liefern. ⓘ
Japan .
Medizinprodukte (mit Ausnahme von In-vitro-Diagnostika) werden in Japan je nach Risiko in vier Klassen eingeteilt:
| Geräteklasse | Risiko ⓘ |
|---|---|
| Klasse I | Unbedeutend |
| Klasse II | Gering |
| Klasse III | Hohes Risiko einer Fehlfunktion |
| Klasse IV | Hohes Risiko könnte lebensbedrohlich sein |
Die Klassen I und II unterscheiden zwischen Produkten mit extrem niedrigem und niedrigem Risiko. Bei den Klassen III und IV, mäßiges bzw. hohes Risiko, handelt es sich um stark und speziell kontrollierte Medizinprodukte. Für In-vitro-Diagnostika gibt es drei Risikoklassifizierungen. ⓘ
Rest der Welt
In den übrigen Regionen der Welt ähneln die Risikoklassifizierungen im Allgemeinen denen der Vereinigten Staaten, der Europäischen Union und Japans oder stellen eine Variante dar, die zwei oder mehr der Risikoklassifizierungen der drei Länder kombiniert. ⓘ
Australien
Die Klassifizierung von Medizinprodukten in Australien ist in Abschnitt 41BD des Therapeutic Goods Act 1989 und in Vorschrift 3.2 der Therapeutic Goods Regulations 2002 festgelegt und wird von der Therapeutic Goods Administration kontrolliert. Ähnlich wie bei der EU-Klassifizierung werden die Produkte in mehrere Kategorien eingeteilt, und zwar in der Reihenfolge des zunehmenden Risikos und des damit verbundenen erforderlichen Kontrollniveaus. Die Produktkategorie wird durch verschiedene Vorschriften festgelegt ⓘ
| Einstufung | Grad des Risikos ⓘ |
|---|---|
| Klasse I | Gering |
| Klasse I - messend oder Klasse I - steril geliefert oder Klasse IIa | Gering - mittel |
| Klasse IIb | Mittel - hoch |
| Klasse III | Hoch |
| Aktive implantierbare medizinische Geräte (AIMD) | Hoch |
Kanada
Das Medical Devices Bureau von Health Canada erkennt vier Klassen von Medizinprodukten an, die sich nach dem Grad der Kontrolle richten, der erforderlich ist, um die Sicherheit und Wirksamkeit des Produkts zu gewährleisten. Geräte der Klasse I stellen das geringste potenzielle Risiko dar und erfordern keine Zulassung. Für Produkte der Klasse II ist eine Erklärung des Herstellers über die Sicherheit und Wirksamkeit des Produkts erforderlich, während Produkte der Klassen III und IV ein größeres potenzielles Risiko darstellen und einer eingehenden Prüfung unterzogen werden. Ein Leitfaden für die Klassifizierung von Produkten wird von Health Canada veröffentlicht. ⓘ
Die kanadischen Klassen für Medizinprodukte entsprechen der Richtlinie 93/42/EWG (MDD) des Europäischen Rates:
- Klasse I (Kanada) entspricht im Allgemeinen der Klasse I (ECD)
- Klasse II (Kanada) entspricht im Allgemeinen der Klasse IIa (ECD)
- Klasse III (Kanada) entspricht im Allgemeinen der Klasse IIb (ECD)
- Klasse IV (Kanada) entspricht im Allgemeinen der Klasse III (ECD)
Beispiele sind chirurgische Instrumente (Klasse I), Kontaktlinsen und Ultraschallscanner (Klasse II), orthopädische Implantate und Hämodialysegeräte (Klasse III) sowie Herzschrittmacher (Klasse IV). ⓘ
Indien
Medizinprodukte werden in Indien von der Central Drugs Standard Control Organisation (CDSCO) reguliert. Die Medizinprodukte werden gemäß den Medical Devices Rules, 2017, auf der Grundlage der Global Harmonization Task Force (GHTF) nach den damit verbundenen Risiken klassifiziert. ⓘ
| Geräteklasse | Risiko | Beispiele ⓘ |
|---|---|---|
| Klasse A | Geringes Risiko | Zunge, Rollstuhl, Brille, Alkoholtupfer |
| Klasse B | Geringes bis mittleres Risiko | Hörgeräte, Thermometer |
| Klasse C | Mäßiges bis hohes Risiko | Beatmungsgeräte, Infusionspumpen |
| Klasse D | Hohes Risiko | Herzschrittmacher, Defibrillatoren, Implantatprothetik, Brustimplantate |
Iran
Im Iran werden etwa 2.000 Arten von Medizinprodukten und medizinischem Bedarf hergestellt, z. B. Geräte, zahnmedizinischer Bedarf, sterile medizinische Einwegartikel, Labormaschinen, verschiedene Biomaterialien und Zahnimplantate. 400 Medizinprodukte werden in den Risikoklassen C und D hergestellt, die alle vom iranischen Gesundheitsministerium in Bezug auf Sicherheit und Leistung auf der Grundlage der EU-Normen zugelassen sind. ⓘ
Einige iranische Medizinprodukte werden nach den Normen der Europäischen Union hergestellt. ⓘ
Einige iranische Hersteller exportieren medizinische Geräte und Zubehör, die den Normen der Europäischen Union entsprechen, in Bewerberländer, darunter 40 asiatische und europäische Länder. ⓘ
Einige iranische Hersteller exportieren ihre Produkte in andere Länder. ⓘ
Normung und regulatorische Belange
Die ISO-Normen für Medizinprodukte werden durch ICS 11.100.20 und 11.040.01 abgedeckt. Das Qualitäts- und Risikomanagement zu diesem Thema für regulatorische Zwecke wird durch ISO 13485 und ISO 14971 geregelt. Die ISO 13485:2016 ist für alle Anbieter und Hersteller von Medizinprodukten, Komponenten, Vertragsdienstleistungen und Vertreiber von Medizinprodukten anwendbar. Die Norm ist die Grundlage für die Einhaltung von Vorschriften auf lokalen Märkten und den meisten Exportmärkten. Darüber hinaus hat die ISO 9001:2008 Vorrang, da sie besagt, dass ein Unternehmen sich mit der Entwicklung neuer Produkte beschäftigt. Sie verlangt, dass die Entwicklung der hergestellten Produkte einen Genehmigungsprozess und eine Reihe strenger Qualitätsstandards und Entwicklungsaufzeichnungen durchläuft, bevor das Produkt vertrieben wird. Weitere Normen sind IEC 60601-1 für elektrische Geräte (sowohl netzbetriebene als auch batteriebetriebene), EN 45502-1 für aktive implantierbare medizinische Geräte und IEC 62304 für medizinische Software. Die US-amerikanische FDA hat ebenfalls eine Reihe von Richtlinien für die Industrie zu diesem Thema veröffentlicht (21 CFR 820 Subchapter H-Medical Devices). Unterabschnitt B enthält Anforderungen an das Qualitätssicherungssystem, ein wichtiger Bestandteil davon sind Designkontrollen (21 CFR 820.30). Um den Anforderungen dieser Industrienormen gerecht zu werden, stellen immer mehr Händler von Medizinprodukten das Beschwerdemanagement in den Vordergrund ihrer Qualitätsmanagementpraktiken. Dieser Ansatz trägt zur Risikominderung bei und erhöht die Sichtbarkeit von Qualitätsproblemen. ⓘ
In den späten 1980er Jahren begann die FDA, die Entwicklung von Software für medizinische Geräte verstärkt zu überprüfen. Auslöser für diesen Wandel war ein Strahlentherapiegerät (Therac-25), bei dem es aufgrund von Software-Kodierungsfehlern zu einer Überdosierung von Patienten kam. Die FDA konzentriert sich nun auf die behördliche Aufsicht über den Entwicklungsprozess von Software für medizinische Geräte und die Tests auf Systemebene. ⓘ
Eine 2011 in den Archives of Internal Medicine veröffentlichte Studie von Dr. Diana Zuckerman und Paul Brown vom National Center for Health Research sowie von Dr. Steven Nissen von der Cleveland Clinic zeigte, dass die meisten Medizinprodukte, die in den letzten fünf Jahren wegen "schwerwiegender Gesundheitsprobleme oder Todesfällen" zurückgerufen wurden, zuvor von der FDA nach dem weniger strengen und kostengünstigeren 510(k)-Verfahren zugelassen worden waren. In einigen wenigen Fällen waren die Geräte als so risikoarm eingestuft worden, dass sie keiner behördlichen Prüfung durch die FDA unterzogen wurden. Von den 113 zurückgerufenen Geräten waren 35 auf kardiovaskuläre Probleme zurückzuführen. Diese Studie war Gegenstand von Anhörungen im Kongress, bei denen die Verfahren und die Aufsicht der FDA neu bewertet wurden. ⓘ
Eine 2014 in JAMA Internal Medicine veröffentlichte Studie von Dr. Diana Zuckerman, Paul Brown und Dr. Aditi Das vom National Center for Health Research untersuchte die öffentlich zugänglichen wissenschaftlichen Erkenntnisse über medizinische Implantate, die von 2008 bis 2012 im Rahmen des 510(k)-Verfahrens der FDA genehmigt wurden. Sie fanden heraus, dass wissenschaftliche Nachweise, die die "wesentliche Gleichwertigkeit" mit anderen bereits auf dem Markt befindlichen Produkten belegen, zwar gesetzlich vorgeschrieben sind, aber nur für 16 % der zufällig ausgewählten Implantate öffentlich zugänglich waren, und nur 10 % lieferten klinische Daten. Von den mehr als 1.100 Prädikatsimplantaten, denen die neuen Implantate im Wesentlichen gleichwertig waren, lagen nur für 3 % öffentlich zugängliche wissenschaftliche Nachweise vor, und nur für 1 % gab es klinische Nachweise der Sicherheit oder Wirksamkeit. Die Forscher kamen zu dem Schluss, dass öffentlich zugängliche wissenschaftliche Nachweise für Implantate erforderlich sind, um die öffentliche Gesundheit zu schützen. ⓘ
In den Jahren 2014 und 2015 wurde ein neues internationales Abkommen, das Medical Device Single Audit Program (MDSAP), mit fünf Teilnehmerländern geschlossen: Australien, Brasilien, Kanada, Japan und die Vereinigten Staaten. Ziel dieses Programms war es, "ein Verfahren zu entwickeln, das ein einziges Audit bzw. eine einzige Inspektion ermöglicht, um sicherzustellen, dass die regulatorischen Anforderungen für Medizinprodukte in allen fünf Ländern erfüllt werden". ⓘ
Im Jahr 2017 wurde eine Studie von Dr. Jay Ronquillo und Dr. Diana Zuckerman in der Fachzeitschrift Milbank Quarterly veröffentlicht, in der festgestellt wurde, dass elektronische Gesundheitsakten und andere Gerätesoftware aufgrund von lebensbedrohlichen Fehlern zurückgerufen wurden. In dem Artikel wird auf die fehlenden Schutzmaßnahmen gegen Hackerangriffe und andere Bedrohungen der Cybersicherheit hingewiesen und festgestellt, dass die derzeitigen Vorschriften zwar notwendig, aber nicht ausreichend sind, um die Sicherheit der Patienten durch die Identifizierung und Beseitigung gefährlicher Fehler in der derzeit auf dem Markt befindlichen Software zu gewährleisten". Sie fügten hinzu, dass die Gesetzesänderungen, die sich aus dem Gesetz mit dem Titel 21st Century Cures Act ergeben, "die Gesundheits-IT weiter deregulieren und Schutzmaßnahmen verringern werden, die die Meldung und den rechtzeitigen Rückruf von fehlerhafter medizinischer Software, die Patienten schaden könnte, erleichtern". ⓘ
Eine Studie von Dr. Stephanie Fox-Rawlings und Kollegen am National Center for Health Research, die 2018 in der politischen Fachzeitschrift Milbank Quarterly veröffentlicht wurde, untersuchte, ob Studien, die von der FDA für Hochrisiko-Medizinprodukte überprüft werden, für Frauen, Minderheiten oder Patienten über 65 Jahre sicher und wirksam sind. Das Gesetz fördert die Patientenvielfalt in klinischen Studien, die der FDA zur Prüfung vorgelegt werden, schreibt sie aber nicht vor. Die Studie ergab, dass die meisten Medizinprodukte mit hohem Risiko nicht getestet und analysiert werden, um sicherzustellen, dass sie für alle wichtigen demografischen Gruppen, insbesondere für rassische und ethnische Minderheiten und Menschen über 65 Jahren, sicher und wirksam sind. Daher liefern sie keine Informationen über Sicherheit oder Wirksamkeit, die Patienten und Ärzten helfen würden, fundierte Entscheidungen zu treffen. ⓘ
Im Jahr 2018 forderte eine Untersuchung, an der Journalisten aus 36 Ländern beteiligt waren und die vom International Consortium of Investigative Journalists (ICIJ) koordiniert wurde, Reformen in den Vereinigten Staaten, insbesondere im Zusammenhang mit dem 510(k)-Verfahren zur substanziellen Äquivalenz; die Untersuchung führte zu ähnlichen Forderungen im Vereinigten Königreich und in der Europäischen Union. ⓘ
Verpackungsnormen

Die Verpackung von Medizinprodukten ist streng geregelt. Häufig werden medizinische Geräte und Produkte bereits in der Verpackung sterilisiert. Die Sterilität muss während des gesamten Vertriebs aufrechterhalten werden, damit sie von den Ärzten sofort verwendet werden können. Eine Reihe von speziellen Verpackungstests misst die Fähigkeit der Verpackung, die Sterilität aufrechtzuerhalten. Zu den einschlägigen Normen gehören:
- ASTM F2097 - Standard Guide for Design and Evaluation of Primary Flexible Packaging for Medical Products
- ASTM F2475-11 - Standard Guide for Biocompatibility Evaluation of Medical Device Packaging Materials
- EN 868 Verpackungsmaterialien und -systeme für zu sterilisierende Medizinprodukte, Allgemeine Anforderungen und Prüfverfahren
- ISO 11607 Verpackungen für in der Endphase sterilisierte Medizinprodukte ⓘ
Die Prüfung von Verpackungen ist Teil eines Qualitätsmanagementsystems einschließlich Verifizierung und Validierung. Es ist wichtig, zu dokumentieren und sicherzustellen, dass die Verpackungen den Vorschriften und den Anforderungen der Endanwendung entsprechen. Die Herstellungsprozesse müssen kontrolliert und validiert werden, um eine gleichbleibende Leistung zu gewährleisten. Die Norm EN ISO 15223-1 definiert Symbole, die zur Übermittlung wichtiger Informationen auf Verpackungen und Etiketten verwendet werden können. ⓘ
Normen zur Biokompatibilität
- ISO 10993 - Biologische Bewertung von Medizinprodukten ⓘ
Sauberkeitsnormen
Seit dem Jahr 2000, als Sulzer Orthopedics mehrere Tausend metallische Hüftimplantate zurückrief, die Rückstände aus der Herstellung enthielten, wird die Sauberkeit von Medizinprodukten immer genauer unter die Lupe genommen. Aufgrund dieses Ereignisses richtete ASTM eine neue Arbeitsgruppe (F04.15.17) ein, die Prüfmethoden, Leitfäden und andere Normen für die Sauberkeit von Medizinprodukten erarbeitet. Diese Arbeitsgruppe hat bisher zwei Normen für permanente Implantate herausgegeben: 1. ASTM F2459: Standardtestverfahren zur Extraktion von Rückständen aus metallischen medizinischen Komponenten und Quantifizierung mittels gravimetrischer Analyse 2. ASTM F2847: Standard Practice for Reporting and Assessment of Residues on Single Use Implants 3. ASTM F3172: Standard Guide for Validating Cleaning Processes Used During the Manufacture of Medical Devices ⓘ
Darüber hinaus hat die Sauberkeit von wiederverwendbaren Produkten zu einer Reihe von Normen geführt, darunter:
- ASTM E2314: Standard Test Method for Determination of Effectiveness of Cleaning Processes for Reusable Medical Instruments Using a Microbiologic Method (Simulated Use Test)".
- ASTM D7225: Standardleitfaden für die Blutreinigungseffizienz von Reinigungsmitteln und Reinigungs-Desinfektionsgeräten
- ASTM F3208: Standardleitfaden für die Auswahl von Testböden zur Validierung von Reinigungsmethoden für wiederverwendbare medizinische Geräte ⓘ
Die Arbeitsgruppe ASTM F04.15.17 arbeitet an mehreren neuen Normen, die sich mit der Gestaltung von Implantaten für die Reinigung, der Auswahl und Prüfung von Bürsten für die Reinigung von wiederverwendbaren Produkten und der Bewertung der Reinigung von Medizinprodukten aus der additiven Fertigung befassen. Darüber hinaus erstellt die FDA neue Richtlinien für die Aufbereitung von wiederverwendbaren Medizinprodukten wie orthoskopischen Rasierern, Endoskopen und Absaugschläuchen. Neue Forschungsergebnisse wurden in ACS Applied Interfaces and Material veröffentlicht, um medizinische Werkzeuge frei von Krankheitserregern zu halten. ⓘ
Design, Prototyping und Produktentwicklung
Die Herstellung medizinischer Geräte erfordert je nach Klassifizierung des Geräts ein bestimmtes Maß an Prozesskontrolle. Höheres Risiko; mehr Kontrollen. In der anfänglichen F&E-Phase beginnen die Hersteller nun damit, ihre Produkte fertigungsgerecht zu gestalten. Das bedeutet, dass die Produkte für die Produktion präziser gestaltet werden können, was zu kürzeren Vorlaufzeiten, engeren Toleranzen und fortschrittlicheren Spezifikationen und Prototypen führt. Mit Hilfe von CAD- oder Modellierungsplattformen geht die Arbeit heute viel schneller vonstatten, und dies kann auch als Werkzeug für die strategische Designentwicklung sowie als Marketinginstrument dienen. ⓘ
Die Nichteinhaltung von Kostenzielen führt zu erheblichen Verlusten für ein Unternehmen. Darüber hinaus ist die Forschung und Entwicklung neuer Geräte angesichts des globalen Wettbewerbs nicht nur eine Notwendigkeit, sondern ein Muss für Hersteller von Medizinprodukten. Die Verwirklichung eines neuen Designs kann sehr kostspielig sein, vor allem angesichts des kürzeren Produktlebenszyklus. Im Zuge des technologischen Fortschritts steigt das Niveau von Qualität, Sicherheit und Zuverlässigkeit mit der Zeit exponentiell an. ⓘ
Bei den ersten Modellen des künstlichen Herzschrittmachers handelte es sich beispielsweise um externe Unterstützungsgeräte, die über Elektrodenkabel auf der Brust Stromimpulse an die Herzmuskulatur weiterleiten. Die Elektroden berührten das Herz direkt über den Brustkorb, so dass die Stimulationsimpulse durch den Körper geleitet wurden. Bei den Empfängern dieser Geräte kam es in der Regel zu einer Infektion an den Elektrodeneingängen, was zur Erprobung des ersten internen Herzschrittmachers führte, bei dem die Elektroden durch eine Thorakotomie am Herzmuskel befestigt wurden. Spätere Entwicklungen führten zu einer Isotopen-Energiequelle, die ein Leben lang halten sollte. ⓘ
Software
Mobile medizinische Anwendungen
Mit der zunehmenden Nutzung von Smartphones im medizinischen Bereich erließ die FDA 2013 eine Richtlinie zur Regulierung mobiler medizinischer Anwendungen und zum Schutz der Nutzer vor deren unbeabsichtigter Nutzung, der bald auch europäische und andere Regulierungsbehörden folgten. Diese Leitlinien unterscheiden die Apps, die der Regulierung unterliegen, anhand der Marketingaussagen der Apps. Die Einbeziehung der Leitlinien während der Entwicklungsphase solcher Apps kann als Entwicklung eines Medizinprodukts betrachtet werden; die Vorschriften müssen angepasst werden und Vorschläge für eine beschleunigte Genehmigung können aufgrund der Art der "Versionen" der Entwicklung mobiler Anwendungen erforderlich sein. ⓘ
Am 25. September 2013 veröffentlichte die FDA den Entwurf eines Leitfadens für die Regulierung mobiler medizinischer Anwendungen, um klarzustellen, welche Art von mobilen Apps im Zusammenhang mit der Gesundheit nicht reguliert werden und welche schon. ⓘ
Cybersecurity
Medizinische Geräte wie Herzschrittmacher, Insulinpumpen, OP-Monitore, Defibrillatoren und chirurgische Instrumente, einschließlich Tiefenhirnstimulatoren, können die Fähigkeit besitzen, lebenswichtige Gesundheitsinformationen aus dem Körper eines Patienten an medizinisches Fachpersonal zu übertragen. Einige dieser Geräte können aus der Ferne gesteuert werden. Dies hat zu Besorgnis über Datenschutz- und Sicherheitsfragen, menschliches Versagen und technische Pannen bei dieser Technologie geführt. Zwar gibt es nur wenige Studien, die sich mit der Anfälligkeit medizinischer Geräte für Hackerangriffe befasst haben, aber es besteht ein Risiko. Im Jahr 2008 wiesen Informatiker nach, dass Herzschrittmacher und Defibrillatoren drahtlos über Funkhardware, eine Antenne und einen Personalcomputer gehackt werden können. Diese Forscher zeigten, dass sie einen kombinierten Herzdefibrillator und -schrittmacher abschalten und so umprogrammieren konnten, dass er potenziell tödliche Schocks abgibt oder seine Batterie leer ist. Jay Radcliff, ein Sicherheitsforscher, der sich für die Sicherheit medizinischer Geräte interessiert, äußerte Bedenken hinsichtlich der Sicherheit dieser Geräte. Er teilte seine Bedenken auf der Sicherheitskonferenz Black Hat mit. Radcliff befürchtet, dass die Geräte verwundbar sind und hat festgestellt, dass ein tödlicher Angriff auf Insulinpumpen und Blutzuckermessgeräte möglich ist. Einige Hersteller medizinischer Geräte spielen die Bedrohung durch solche Angriffe herunter und argumentieren, dass die nachgewiesenen Angriffe von erfahrenen Sicherheitsforschern durchgeführt wurden und in der realen Welt wohl kaum vorkommen werden. Gleichzeitig haben andere Hersteller Software-Sicherheitsexperten gebeten, die Sicherheit ihrer Geräte zu untersuchen. Erst im Juni 2011 hatten Sicherheitsexperten gezeigt, dass ein Wissenschaftler mit leicht erhältlicher Hardware und einem Benutzerhandbuch sowohl die Daten des Systems einer drahtlosen Insulinpumpe als auch eines Blutzuckermessgeräts abgreifen kann. Mit der PIN des Geräts konnte der Wissenschaftler die Dosierung des Insulins drahtlos steuern. Anand Raghunathan, einer der Forscher in dieser Studie, erklärt, dass medizinische Geräte immer kleiner und leichter werden, so dass sie leicht getragen werden können. Der Nachteil ist, dass zusätzliche Sicherheitsfunktionen die Batterie und die Größe zusätzlich belasten und die Preise in die Höhe treiben würden. Dr. William Maisel stellte einige Überlegungen zu den Beweggründen für diese Aktivitäten an. Die Motivation für das Hacken könnte die Beschaffung privater Informationen zur Erzielung finanzieller Gewinne oder Wettbewerbsvorteile, die Schädigung des Rufs eines Geräteherstellers, Sabotage, die Absicht, finanziellen oder persönlichen Schaden anzurichten, oder einfach nur die Befriedigung des Angreifers sein. Die Forscher schlagen einige Sicherheitsvorkehrungen vor. Eine davon wäre die Verwendung von Rolling Codes. Eine andere Lösung ist die sogenannte "körpergekoppelte Kommunikation", bei der die menschliche Haut als Wellenleiter für die drahtlose Kommunikation genutzt wird. Am 28. Dezember 2016 veröffentlichte die US-amerikanische Gesundheitsbehörde FDA (Food and Drug Administration) ihre Empfehlungen, die rechtlich nicht durchsetzbar sind, wie Hersteller von Medizinprodukten die Sicherheit von mit dem Internet verbundenen Geräten gewährleisten sollten. ⓘ
Ähnlich wie Gefahren können auch Bedrohungen und Schwachstellen der Cybersicherheit nicht beseitigt werden, sondern müssen verwaltet und auf ein vernünftiges Maß reduziert werden. Bei der Entwicklung von Medizinprodukten sollte der Grad des Cybersicherheitsrisikos bereits in einem frühen Stadium des Prozesses bestimmt werden, um einen Ansatz für das Management von Cybersicherheitsschwachstellen (einschließlich einer Reihe von Designkontrollen für die Cybersicherheit) zu entwickeln. Der Ansatz für die Konzeption von Medizinprodukten sollte mit dem NIST Cybersecurity Framework für das Management von Cybersicherheitsrisiken übereinstimmen. ⓘ
Im August 2013 hat die FDA mehr als 20 Vorschriften zur Verbesserung der Sicherheit von Daten in Medizinprodukten erlassen, um auf die wachsenden Risiken einer begrenzten Cybersicherheit zu reagieren. ⓘ
Künstliche Intelligenz
Die Zahl der zugelassenen Medizinprodukte, die künstliche Intelligenz oder maschinelles Lernen (AI/ML) nutzen, nimmt zu. Im Jahr 2020 gab es mehrere hundert KI/ML-Medizinprodukte, die von der US-amerikanischen FDA zugelassen oder in Europa mit dem CE-Zeichen versehen waren. Die meisten KI/ML-Geräte konzentrieren sich auf die Radiologie. Bis 2020 gab es weder in den USA noch in Europa einen spezifischen Regulierungspfad für KI/ML-basierte Medizinprodukte. Im Januar 2021 veröffentlichte die FDA jedoch einen Vorschlag für einen Rechtsrahmen für KI/ML-basierte Software, und die EU-Verordnung über Medizinprodukte, die im Mai 2021 die EU-Richtlinie über Medizinprodukte ablöst, definiert regulatorische Anforderungen für Medizinprodukte, einschließlich KI/ML-Software. ⓘ
Medizinische Geräte
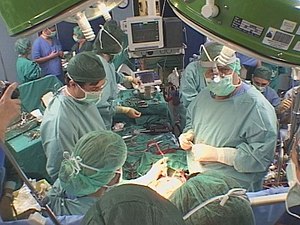
Medizinische Geräte (auch Armamentarium genannt) sollen bei der Diagnose, Überwachung oder Behandlung von Krankheiten helfen. ⓘ
Arten
Es gibt mehrere Grundtypen:
- Zu den diagnostischen Geräten gehören medizinische Bildgebungsgeräte, die zur Unterstützung der Diagnose eingesetzt werden. Beispiele sind Ultraschall- und MRT-Geräte, PET- und CT-Scanner sowie Röntgengeräte.
- Zu den Behandlungsgeräten gehören Infusionspumpen, medizinische Laser und LASIK-Chirurgiegeräte.
- Lebenserhaltende Geräte werden zur Aufrechterhaltung der Körperfunktionen eines Patienten eingesetzt. Dazu gehören medizinische Beatmungsgeräte, Inkubatoren, Anästhesiegeräte, Herz-Lungen-Maschinen, ECMO- und Dialysegeräte.
- Medizinische Monitore ermöglichen es dem medizinischen Personal, den Gesundheitszustand eines Patienten zu messen. Die Monitore können die Vitalparameter des Patienten und andere Parameter wie EKG, EEG und Blutdruck messen.
- Medizinische Laborgeräte automatisieren oder unterstützen die Analyse von Blut, Urin, Genen und gelösten Gasen im Blut.
- Medizinische Diagnosegeräte können für bestimmte Zwecke auch zu Hause eingesetzt werden, z. B. zur Kontrolle von Diabetes mellitus.
- Therapeutische Geräte: Geräte für die physikalische Therapie, z. B. Geräte für die kontinuierliche passive Bewegung (CPM) ⓘ
Die Identifizierung von Medizinprodukten wurde in jüngster Zeit durch die Einführung der eindeutigen Gerätekennzeichnung (Unique Device Identification, UDI) und die standardisierte Benennung mit Hilfe der Globalen Nomenklatur für Medizinprodukte (Global Medical Device Nomenclature, GMDN) verbessert, die vom International Medical Device Regulatory Forum (IMDRF) gebilligt wurde. ⓘ
Ein Biomedizintechniker (BMET) ist ein wichtiger Bestandteil des Gesundheitssystems. Sie sind vor allem in Krankenhäusern beschäftigt und für die Wartung der medizinischen Geräte einer Einrichtung zuständig. BMET fungieren hauptsächlich als Schnittstelle zwischen Arzt und Gerät. ⓘ
Spende medizinischer Geräte
Die Verfügbarkeit von medizinischer Ausrüstung ist aus Sicht der globalen Gesundheit ein Problem, da Länder mit geringen Ressourcen nicht in der Lage sind, lebenswichtige und lebensrettende Ausrüstung zu beschaffen oder zu bezahlen. Eine häufig angewandte Strategie zur Lösung dieses Problems sind gut gemeinte Gerätespenden von Einzelpersonen, Organisationen, Herstellern und Wohltätigkeitsorganisationen aus ressourcenreichen Ländern an ressourcenarme Länder. Probleme mit der Wartung, der Verfügbarkeit von Technikern für biomedizinische Geräte (BMET), den Versorgungsketten, der Benutzerschulung und der Angemessenheit der Spenden bedeuten jedoch, dass diese häufig nicht den beabsichtigten Nutzen bringen. Die WHO schätzt, dass 95 % der medizinischen Ausrüstung in Ländern mit niedrigem und mittlerem Einkommen (LMIC) importiert und 80 % davon von internationalen Gebern oder ausländischen Regierungen finanziert werden. Während bis zu 70 % der medizinischen Ausrüstung in den afrikanischen Ländern südlich der Sahara gespendet wird, werden nur 10 % bis 30 % der gespendeten Ausrüstung auch eingesetzt. Eine Überprüfung der derzeitigen Praxis und der Leitlinien für die Spende von medizinischem Gerät für die chirurgische und anästhesiologische Versorgung in LMICs hat gezeigt, dass der Spendenprozess sehr komplex ist und zahlreiche Mängel aufweist. Erforderlich sind eine bessere Zusammenarbeit und Planung zwischen Spendern und Empfängern, die Evaluierung von Spendenprogrammen und eine konzertierte Aktion zur Aufklärung von Spendern und Empfängern über die bestehenden Richtlinien und Maßnahmen für Gerätespenden. ⓘ
Akademische Ressourcen
- Zeitschrift Medical & Biological Engineering & Computing
- Zeitschrift Expert Review of Medical Devices
- Zeitschrift für klinische Technik ⓘ
Forschungsinstitute für Verpackungen an Universitäten
- Universität von Minnesota - Zentrum für Medizinprodukte (MDC)
- Universität Strathclyde - Strathclyde-Institut für Medizinprodukte (SIMD)
- Flinders University - Forschungsinstitut für medizinische Geräte (MDRI)
- Michigan State University - Schule für Verpackung (SoP)
- IIT Bombay - Biomedizinische Technik und Technologie (Inkubationszentrum) (BETiC) ⓘ
Gesetzliche Definition
In Deutschland regelte das Gesetz über Medizinprodukte (Medizinproduktegesetz – MPG) vom 2. August 1994 bis zum 26. Mai 2021 den Verkehr mit Medizinprodukten. Es diente der nationalen Umsetzung von drei europäischen (Stamm-)Richtlinien (Richtlinie 90/385/EWG [aktive implantierbare medizinische Geräte], Richtlinie 93/42/EWG [sonstige Medizinprodukte] und Richtlinie 98/79/EG [In-vitro-Diagnostika]), die durch spätere Änderungsrichtlinien ergänzt bzw. geändert wurden, zuletzt mit Richtlinie 2007/47/EG vom 5. September 2007 zum 21. März 2010. Das MPG und seine acht ausführenden Rechtsverordnungen enthalten darüber hinaus weitere nationale Regelungen, die hauptsächlich der Überwachung im Markt befindlicher Medizinprodukte (Marktüberwachung) dienen. ⓘ
§ 3 MPG enthielt in Nr. 1 bis 4 die Legaldefinition/en des Begriffs Medizinprodukt. ⓘ
Seit dem 26. Mai 2021 wurde das Medizinproduktegesetz durch das Medizinprodukterecht-Durchführungsgesetz (MPDG) abgelöst, das der Umsetzung der europäischen Medizinprodukteverordnung (Medical Device Regulation, MDR) dient. ⓘ
Einteilung
Aktive, nicht-aktive und implantierbare Medizinprodukte
Nach Anhang VIII der EU-Verordnung 745/2017 werden Medizinprodukte in aktive, nicht-aktive und Medizinprodukte mit Messfunktion eingeteilt:
- Aktive Medizinprodukte sind mit Hilfe einer externen Energiequelle (Strom, Akku, Batterie, thermische oder kinetische Energie oder Gasdruck) betriebene Geräte.
- Nicht-aktive Medizinprodukte sind „passiv“, wirken durch Schwerkraft oder werden mit Muskelkraft betrieben.
- Medizinprodukte mit Messfunktion können aktiv oder nicht-aktiv-sein; einige davon müssen regelmäßig messtechnisch kontrolliert werden. ⓘ
Ein implantierbares Medizinprodukt kann aktiv sein; beispielsweise ein implantierbarer Defibrillator, da er eine Batterie enthält und durch einen medizinischen Eingriff in den menschlichen Körper eingebracht wird, um nach dem Eingriff dort zu verbleiben. Für aktive implantierbare Medizinprodukte gelten besondere Richtlinien. Beispiele für nicht-aktive implantierbare Medizinprodukte sind Endoprothesen oder Portkatheter. Ein Blutzuckermessgerät ist ein aktives Medizinprodukt mit Messfunktion und gleichzeitig ein In-vitro-Diagnostikum. ⓘ
Medizinprodukte der Anlagen 1, 2 und 3
Nach § 10 der Medizinprodukte-Betreiberverordnung (MPBetreibV) gelten in Deutschland für bestimmte nichtimplantierbare aktive Medizinprodukte, Säuglingsinkubatoren sowie externe aktive Komponenten aktiver Implantate laut Anlage 1 besondere Auflagen, zum Beispiel bezüglich regelmäßiger sicherheitstechnischer Kontrollen und dokumentierter Einweisung in die Gerätebedienung. Entscheidend ist die vom Hersteller festgelegte Zweckbestimmung, ob das Medizinprodukt unter eine der Gruppen der Anlage 1 zur MPBetreibV fällt. Ähnliches gilt für Medizinprodukte der Anlage 2, die messtechnischen Kontrollen unterliegen. Für Anlage-1- und Anlage-2-Produkte ist ein Medizinproduktebuch zu führen. ⓘ
Zur Anlage 3 zählen alle aktiven implantierbaren sowie ausgewählte nicht-aktive implantierbare Medizinprodukte (Herzklappen, nicht resorbierbare Gefäßprothesen und -stützen, Gelenkersatz für Hüfte oder Knie, Wirbelkörperersatzsysteme und Bandscheibenprothesen und Brustimplantate). ⓘ
Ausnahmen gelten für automatische externe Defibrillatoren, die sich an öffentlich zugänglichen Orten befinden und für die Anwendung durch Laien vorgesehen sind (§ 11 der Medizinprodukte-Betreiberverordnung). ⓘ
| Medizinprodukt | aktiv | Anlage 1 | Anlage 2 | Anlage 3 | Sicherheitstechnische Kontrolle | Bestandsverzeichnis | Medizinproduktebuch |
|---|---|---|---|---|---|---|---|
| Absaugpumpe | x | nach Herstellervorgabe | x | ||||
| mechanisches Blutdruckmessgerät mit Aneroidmanometer | x | ||||||
| elektronisches Blutdruckmessgerät | x | x | nach Herstellervorgabe | x | x | ||
| Ernährungspumpe | x | x | x | ||||
| Implantierbarer Kardioverter-Defibrillator | x | x | |||||
| Infusionssystem | |||||||
| Knieprothese | x | ||||||
| Überwachungsmonitor | x | x | x | x | x | x | |
| Spritzenpumpe | x | x | x | x | x |
Einteilung zur Aufbereitung
Die Medizinprodukte-Betreiberverordnung verlangt eine ordnungsgemäße Aufbereitung. Dafür wurde von der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO), dem Robert Koch-Institut (RKI) und dem Bundesinstitutes für Arzneimittel und Medizinprodukte (BfArM) eine gemeinsame Empfehlung herausgegeben. Danach werden wiederverwendbare Geräte und Instrumente in unkritische, semikritische und kritische Medizinprodukte eingeteilt. Entscheidend für die Einteilung ist die bestimmungsgemäße Anwendung des jeweiligen Produkts. ⓘ
Kommt das Produkt nur mit intakter Haut in Berührung, gilt es als unkritisch, oft ist nur eine Reinigung oder Desinfektion nötig. Semikritische Produkte berühren Schleimhaut oder krankhaft veränderte Haut, bei der Aufbereitung muss deshalb immer gereinigt und desinfiziert (Semikritisch A), in einigen Fällen zusätzlich unmittelbar nach der Anwendung nicht fixierend vorgereinigt, dann möglichst maschinell gereinigt und desinfiziert beziehungsweise sterilisiert werden (Semikritisch B). Dagegen müssen kritische Medizinprodukte, die die Haut beziehungsweise Schleimhaut durchdringen, immer sterilisiert werden. Je nachdem ob Hohlräume oder schwer zugängliche Teile vorhanden sind, die Aufbereitung die Funktion und Sicherheit des Medizinproduktes beeinflusst oder die Anzahl der Aufbereitungszyklen begrenzt ist, wird das kritische Medizinprodukt den Aufbereitungsstufen A, B oder C mit den entsprechenden Verfahren zugeordnet. ⓘ
Gesetzliche Regelungen
Medizinprodukte-Verwaltungsvorschrift
Die Bundesregierung hat am 24. Mai 2012 die Allgemeine Verwaltungsvorschrift zur Durchführung des Medizinproduktegesetzes (Medizinprodukte-Durchführungsvorschrift – MPGVwV) erlassen, die am 1. Januar 2013 in Kraft trat. ⓘ
Die Verwaltungsvorschrift ist an die Bundesländer gerichtet und dient behördenintern der Vereinheitlichung der Marktüberwachung von Medizinprodukten in Deutschland. Neue Koordinierungsstelle der Länder ist die Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten (ZLG) mit Sitz in Bonn. ⓘ
Die Behörden führen nunmehr vermehrt unangemeldete Audits bei Herstellern und Betreibern durch und prüfen, ob die Voraussetzungen für das Inverkehrbringen und die Inbetriebnahme der Medizinprodukte (weiter) gegeben sind. § 1 Absatz 1 Satz 2 MPGVwV verpflichtet die Länder auch zur Überwachung der Einhaltung der Vorgaben des Heilmittelwerbegesetzes (HWG). ⓘ
Technische Dokumentation für Medizinprodukte
An die Dokumentation eines Medizinprodukts bestehen durch Gesetze und im Rahmen des Qualitätsmanagements besondere Anforderungen. ⓘ
Marktzahlen in der EU einschließlich Schweiz und Norwegen
Das Marktvolumen der Medizinprodukte in der EU einschließlich Schweiz und Norwegen wird für 2009 mit 95 Milliarden Euro abgeschätzt. Davon fließen ca. 4 Milliarden Euro in die Entwicklung neuer Medizinprodukte. Etwa 575.000 Arbeitsplätze sind in der Medizinprodukteindustrie befasst. Ungefähr 25.000 Unternehmen zählen zur Medizinprodukteindustrie, davon fast 95 % klein- und mittelständische Unternehmen. Die Gesamtbilanz für den Handel mit Medizinprodukten ist positiv, 2012 lag sie bei 15,5 Milliarden Euro, was einen Zuwachs um mehr als das Doppelte seit 2006 bedeutet. Die Zahl der erfolgreichen Patentierungen im Bereich der Medizinprodukte übertrifft mit 10.412 im Jahr 2012 nach Angaben des europäischen Patentamtes (EPA) alle anderen technischen Bereiche. Weltweit liegt Deutschland hinter den USA bei Medizinprodukteinnovationen an zweiter Stelle. ⓘ
Zulassung der Medizinprodukte in EU und USA
Marktzugangsverfahren in den USA
„Premarket Approval“ (PMA)
Geräte, die ein potenziell hohes Risiko für den Patienten mit sich bringen (Klasse III), unterliegen einer behördlichen Zulassung, nämlich dem „Premarket Approval“ (PMA). In diesem Verfahren müssen die (grundsätzlich für alle Produktklassen nachzuweisende) Sicherheit als auch die Wirksamkeit durch klinische Studien nachgewiesen werden. Dieses Verfahren erfolgt jedoch nur bei rund 1 Prozent aller Produkte. ⓘ
Gewährleistung der Verpackungs-, Transport- und Lagerstabilität von Medizinprodukten
Aspekte wie das richtige Verpacken, Transportieren und Lagern beeinflussen die Qualität von Medizinprodukten. ⓘ
Transportstabilität
Während des Transports darf das Medizinprodukt nicht beschädigt werden. Wenn eine Gefahr für Kontamination besteht, sollen die Medizinprodukte in einer Schutzverpackung transportiert werden. Die Schutzverpackung dient dem Schutz während dem Transport und der Lagerung. Wenn die Schutzverpackung geöffnet wird, muss diese nach der Entnahme sofort wieder verschlossen werden. Bevor die Schutzverpackung geöffnet wird, sollte darauf geachtet werden, dass die Verpackung staubfrei ist. ⓘ
Lagerstabilität
Die Lagerstabilität von Medizinprodukten ist von Kriterien wie z. B. äußere Einflüsse, Art der Lagerung, Art des Transports und Inhalt der Verpackung abhängig. Diese Bedingungen müssen in Bezug auf die zu lagernden Produkte geprüft werden. Die zulässige Lagerdauer ergibt sich in der Regel aus den Herstellerangaben oder wird von Hygieneverantwortlichen schriftlich festgelegt. Zu bedenken ist, dass die angegebene Lagerdauer nur bei sach- und fachgerechter Lagerung gültig ist. ⓘ
Medizinprodukte müssen trocken und staubarm gelagert und vor
- direkter Sonneneinstrahlung und UV-Strahlung
- Beschädigung
- mechanischen und chemischen Einflüssen
- Temperaturschwankungen (maximal 20 K/Tag)
- Ungeziefer
geschützt werden. Durch die vorgeschriebene Lagerdauer soll das Risiko einer Kontamination beim Transport und Öffnen minimiert werden. ⓘ

