Cheyne-Stokes-Atmung
| Cheyne-Stokes-Atmung ⓘ | |
|---|---|

| |
| Diagramm mit Cheyne-Stokes-Atmung (unten) und anderen pathologischen Atemmustern | |
| Aussprache |
|
Die Cheyne-Stokes-Atmung ist ein anormales Atemmuster, das durch eine zunehmend tiefere und manchmal schnellere Atmung gekennzeichnet ist, gefolgt von einer allmählichen Abnahme, die zu einem vorübergehenden Atemstillstand führt, der Apnoe genannt wird. Das Muster wiederholt sich, wobei jeder Zyklus normalerweise 30 Sekunden bis 2 Minuten dauert. Es handelt sich um eine Oszillation der Ventilation zwischen Apnoe und Hyperpnoe mit einem Crescendo-Diminuendo-Muster, die mit wechselnden Serumpartialdrücken von Sauerstoff und Kohlendioxid einhergeht. ⓘ
Die Cheyne-Stokes-Atmung und die periodische Atmung sind die beiden Bereiche auf einem Spektrum von Schweregraden des oszillierenden Tidalvolumens. Der Unterschied liegt darin, was am Tiefpunkt der Ventilation beobachtet wird: Bei der Cheyne-Stokes-Atmung handelt es sich um Apnoe (da Apnoe ein wichtiges Merkmal in der ursprünglichen Beschreibung ist), bei der periodischen Atmung um Hypopnoe (abnorm kleine, aber nicht fehlende Atemzüge). ⓘ
Diese Phänomene können sowohl im Wachzustand als auch im Schlaf auftreten, wo sie als zentrales Schlafapnoe-Syndrom (CSAS) bezeichnet werden. ⓘ
Es kann durch eine Schädigung des Atmungszentrums oder durch physiologische Anomalien bei kongestiver Herzinsuffizienz verursacht werden und tritt auch bei Neugeborenen mit unreifen Atmungsorganen und bei Besuchern auf, die sich in großen Höhen befinden. Ein Beispiel ist das Atemmuster beim Joubert-Syndrom und verwandten Erkrankungen. ⓘ
Bei der Cheyne-Stokes-Atmung – benannt nach John Cheyne (1777–1836) und William Stokes (1804–1878) – handelt es sich um eine pathologische Atmungsform. Sie ist durch ein periodisches An- und Abschwellen der Atemtiefe und des Abstands der einzelnen Atemzüge voneinander charakterisiert. An die flachsten Atemzüge schließt sich oft ein kürzerer Atemstillstand an, dann setzen wieder Atemzüge ein, die sich zunehmend vertiefen. ⓘ
Pathophysiologie
Zu den Ursachen können Herzversagen, Nierenversagen, Narkosevergiftungen und erhöhter Hirndruck gehören. Die Pathophysiologie der Cheyne-Stokes-Atmung lässt sich wie folgt zusammenfassen: Apnoe führt zu einer erhöhten CO2-Konzentration, die eine übermäßige kompensatorische Hyperventilation verursacht, die wiederum zu einer CO2-Absenkung führt, die wiederum eine Apnoe verursacht, wodurch der Zyklus erneut beginnt. ⓘ
Bei einer Herzinsuffizienz ist der Mechanismus der Oszillation eine instabile Rückkopplung im Atmungskontrollsystem. Bei einer normalen Atmungskontrolle ermöglicht die negative Rückkopplung die Aufrechterhaltung eines stabilen Niveaus der alveolären Gaskonzentrationen und damit stabile Gewebespiegel von Sauerstoff und Kohlendioxid (CO2). Im Steady-State entspricht die CO2-Produktionsrate der Nettorate, mit der CO2 aus dem Körper ausgeatmet wird, was (unter der Annahme, dass die Umgebungsluft kein CO2 enthält) das Produkt aus alveolärer Ventilation und endtidaler CO2-Konzentration ist. Aufgrund dieser Wechselbeziehung bildet die Menge der möglichen stationären Zustände eine Hyperbel:
- Alveolare Ventilation = körpereigene CO2-Produktion/endtidaler CO2-Anteil. ⓘ
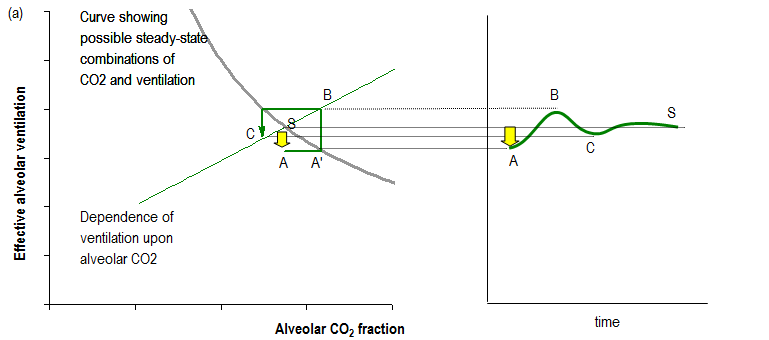
In der Abbildung unten ist diese Beziehung die Kurve, die von links oben nach rechts unten verläuft. Nur bei Positionen entlang dieser Kurve kann die CO2-Produktion des Körpers durch die Ausatmung von CO2 genau kompensiert werden. In der Zwischenzeit gibt es eine weitere Kurve, die in der Abbildung der Einfachheit halber als gerade Linie von links unten nach rechts oben dargestellt ist und die die ventilatorische Reaktion des Körpers auf unterschiedliche CO2-Konzentrationen darstellt. Dort, wo sich die Kurven kreuzen, befindet sich der potenzielle stationäre Zustand (S). ⓘ
Durch Atemkontrollreflexe führt jeder kleine vorübergehende Abfall der Ventilation (A) zu einem entsprechenden kleinen Anstieg (A') der alveolären CO2-Konzentration, der vom Atemkontrollsystem wahrgenommen wird, so dass es zu einem anschließenden kleinen kompensatorischen Anstieg der Ventilation (B) über den Steady-State-Wert (S) kommt, der dazu beiträgt, den CO2-Wert wieder auf seinen Steady-State-Wert zu bringen. Im Allgemeinen können vorübergehende oder anhaltende Störungen der Ventilation, des CO2- oder des Sauerstoffgehalts durch das Atemkontrollsystem auf diese Weise ausgeglichen werden. ⓘ
In einigen pathologischen Zuständen ist die Rückkopplung jedoch stärker als nötig, um das System einfach wieder in den Gleichgewichtszustand zu bringen. Stattdessen kommt es zu einem Überschwingen der Ventilation, das eine der ursprünglichen Störung entgegengesetzte Störung erzeugen kann. Wenn diese sekundäre Störung größer ist als die ursprüngliche, wird die nächste Reaktion noch größer sein, und so weiter, bis sich sehr große Schwingungen entwickelt haben, wie in der Abbildung unten dargestellt. ⓘ
Der Zyklus der Vergrößerung der Störungen erreicht eine Grenze, wenn die aufeinanderfolgenden Störungen nicht mehr größer werden, was eintritt, wenn die physiologischen Reaktionen nicht mehr linear zur Größe des Reizes zunehmen. Das offensichtlichste Beispiel hierfür ist, wenn die Ventilation auf Null sinkt: Sie kann nicht mehr tiefer werden. So kann die Cheyne-Stokes-Atmung über einen Zeitraum von vielen Minuten oder Stunden mit einem sich wiederholenden Muster von Apnoen und Hyperpnoen aufrechterhalten werden. ⓘ
Das Ende der linearen Abnahme der Ventilation als Reaktion auf den Rückgang des CO2 liegt jedoch nicht bei der Apnoe. Sie tritt ein, wenn die Ventilation so gering ist, dass die eingeatmete Luft nie den Alveolarraum erreicht, weil das inspirierte Tidalvolumen nicht größer ist als das Volumen der großen Atemwege wie der Luftröhre. Folglich kann die Ventilation des Alveolarraums am Tiefpunkt der periodischen Atmung praktisch gleich Null sein; das leicht zu beobachtende Gegenstück dazu ist, dass die endtidalen Gaskonzentrationen zu diesem Zeitpunkt nicht den realistischen Alveolarkonzentrationen entsprechen. ⓘ
Durch klinische Beobachtung wurden viele potenziell beitragende Faktoren ermittelt, die jedoch leider alle miteinander verknüpft sind und in hohem Maße variieren. Weithin anerkannte Risikofaktoren sind Hyperventilation, verlängerte Kreislaufzeit und verminderte Blutgaspufferkapazität. ⓘ
Sie sind physiologisch miteinander verknüpft, da (bei einem bestimmten Patienten) die Kreislaufzeit mit steigendem Herzzeitvolumen abnimmt. Ebenso ist bei einer gegebenen CO2-Produktionsrate des Gesamtkörpers die alveoläre Ventilation umgekehrt proportional zur endtidalen CO2-Konzentration (da ihr gemeinsames Produkt der CO2-Produktionsrate des Gesamtkörpers entsprechen muss). Die Chemoreflex-Sensitivität ist eng mit der Lage des Steady-State verbunden, denn wenn die Chemoreflex-Sensitivität zunimmt (bei ansonsten gleichen Bedingungen), steigt die Steady-State-Ventilation und sinkt das Steady-State-CO2. Da die Ventilation und das CO2 leicht zu beobachten sind und es sich dabei um häufig gemessene klinische Variablen handelt, für deren Beobachtung kein besonderes Experiment durchgeführt werden muss, wird in der Literatur eher über Anomalien dieser Variablen berichtet. Andere Variablen, wie z. B. die Chemoreflex-Sensitivität, können jedoch nur durch ein spezielles Experiment gemessen werden, so dass Anomalien bei diesen Variablen nicht in klinischen Routinedaten zu finden sind. Wird bei Patienten mit Cheyne-Stokes-Atmung die hyperkapnische Beatmungsempfindlichkeit gemessen, kann sie um 100 % oder mehr erhöht sein. Wenn sie nicht gemessen wird, können ihre Folgen - wie ein niedriger mittlerer PaCO2-Wert und eine erhöhte mittlere Ventilation - manchmal als wichtigstes Merkmal erscheinen. ⓘ
Ursächlich ist eine nichtlineare Sensitivität des Atemzentrums auf den CO2-Partialdruck im arteriellen Blut. Da der ansteigende CO2-Partialdruck im arteriellen Blut als stärkster Atemreiz wirkt, steigen Atemzugtiefe und Atemfrequenz, bis ein niedriger CO2-Gehalt im Blut wieder zu verringerter Atmung und Pausen führt. Der CO₂-Partialdruck beginnt dann wieder anzusteigen, bis der Zyklus von vorn beginnt. Da die Empfindlichkeit auf CO2 bei niedrigen Partialdrücken überproportional geringer und bei hohen Partialdrücken überproportional hoch ist, kommt es zu einem „Schwingen des Atemreglers“. ⓘ
Ein negativer Einfluss der Cheyne-Stokes-Atmung auf den klinischen Verlauf der Herzinsuffizienz wird diskutiert. Je ausgeprägter die Herzinsuffizienz – und dabei vor allem die linksventrikuläre Komponente – umso ausgeprägter können zentrale und periodische Atemmuster sein. ⓘ
Begleitende Bedingungen
Dieses abnorme Atmungsmuster, bei dem die Atmung zeitweise ausbleibt und dann wieder schneller wird, kann bei Patienten mit Herzinsuffizienz, Schlaganfall, Hyponatriämie, traumatischen Hirnverletzungen und Hirntumoren auftreten. In einigen Fällen kann sie auch bei ansonsten gesunden Menschen während des Schlafs in großer Höhe auftreten. Sie kann bei allen Formen der toxischen metabolischen Enzephalopathie auftreten. Sie ist ein Symptom der Kohlenmonoxidvergiftung, zusammen mit Synkope oder Koma. Diese Art der Atmung unterscheidet sich von der Atemdepression, die häufig nach der Verabreichung von Morphin auftritt. ⓘ
Hospize dokumentieren manchmal das Vorhandensein der Cheyne-Stokes-Atmung, wenn sich ein Patient dem Tod nähert, und berichten, dass Patienten, die nach solchen Episoden noch sprechen können, keine mit der Atmung verbundenen Ängste äußern, obwohl dies für die Angehörigen manchmal beunruhigend ist. ⓘ
Verwandte Muster
Die Cheyne-Stokes-Atmung ist nicht dasselbe wie die Biot-Atmung ("Cluster-Atmung"), bei der Gruppen von Atemzügen in der Regel ähnlich groß sind. ⓘ
Sie unterscheiden sich von der Kussmaul-Atmung dadurch, dass das Kussmaul-Muster eine gleichmäßige, sehr tiefe Atmung mit normaler oder erhöhter Frequenz ist. ⓘ
Geschichte
Die Erkrankung wurde nach den Ärzten John Cheyne und William Stokes benannt, die sie im 19. Jahrhundert erstmals beschrieben. ⓘ
Der Begriff wurde in der Sowjetunion nach dem Tod von Joseph Stalin im Jahr 1953 weithin bekannt und verwendet, weil die sowjetische Presse verkündete, dass der kranke Stalin an Cheyne-Stokes-Atmung litt. ⓘ
Therapie
Zur Behandlung der Cheyne-Stokes-Atmung kommen als Beatmungsverfahren die antizyklisch modulierte Ventilation (AZMV) bzw. die adaptive Servoventilation (ASV) zur Geltung, welche das früher eingesetzte BiPAP-Verfahren (für bilevel positive airway pressure) abgelöst haben. Dabei wird über ein Maskensystem von Atemzug zu Atemzug eine automatische Regulation des Atemdrucks eingesetzt und das Schwingen der Atemregulation mechanisch gedämpft. Diese Verfahren haben gegenüber der klassischen CPAP-Beatmung verschiedene Vorteile: Sie gleichen Atemschwankungen aufgrund der Cheyne-Stokes-Atmung antizyklisch aus und modulieren die pathophysiologischen Atemmuster in die physiologische Richtung. ⓘ
Seit der Veröffentlichung erster Ergebnisse der SERVE-HF-Studie, sollte die ASV aufgrund erhöhter Mortalität bei Herzinsuffizienzpatienten mit eingeschränkter linksventrikulärer Ejektionsfraktion allerdings nicht mehr verwendet werden. ⓘ
In einzelnen Fällen führt eine Gabe von zusätzlichem Sauerstoff (2–4 l/min) zu einer Linearisierung der Atemantwortkurve und somit zu einer medikamentösen Dämpfung der schwingenden Atemregulation. ⓘ
Im Fall der akuten Höhenkrankheit muss ein sofortiger Abstieg bis zur Besserung aller Beschwerden erfolgen. Dieses ist notwendig, um wieder ausreichende Sauerstoffzufuhr zu gewährleisten. ⓘ