Epoxide
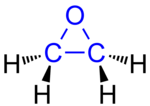
Die Epoxide, auch Epoxyde, nach dem Hantzsch-Widman-System Oxirane oder nach der Austauschnomenklatur Oxacyclopropane, sind eine chemische Stoffgruppe sehr reaktionsfähiger, cyclischer, organischer Verbindungen. Sie enthalten einen Dreiring, bei dem im Vergleich zum Cyclopropan eine Methylengruppe durch ein Sauerstoffatom ersetzt ist. Epoxidgruppen bilden somit die einfachsten sauerstoffhaltigen Heterocyclen. Die Sauerstoffbrücke wird als Epoxybrücke bezeichnet. ⓘ

Ein Epoxid ist ein zyklischer Ether mit einem dreiatomigen Ring. Dieser Ring hat die Form eines gleichseitigen Dreiecks und ist daher sehr reaktionsfreudig, und zwar stärker als andere Ether. Sie werden in großem Maßstab für zahlreiche Anwendungen hergestellt. Im Allgemeinen sind Epoxide mit niedrigem Molekulargewicht farblos, unpolar und oft flüchtig. ⓘ
Nomenklatur
Eine Verbindung, die die funktionelle Gruppe Epoxid enthält, kann als Epoxid, Epoxyd, Oxiran und Ethoxyline bezeichnet werden. Einfache Epoxide werden häufig auch als Oxide bezeichnet. So ist das Epoxid von Ethylen (C2H4) Ethylenoxid (C2H4O). Viele Verbindungen haben Trivialnamen; so wird Ethylenoxid zum Beispiel "Oxiran" genannt. Einige Namen betonen das Vorhandensein der funktionellen Epoxidgruppe, wie bei der Verbindung 1,2-Epoxyheptan, die auch als 1,2-Heptenoxid bezeichnet werden kann. ⓘ
Ein Polymer, das aus Epoxidvorstufen gebildet wird, wird als Epoxid bezeichnet, aber solche Materialien enthalten keine Epoxidgruppen (oder nur wenige restliche Epoxidgruppen, die bei der Bildung des Harzes nicht umgesetzt werden). ⓘ
Synthese
Die vorherrschenden Epoxide in der Industrie sind Ethylenoxid und Propylenoxid, die in einer Größenordnung von etwa 15 bzw. 3 Millionen Tonnen/Jahr hergestellt werden. ⓘ
Heterogen katalysierte Oxidation von Alkenen
Bei der Epoxidierung von Ethylen kommt es zu einer Reaktion mit Sauerstoff. Nach einem 1974 vorgeschlagenen Reaktionsmechanismus wird mindestens ein Ethylenmolekül für sechs zu Ethylenoxid umgewandelte Moleküle vollständig oxidiert:
- 7 H2C=CH2 + 6 O2 → 6 C2H4O + 2 CO2 + 2 H2O ⓘ
Die direkte Reaktion von Sauerstoff mit Alkenen ist nur für dieses Epoxid nützlich. In der Regel werden modifizierte heterogene Silberkatalysatoren verwendet. Andere Alkene reagieren nicht brauchbar, sogar Propylen, obwohl TS-1-geträgerte Au-Katalysatoren eine selektive Epoxidierung von Propylen durchführen können. ⓘ
Olefin-(Alken-)Oxidation mit organischen Peroxiden und Metallkatalysatoren
Abgesehen von Ethylenoxid werden die meisten Epoxide durch Behandlung von Alkenen mit peroxidhaltigen Reagenzien erzeugt, die ein einzelnes Sauerstoffatom abgeben. Diese Reaktionen sind mit Sicherheitsbedenken behaftet, da organische Peroxide zu spontaner Zersetzung oder sogar Verbrennung neigen. ⓘ
Metallkomplexe sind nützliche Katalysatoren für Epoxidierungen mit Wasserstoffperoxid und Alkylhydroperoxiden. Die eher elektrophilen Peroxycarbonsäuren wandeln Alkene ohne den Einsatz von Metallkatalysatoren in Epoxide um. In speziellen Anwendungen werden auch andere peroxidhaltige Reagenzien wie Dimethyldioxiran eingesetzt. Je nach Reaktionsmechanismus und Geometrie des Alken-Ausgangsmaterials können cis- und/oder trans-Epoxiddiastereomere gebildet werden. Sind im Ausgangsmaterial weitere Stereozentren vorhanden, können diese die Stereochemie der Epoxidierung beeinflussen. Metallkatalysierte Epoxidierungen wurden zunächst mit tert-Butylhydroperoxid (TBHP) erforscht. Durch die Assoziation von TBHP mit dem Metall (M) entsteht der aktive Metall-Peroxy-Komplex, der die MOOR-Gruppe enthält, die dann ein O-Zentrum auf das Alken überträgt.
 Vereinfachter Mechanismus für die metallkatalysierte Epoxidierung von Alkenen mit Peroxid (ROOH)-Reagenzien ⓘ
Vereinfachter Mechanismus für die metallkatalysierte Epoxidierung von Alkenen mit Peroxid (ROOH)-Reagenzien ⓘ
Organische Peroxide werden für die Herstellung von Propylenoxid aus Propylen verwendet. Auch hierfür werden Katalysatoren benötigt. Als Sauerstoffquellen können sowohl t-Butylhydroperoxid als auch Ethylbenzolhydroperoxid verwendet werden. ⓘ
Olefinperoxidation mit Peroxycarbonsäuren
In der Regel wird im Laborbetrieb die Prilezhaev-Reaktion eingesetzt. Bei diesem Ansatz wird das Alken mit einer Peroxysäure wie m-CPBA oxidiert. Ein Beispiel hierfür ist die Epoxidierung von Styrol mit Perbenzoesäure zu Styroloxid:
Die Reaktion läuft über den so genannten "Schmetterlingsmechanismus" ab. Das Peroxid wird als elektrophil und das Alken als nukleophil betrachtet. Die Reaktion wird als konzertiert angesehen (die Zahlen im unten stehenden Mechanismus dienen der Vereinfachung). Der Schmetterlingsmechanismus ermöglicht eine ideale Positionierung des O-O-Sigma-Sternorbitals für den Angriff der C-C-Pi-Elektronen. Da zwei Bindungen zum Epoxidsauerstoff gebrochen und gebildet werden, ist dies formal ein Beispiel für einen Coarctat-Übergangszustand.
Hydroperoxide werden auch bei katalytischen enantioselektiven Epoxidierungen wie der Sharpless-Epoxidierung und der Jacobsen-Epoxidierung eingesetzt. Zusammen mit der Shi-Epoxidierung eignen sich diese Reaktionen für die enantioselektive Synthese von chiralen Epoxiden. Oxaziridin-Reagenzien können auch zur Erzeugung von Epoxiden aus Alkenen verwendet werden. ⓘ
Homogen katalysierte asymmetrische Epoxidierungen
Arenoxide sind Zwischenprodukte bei der Oxidation von Arenen durch Cytochrom P450. Bei prochiralen Arenen (Naphthalin, Toluol, Benzoate, Benzopyren) werden die Epoxide oft mit hoher Enantioselektivität erhalten. ⓘ
Chirale Epoxide lassen sich oft enantioselektiv aus prochiralen Alkenen ableiten. Viele Metallkomplexe liefern aktive Katalysatoren, aber die wichtigsten sind Titan, Vanadium und Molybdän.
 Die Sharpless-Epoxidierung ⓘ
Die Sharpless-Epoxidierung ⓘ
Die Sharpless-Epoxidierungsreaktion ist eine der wichtigsten enantioselektiven chemischen Reaktionen. Sie wird zur Herstellung von 2,3-Epoxyalkoholen aus primären und sekundären Allylalkoholen verwendet. ⓘ

Intramolekulare SN2-Substitution
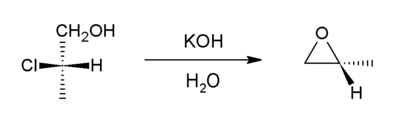
Bei dieser Methode wird eine Dehydrohalogenierung durchgeführt. Es handelt sich um eine Variante der Williamson-Ethersynthese. In diesem Fall verdrängt ein Alkoxidion intramolekular das Chlorid. Die Vorläuferverbindungen werden als Halohydrine bezeichnet und können durch Halohydratisierung eines Alkens erzeugt werden. Ausgehend von Propylenchlorhydrin entsteht auf diesem Weg der größte Teil des weltweiten Angebots an Propylenoxid. ⓘ
Eine intramolekulare Epoxidbildungsreaktion ist einer der Schlüsselschritte bei der Darzens-Reaktion. ⓘ
Bei der Johnson-Corey-Chaykovsky-Reaktion werden Epoxide aus Carbonylgruppen und Sulfoniumyliden gebildet. Bei dieser Reaktion ist ein Sulfonium die Abgangsgruppe anstelle des Chlorids. ⓘ
Nucleophile Epoxidierung
Olefine mit Elektronenmangel, wie Enone und Acrylderivate, können mit nukleophilen Sauerstoffverbindungen wie Peroxiden epoxidiert werden. Die Reaktion läuft in zwei Schritten ab. Zunächst führt der Sauerstoff eine nukleophile konjugierte Addition durch, wobei ein stabilisiertes Carbanion entsteht. Dieses Carbanion greift dann dasselbe Sauerstoffatom an und verdrängt eine Abgangsgruppe von ihm, um den Epoxidring zu schließen. ⓘ
Biosynthese
Epoxide sind in der Natur nicht häufig anzutreffen. Sie entstehen in der Regel durch Oxygenierung von Alkenen durch Cytochrom P450 (siehe aber auch die kurzlebigen Epoxyeicosatriensäuren, die als Signalmoleküle fungieren, und die ähnlichen Epoxydocosapentaensäuren und Epoxyeicosatetraensäuren). ⓘ
Reaktionen
Ringöffnungsreaktionen dominieren die Reaktivität von Epoxiden. ⓘ
Hydrolyse und Addition von Nukleophilen
Epoxide reagieren mit einer breiten Palette von Nukleophilen, z. B. Alkoholen, Wasser, Aminen, Thiolen und sogar Halogeniden. Mit zwei oft nahezu gleichwertigen Angriffsstellen sind Epoxide Beispiele für "zweizähnige Substrate". Die Regioselektivität von Ringöffnungsreaktionen unsymmetrischer Epoxide hängt von den Bedingungen ab. Diese Klasse von Reaktionen ist die Grundlage von Epoxidklebern und der Herstellung von Glykolen. ⓘ
Polymerisation und Oligomerisierung
Die Polymerisation von Epoxiden führt zu Polyethern. Zum Beispiel polymerisiert Ethylenoxid zu Polyethylenglykol, auch bekannt als Polyethylenoxid. Die Reaktion eines Alkohols oder eines Phenols mit Ethylenoxid, die Ethoxylierung, wird häufig zur Herstellung von Tensiden verwendet:
- ROH + n C2H4O → R(OC2H4)nOH ⓘ
Mit Anhydriden werden aus Epoxiden Polyester hergestellt. ⓘ
Desoxygenierung
Epoxide können mit oxophilen Reagenzien desoxydiert werden. Diese Reaktion kann unter Verlust oder Beibehaltung der Konfiguration ablaufen. Die Kombination von Wolframhexachlorid und n-Butyllithium ergibt das Alken. ⓘ
Andere Reaktionen
- Die Reduktion eines Epoxids mit Lithiumaluminiumhydrid oder Aluminiumhydrid ergibt den entsprechenden Alkohol. Diese Reduktion erfolgt durch nucleophile Addition von Hydrid (H-).
- Die reduktive Spaltung von Epoxiden ergibt β-Lithioalkoxide.
- Durch Reduktion mit Wolframhexachlorid und n-Butyllithium entsteht das Alken
- Epoxide unterliegen Ringerweiterungsreaktionen, die durch den Einbau von Kohlendioxid zu cyclischen Carbonaten veranschaulicht werden.
- Bei der Behandlung mit Thioharnstoff wandeln sich die Epoxide in Episulfide um, die als Thiirane bezeichnet werden. ⓘ
Verwendungen
Benzoloxid liegt im Gleichgewicht mit dem Oxepin-Isomer vor. ⓘ
Ethylenoxid wird häufig zur Herstellung von Detergenzien und Tensiden durch Ethoxylierung verwendet. Bei seiner Hydrolyse entsteht Ethylenglykol. Es wird auch für die Sterilisation von medizinischen Instrumenten und Materialien verwendet. ⓘ
Die Reaktion von Epoxiden mit Aminen ist die Grundlage für die Bildung von Epoxidklebstoffen und Strukturmaterialien. Ein typischer Aminhärter ist Triethylentetramin (TETA). ⓘ
Sicherheit
Epoxide sind Alkylierungsmittel, was viele von ihnen hochgiftig macht. ⓘ
Vertreter
Das einfachste und technisch interessanteste Epoxid ist Ethylenoxid (Ethenoxid). Es wird durch Oxidation von Ethen an einem Silberkatalysator hergestellt (Heterogene Katalyse). Aufgrund der in einem Dreiring herrschenden Ringspannung von ca. 115 kJ/mol kann der Ring durch nucleophilen Angriff auf ein C-Atom relativ leicht geöffnet werden. Das Sauerstoffatom des Epoxidrings ist dabei zwar die Abgangsgruppe, bleibt aber mit einem C-Atom des Epoxids verbunden und ist somit weiterhin Bestandteil des Moleküls. ⓘ
Ist eines oder sind mehrere Wasserstoffatome des Ethylenoxids durch Organyl-Reste (Alkyl-Reste, Aryl-Reste, Alkylaryl-Reste etc.) ersetzt, sind diese Verbindungen ebenfalls Oxirane. ⓘ
Ein Polymer aus mehreren Epoxid-Segmenten ist ein Polyepoxid, auch Epoxidharz. Diese werden als Klebstoff oder in Kompositwerkstoffen verwendet. ⓘ
Epoxide sind Zwischenprodukte bei der Herstellung des Grippe-Medikaments Oseltamivir (Tamiflu) aus in Japanischem Sternanis enthaltener Shikimisäure. ⓘ
Einige Epoxidharze (z. B. Bisphenol-A-diglycidylether und -F) sind hochgradige Allergene, was vor allem Arbeitskräfte betrifft, die in der Fertigung direkt exponiert sind (z. B. bei der Herstellung von Flugzeugen oder modernen Windkraftanlagen). ⓘ
Bildung durch Epoxidierung einer Doppelbindung
Epoxide können bei Raumtemperatur durch die Reaktion eines Alkens und einer Peroxycarbonsäure gebildet werden (Prileschajew-Reaktion). Neben dem Epoxid entsteht eine Carbonsäure. ⓘ
 Bildung eines Epoxides aus einer Peroxycarbonsäure und einem Alken ⓘ
Bildung eines Epoxides aus einer Peroxycarbonsäure und einem Alken ⓘ
Häufig wird als Peroxycarbonsäure meta-Chlorperbenzoesäure (MCPBA) eingesetzt, da diese im Gegensatz zu anderen Percarbonsäuren relativ stabil und sicher handhabbar ist. Andere Peroxycarbonsäuren, die zur Epoxidierung eingesetzt werden können, sind Peroxyameisensäure und Peroxyessigsäure. Sie werden während der Reaktion aus Ameisensäure bzw. Essigsäure und Wasserstoffperoxid hergestellt (In-situ-Verfahren). ⓘ