Joule-Thomson-Effekt
In der Thermodynamik beschreibt der Joule-Thomson-Effekt (auch Joule-Kelvin-Effekt oder Kelvin-Joule-Effekt genannt) die Temperaturänderung eines realen Gases oder einer Flüssigkeit (im Unterschied zu einem idealen Gas), wenn es durch ein Ventil oder einen porösen Stopfen gepresst wird, während es isoliert bleibt, so dass kein Wärmeaustausch mit der Umgebung stattfindet. Dieses Verfahren wird als Drosselungsprozess oder Joule-Thomson-Prozess bezeichnet. Bei Raumtemperatur kühlen sich alle Gase außer Wasserstoff, Helium und Neon bei der Ausdehnung durch den Joule-Thomson-Prozess ab, wenn sie durch eine Öffnung gedrosselt werden; bei diesen drei Gasen tritt der gleiche Effekt auf, allerdings nur bei niedrigeren Temperaturen. Die meisten Flüssigkeiten, wie z. B. Hydrauliköle, werden durch den Joule-Thomson-Drosselungsprozess erwärmt. ⓘ
Der Drosselungsprozess bei der Gaskühlung wird üblicherweise bei Kühlprozessen wie Verflüssigern genutzt. In der Hydraulik kann der Erwärmungseffekt der Joule-Thomson-Drosselung genutzt werden, um intern undichte Ventile zu finden, da diese Wärme erzeugen, die mit einem Thermoelement oder einer Wärmebildkamera nachgewiesen werden kann. Die Drosselung ist ein grundsätzlich irreversibler Prozess. Die Drosselung aufgrund des Strömungswiderstands in Versorgungsleitungen, Wärmetauschern, Regeneratoren und anderen Komponenten von (thermischen) Maschinen ist eine Verlustquelle, die deren Leistung einschränkt. ⓘ

Beispiele von Auftreten und Anwendungen:
- Abkühlung von Sodawasser, Schlagsahne und Softeis beim Ausschäumen aus einer Druckflasche
- Gefrieren von Wasser in Beschneiungsanlagen, sogenannten Schneekanonen. Insbesondere bei Druckluftkanonen und Schneelanzen.
- Herstellung von Trockeneis beim Zahnarzt oder beim Trockeneisstrahlen (siehe Sandstrahlen)
- Gasverflüssigung im Linde-Verfahren ⓘ
Geschichte
Der Effekt ist nach James Prescott Joule und William Thomson, 1. Baron Kelvin, benannt, die ihn 1852 entdeckten. Er knüpfte an frühere Arbeiten von Joule über die Joule-Ausdehnung an, bei der sich ein Gas im Vakuum frei ausdehnt und die Temperatur unverändert bleibt, wenn das Gas ideal ist. ⓘ
Beschreibung
Die adiabatische (ohne Wärmeaustausch) Ausdehnung eines Gases kann auf verschiedene Weise erfolgen. Die Temperaturänderung, die das Gas während der Expansion erfährt, hängt nicht nur vom Anfangs- und Enddruck ab, sondern auch von der Art und Weise, in der die Expansion durchgeführt wird. ⓘ
- Ist der Expansionsprozess reversibel, d. h. befindet sich das Gas zu jedem Zeitpunkt im thermodynamischen Gleichgewicht, spricht man von einer isentropen Expansion. In diesem Fall verrichtet das Gas während der Expansion positive Arbeit, und seine Temperatur sinkt.
- Bei einer freien Ausdehnung hingegen verrichtet das Gas keine Arbeit und nimmt keine Wärme auf, so dass die innere Energie erhalten bleibt. Bei einer solchen Ausdehnung würde die Temperatur eines idealen Gases konstant bleiben, aber die Temperatur eines realen Gases sinkt, außer bei sehr hohen Temperaturen.
- Die in diesem Artikel besprochene Expansionsmethode, bei der ein Gas oder eine Flüssigkeit mit einem Druck P1 in einen Bereich mit niedrigerem Druck P2 strömt, ohne dass sich die kinetische Energie wesentlich ändert, wird als Joule-Thomson-Expansion bezeichnet. Diese Expansion ist von Natur aus irreversibel. Während dieser Ausdehnung bleibt die Enthalpie unverändert (siehe Beweis unten). Im Gegensatz zu einer freien Ausdehnung wird Arbeit verrichtet, was zu einer Änderung der inneren Energie führt. Ob die innere Energie zunimmt oder abnimmt, hängt davon ab, ob Arbeit an oder durch das Fluid verrichtet wird; dies wird durch den Anfangs- und Endzustand der Expansion und die Eigenschaften des Fluids bestimmt. ⓘ
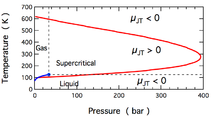
Die Temperaturänderung, die während einer Joule-Thomson-Expansion auftritt, wird durch den Joule-Thomson-Koeffizienten quantifiziert, . Dieser Koeffizient kann entweder positiv (Abkühlung) oder negativ (Erwärmung) sein; die Bereiche, in denen dies bei molekularem Stickstoff, N2, der Fall ist, sind in der Abbildung dargestellt. Beachten Sie, dass die meisten Bedingungen in der Abbildung dem überkritischen Zustand von N2 entsprechen, bei dem es einige Eigenschaften eines Gases und einige einer Flüssigkeit hat, aber nicht wirklich als eines von beiden beschrieben werden kann. Der Koeffizient ist sowohl bei sehr hohen als auch bei sehr niedrigen Temperaturen negativ; bei sehr hohem Druck ist er bei allen Temperaturen negativ. Die maximale Inversionstemperatur (621 K für N2) tritt auf, wenn sich der Druck dem Nullpunkt nähert. Für N2-Gas bei niedrigen Drücken, ist bei hohen Temperaturen negativ und bei niedrigen Temperaturen positiv. Bei Temperaturen unterhalb der Koexistenzkurve Gas-Flüssigkeit kondensiert N2 zu einer Flüssigkeit und der Koeffizient wird wieder negativ. Bei N2-Gas unterhalb von 621 K kann also eine Joule-Thomson-Expansion zur Abkühlung des Gases genutzt werden, bis sich flüssiges N2 bildet. ⓘ
Physikalischer Mechanismus
Es gibt zwei Faktoren, die die Temperatur einer Flüssigkeit während einer adiabatischen Ausdehnung ändern können: eine Änderung der inneren Energie oder die Umwandlung zwischen potenzieller und kinetischer innerer Energie. Die Temperatur ist das Maß für die thermische kinetische Energie (Energie, die mit der Molekularbewegung verbunden ist); eine Temperaturänderung bedeutet also eine Änderung der thermischen kinetischen Energie. Die innere Energie ist die Summe der thermischen kinetischen Energie und der thermischen potenziellen Energie. Selbst wenn sich die innere Energie nicht ändert, kann sich also die Temperatur aufgrund der Umwandlung von kinetischer und potenzieller Energie ändern; dies geschieht bei einer freien Ausdehnung und führt in der Regel zu einem Temperaturrückgang, wenn sich die Flüssigkeit ausdehnt. Wenn während der Ausdehnung Arbeit an oder durch die Flüssigkeit verrichtet wird, ändert sich die gesamte innere Energie. Dies geschieht bei einer Joule-Thomson-Ausdehnung und kann zu einer stärkeren Erwärmung oder Abkühlung führen als bei einer freien Ausdehnung. ⓘ
Bei einer Joule-Thomson-Ausdehnung bleibt die Enthalpie konstant. Die Enthalpie, ist definiert als
wobei die innere Energie ist, der Druck und das Volumen ist. Unter den Bedingungen einer Joule-Thomson-Expansion stellt die Änderung von die von der Flüssigkeit geleistete Arbeit (siehe Beweis unten). Wenn zunimmt, wobei konstant, dann abnehmen, da das Fluid Arbeit an seiner Umgebung verrichtet. Dies führt zu einer Abnahme der Temperatur und zu einem positiven Joule-Thomson-Koeffizienten. Umgekehrt bedeutet eine Abnahme von bedeutet umgekehrt, dass das Fluid Arbeit verrichtet und die innere Energie zunimmt. Wenn die Zunahme der kinetischen Energie die Zunahme der potenziellen Energie übersteigt, steigt die Temperatur des Fluids an und der Joule-Thomson-Koeffizient ist negativ. ⓘ
Für ein ideales Gas, während einer Joule-Thomson-Expansion nicht verändert. Folglich gibt es keine Änderung der inneren Energie; da es auch keine Änderung der thermischen potentiellen Energie gibt, kann es auch keine Änderung der thermischen kinetischen Energie und somit keine Temperaturänderung geben. In realen Gasen, ändert sich. ⓘ
Das Verhältnis des Wertes von zu dem Wert, der für ein ideales Gas bei derselben Temperatur erwartet wird, wird als Kompressibilitätsfaktor bezeichnet, . Für ein Gas ist dieser Wert bei niedriger Temperatur in der Regel kleiner als 1 und bei hoher Temperatur größer als 1 (siehe die Diskussion unter Kompressibilitätsfaktor). Bei niedrigem Druck bewegt sich der Wert von immer gegen Eins, wenn sich ein Gas ausdehnt. Daher gilt bei niedriger Temperatur, und mit der Ausdehnung des Gases an, was zu einem positiven Joule-Thomson-Koeffizienten führt. Bei hoher Temperatur, und bei der Ausdehnung des Gases ab; wenn die Abnahme groß genug ist, wird der Joule-Thomson-Koeffizient negativ sein. ⓘ
Bei Flüssigkeiten und überkritischen Fluiden unter hohem Druck, mit zunehmendem Druck an. Dies ist darauf zurückzuführen, dass die Moleküle zusammengedrängt werden, so dass das Volumen aufgrund des höheren Drucks kaum abnehmen kann. Unter solchen Bedingungen ist der Joule-Thomson-Koeffizient negativ, wie in der obigen Abbildung zu sehen ist. ⓘ
Der mit dem Joule-Thomson-Effekt verbundene physikalische Mechanismus ist eng mit dem einer Stoßwelle verwandt, obwohl sich eine Stoßwelle dadurch unterscheidet, dass die Änderung der kinetischen Massenenergie des Gasstroms nicht vernachlässigbar ist. ⓘ
Der Joule-Thomson-Koeffizient (Kelvin)

Die Änderungsrate der Temperatur in Abhängigkeit vom Druck bei einem Joule-Thomson-Prozess (d. h. bei konstanter Enthalpie ) ist der Joule-Thomson-Koeffizient (Kelvin-Koeffizient) . Dieser Koeffizient kann durch das Volumen des Gases ausgedrückt werden , seiner Wärmekapazität bei konstantem Druck und dem Wärmeausdehnungskoeffizienten ausgedrückt werden:
Siehe § Ableitung des Joule-Thomson-Koeffizienten unten für den Beweis dieser Beziehung. Der Wert von wird in der Regel in °C/bar (SI-Einheiten: K/Pa) angegeben und hängt von der Art des Gases sowie von der Temperatur und dem Druck des Gases vor der Expansion ab. Die Druckabhängigkeit beträgt in der Regel nur einige Prozent für Drücke bis 100 bar. ⓘ
Alle realen Gase haben einen Inversionspunkt, an dem der Wert von das Vorzeichen wechselt. Die Temperatur dieses Punktes, die Joule-Thomson-Inversionstemperatur, hängt von dem Druck des Gases vor der Expansion ab. ⓘ
Bei einer Gasexpansion sinkt der Druck, so dass das Vorzeichen von per Definition negativ ist. In der folgenden Tabelle wird daher erläutert, wann der Joule-Thomson-Effekt ein reales Gas abkühlt oder erwärmt:
| Wenn die Temperatur des Gases | dann ist | da ist | also sein muss | also das Gas ⓘ |
|---|---|---|---|---|
| unterhalb der Inversionstemperatur | positiv | immer negativ | negativ | kühlt |
| oberhalb der Inversions-Temperatur | negativ | positiv | wärmt |
Helium und Wasserstoff sind zwei Gase, deren Joule-Thomson-Inversionstemperaturen bei einem Druck von einer Atmosphäre sehr niedrig sind (z. B. etwa 45 K, -228 °C für Helium). Daher erwärmen sich Helium und Wasserstoff, wenn sie bei konstanter Enthalpie bei typischen Raumtemperaturen expandieren. Stickstoff und Sauerstoff, die beiden häufigsten Gase in der Luft, haben dagegen Inversionstemperaturen von 621 K (348 °C) bzw. 764 K (491 °C): Diese Gase können durch den Joule-Thomson-Effekt von Raumtemperatur abgekühlt werden. ⓘ
Für ein ideales Gas, ist immer gleich Null: Ideale Gase erwärmen sich weder noch kühlen sie sich ab, wenn sie bei konstanter Enthalpie expandieren. ⓘ
Anwendungen
In der Praxis wird der Joule-Thomson-Effekt dadurch erreicht, dass man das Gas durch eine Drosselvorrichtung (in der Regel ein Ventil) expandieren lässt, die sehr gut isoliert sein muss, um jegliche Wärmeübertragung auf das oder vom Gas zu verhindern. Während der Expansion wird dem Gas keine externe Arbeit entzogen (das Gas darf z. B. nicht durch eine Turbine expandiert werden). ⓘ
Die bei der Joule-Thomson-Expansion erzeugte Kühlung macht sie zu einem wertvollen Werkzeug in der Kältetechnik. Der Effekt wird in der Linde-Technik als Standardverfahren in der petrochemischen Industrie eingesetzt, wo der Kühleffekt zur Verflüssigung von Gasen genutzt wird, und auch in vielen kryogenen Anwendungen (z. B. zur Herstellung von flüssigem Sauerstoff, Stickstoff und Argon). Ein Gas muss unterhalb seiner Inversionstemperatur liegen, um durch den Linde-Zyklus verflüssigt zu werden. Aus diesem Grund können einfache Linde-Zyklus-Verflüssiger, die bei Umgebungstemperatur arbeiten, nicht zur Verflüssigung von Helium, Wasserstoff oder Neon eingesetzt werden. Der Joule-Thomson-Effekt kann jedoch auch zur Verflüssigung von Helium genutzt werden, sofern das Heliumgas zunächst unter seine Inversionstemperatur von 40 K abgekühlt wird. ⓘ
Nachweis, dass die spezifische Enthalpie konstant bleibt
In der Thermodynamik sind sogenannte "spezifische" Größen Größen pro Masseneinheit (kg) und werden mit Kleinbuchstaben bezeichnet. So sind h, u und v die spezifische Enthalpie, die spezifische innere Energie bzw. das spezifische Volumen (Volumen pro Masseneinheit bzw. reziproke Dichte). Bei einem Joule-Thomson-Prozess bleibt die spezifische Enthalpie h konstant. Um dies zu beweisen, muss zunächst die Nettoarbeit berechnet werden, die geleistet wird, wenn sich eine Masse m des Gases durch den Stopfen bewegt. Diese Gasmenge hat im Bereich des Drucks P1 (Bereich 1) ein Volumen von V1 = m v1 und im Bereich des Drucks P2 (Bereich 2) ein Volumen von V2 = m v2. Im Bereich 1 beträgt die "Strömungsarbeit", die der Rest des Gases an der Gasmenge verrichtet, dann: W1 = m P1v1. Im Bereich 2 beträgt die von der Gasmenge auf den Rest des Gases ausgeübte Arbeit: W2 = m P2v2. Die gesamte an der Gasmasse m geleistete Arbeit ist also
Die Änderung der inneren Energie abzüglich der gesamten an der Gasmenge geleisteten Arbeit ist nach dem ersten Hauptsatz der Thermodynamik die gesamte der Gasmenge zugeführte Wärme.
Beim Joule-Thomson-Prozess ist das Gas isoliert, so dass keine Wärme absorbiert wird. Dies bedeutet, dass
wobei u1 und u2 die spezifischen inneren Energien des Gases in den Bereichen 1 bzw. 2 bezeichnen. Unter Verwendung der Definition der spezifischen Enthalpie h = u + Pv bedeutet die obige Gleichung, dass
wobei h1 und h2 die spezifischen Enthalpien der Gasmenge in den Regionen 1 bzw. 2 bezeichnen. ⓘ
Drosselung im T-s-Diagramm

Eine sehr bequeme Möglichkeit, den Drosselungsprozess quantitativ zu verstehen, ist die Verwendung von Diagrammen wie h-T-Diagrammen, h-P-Diagrammen und anderen. Am häufigsten werden die sogenannten T-s-Diagramme verwendet. Abbildung 2 zeigt das T-s-Diagramm von Stickstoff als Beispiel. Verschiedene Punkte sind wie folgt angegeben:
- T = 300 K, p = 200 bar, s = 5,16 kJ/(kgK), h = 430 kJ/kg;
- T = 270 K, p = 1 bar, s = 6,79 kJ/(kgK), h = 430 kJ/kg;
- T = 133 K, p = 200 bar, s = 3,75 kJ/(kgK), h = 150 kJ/kg;
- T = 77,2 K, p = 1 bar, s = 4,40 kJ/(kgK), h = 150 kJ/kg; T = 77,2 K, p = 1 bar, s = 4,40 kJ/(kgK), h = 150 kJ/kg;
- T = 77,2 K, p = 1 bar, s = 2,83 kJ/(kgK), h = 28 kJ/kg (gesättigte Flüssigkeit bei 1 bar);
- T = 77,2 K, p = 1 bar, s = 5,41 kJ/(kgK), h = 230 kJ/kg (gesättigtes Gas bei 1 bar). ⓘ
Wie bereits gezeigt, hält die Drosselung h konstant. Z.B. folgt die Drosselung von 200 bar und 300 K (Punkt a in Abb. 2) der Isenthalpielinie (Linie der konstanten spezifischen Enthalpie) von 430 kJ/kg. Bei 1 bar ergibt sich Punkt b mit einer Temperatur von 270 K. Eine Drosselung von 200 bar auf 1 bar führt also zu einer Abkühlung von Raumtemperatur auf unter den Gefrierpunkt von Wasser. Eine Drosselung von 200 bar und einer Anfangstemperatur von 133 K (Punkt c in Abb. 2) auf 1 bar führt zu Punkt d, der sich im Zweiphasenbereich des Stickstoffs bei einer Temperatur von 77,2 K befindet. Da die Enthalpie eine extensive Größe ist, ist die Enthalpie in d (hd) gleich der Enthalpie in e (he) multipliziert mit dem Massenanteil der Flüssigkeit in d (xd) plus der Enthalpie in f (hf) multipliziert mit dem Massenanteil des Gases in d (1 - xd). Also
Mit Zahlen: 150 = xd 28 + (1 - xd) 230. xd ist also etwa 0,40. Das bedeutet, dass der Massenanteil der Flüssigkeit im Flüssigkeits-Gas-Gemisch, das das Drosselventil verlässt, 40 % beträgt. ⓘ
Herleitung des Joule-Thomson-Koeffizienten
Es ist schwierig, sich physikalisch vorzustellen, was der Joule-Thomson-Koeffizient bedeutet, darstellt. Außerdem wird bei modernen Bestimmungen von nicht nach der ursprünglichen Methode von Joule und Thomson, sondern messen eine andere, eng verwandte Größe. Daher ist es nützlich, die Beziehungen zwischen und anderen, einfacher zu messenden Größen abzuleiten, wie im Folgenden beschrieben. ⓘ
Der erste Schritt, um diese Ergebnisse zu erhalten, besteht darin, festzustellen, dass der Joule-Thomson-Koeffizient die drei Variablen T, P und H umfasst. Ein nützliches Ergebnis erhält man sofort, wenn man die zyklische Regel anwendet; in Bezug auf diese drei Variablen kann diese Regel wie folgt geschrieben werden
Jede der drei partiellen Ableitungen in diesem Ausdruck hat eine spezifische Bedeutung. Die erste ist , die zweite ist die Wärmekapazität bei konstantem Druck, , definiert durch
und die dritte ist der Kehrwert des isothermen Joule-Thomson-Koeffizienten, , definiert durch
- .
Diese letzte Größe lässt sich leichter messen als . Der Ausdruck der zyklischen Regel lautet also
Diese Gleichung kann verwendet werden, um aus dem einfacher zu messenden isothermen Joule-Thomson-Koeffizienten Joule-Thomson-Koeffizienten zu erhalten. Sie wird im Folgenden verwendet, um einen mathematischen Ausdruck für den Joule-Thomson-Koeffizienten in Bezug auf die volumetrischen Eigenschaften einer Flüssigkeit zu erhalten. ⓘ
Ausgangspunkt ist die Grundgleichung der Thermodynamik in Bezug auf die Enthalpie; diese lautet
Wenn man nun durch dP "dividiert" und die Temperatur konstant hält, erhält man
Die partielle Ableitung auf der linken Seite ist der isotherme Joule-Thomson-Koeffizient, und die Ableitung auf der rechten Seite kann durch den Wärmeausdehnungskoeffizienten über eine Maxwell-Beziehung ausgedrückt werden. Die entsprechende Beziehung lautet
wobei α der kubische Wärmeausdehnungskoeffizient ist. Ersetzt man diese beiden partiellen Ableitungen, so erhält man
Dieser Ausdruck kann nun Folgendes ersetzen in der früheren Gleichung für ersetzen, um zu erhalten:
Dies liefert einen Ausdruck für den Joule-Thomson-Koeffizienten in Form der allgemein verfügbaren Eigenschaften Wärmekapazität, molares Volumen und Wärmeausdehnungskoeffizient. Er zeigt, dass die Joule-Thomson-Inversionstemperatur, bei der Null ist, auftritt, wenn der Wärmeausdehnungskoeffizient gleich dem Kehrwert der Temperatur ist. Da dies für ideale Gase bei allen Temperaturen gilt (siehe Ausdehnung in Gasen), ist der Joule-Thomson-Koeffizient eines idealen Gases bei allen Temperaturen gleich Null. ⓘ
Das zweite Joule'sche Gesetz
Für ein ideales Gas, das durch geeignete mikroskopische Postulate definiert ist, lässt sich leicht nachweisen, dass αT = 1 ist, so dass die Temperaturänderung eines solchen idealen Gases bei einer Joule-Thomson-Ausdehnung gleich Null ist. Für ein solches ideales Gas impliziert dieses theoretische Ergebnis, dass:
- Die innere Energie einer festen Masse eines idealen Gases hängt nur von seiner Temperatur ab (nicht von Druck oder Volumen). ⓘ
Diese Regel wurde ursprünglich von Joule experimentell für reale Gase gefunden und ist als zweites Joule'sches Gesetz bekannt. In verfeinerten Experimenten wurden erhebliche Abweichungen von diesem Gesetz festgestellt. ⓘ






























