Dampfreformierung
Dampfreformierung oder Dampf-Methan-Reformierung (SMR) ist ein Verfahren zur Herstellung von Synthesegas (Wasserstoff und Kohlenmonoxid) durch Reaktion von Kohlenwasserstoffen mit Wasser. In der Regel wird Erdgas als Ausgangsstoff verwendet. Der Hauptzweck dieser Technologie ist die Erzeugung von Wasserstoff. Die Reaktion wird durch dieses Gleichgewicht dargestellt:
- Fehler beim Parsen (Syntaxfehler): {\displaystyle \ce{CH4 + H2O <=> CO + 3 H2 <span title="Aus: Englische Wikipedia, Einführungsabschnitt" class="plainlinks">[https://en.wikipedia.org/wiki/Steam_reforming <span style="color:#dddddd">ⓘ</span>]</span>}}
Die Reaktion ist stark endotherm (ΔHSR = 206 kJ/mol). ⓘ
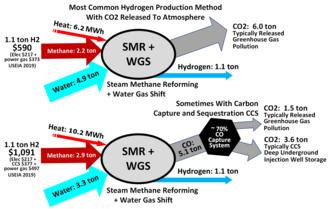
Der durch Dampfreformierung erzeugte Wasserstoff wird als "grauer Wasserstoff" bezeichnet, wenn das überschüssige Kohlendioxid in die Atmosphäre entlassen wird, und als "blauer Wasserstoff", wenn das Kohlendioxid (größtenteils) abgeschieden und geologisch gespeichert wird - siehe Kohlenstoffabscheidung und -speicherung. Kohlenstofffreier "grüner" Wasserstoff wird durch thermochemische Wasserspaltung unter Verwendung von Solarthermie, kohlenstoffarmer oder -freier Elektrizität oder Abwärme oder durch Elektrolyse mit kohlenstoffarmer oder -freier Elektrizität erzeugt. Türkisfarbener" Wasserstoff ohne Kohlenstoffemissionen wird durch einstufige Methanpyrolyse von Erdgas hergestellt). ⓘ
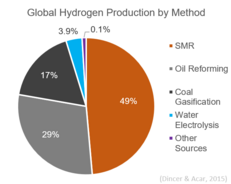
Durch Dampfreformierung von Erdgas wird der größte Teil des weltweit produzierten Wasserstoffs erzeugt. Wasserstoff wird in der industriellen Synthese von Ammoniak und anderen Chemikalien verwendet. ⓘ

1) Zufuhr von Methan, 2) Zufuhr von Wasser, 3) Primärreformer, 4) Zufuhr von Luft, 5) Sekundärreformer, 6) Katalysator, 7) Kompressor, 8) Wäscher ⓘ
Reaktionen
Die Dampfreformierung ist ein allothermer Prozess, der nach der folgenden Gleichung abläuft:
- (Methan + Wasserdampf → Kohlenstoffmonoxid + Wasserstoff; endotherm) ⓘ
Die benötigte Reaktionswärme kann durch die partielle Oxidation aufgebracht werden:
- (Methan + Sauerstoff → Kohlenstoffmonoxid + Wasserstoff; exotherm) ⓘ
Zur Steigerung der Wasserstoffausbeute kann das entstehende Kohlenmonoxid in einer weiteren Reaktion, der Wassergas-Shift-Reaktion, zu Kohlendioxid und weiterem Wasserstoff umgesetzt werden. ⓘ
- (Wassergas-Shift-Reaktion; leicht exotherm) ⓘ
Zur Durchführung wird heißer Wasserdampf mit dem zu reformierenden Gas (zum Beispiel Erdgas) oder mit verdampfter Flüssigkeit (zum Beispiel Leichtbenzin) vermischt und unter ständiger Energiezufuhr an einem heterogenen Katalysator in der Gasphase umgesetzt. ⓘ
Die Reaktionskinetik der Dampfreformierung, insbesondere unter Verwendung von Nickel-Tonerde-Katalysatoren, wurde seit den 1950er Jahren eingehend untersucht. ⓘ
Vor-Reformierung

Der Zweck des Vorreformierens besteht darin, höhere Kohlenwasserstoffe wie Propan, Butan oder Naphtha in Methan (CH4) aufzuspalten, was eine effizientere Reformierung im nachgeschalteten Prozess ermöglicht. ⓘ
Dampfreformierung
Die namengebende Reaktion ist die Dampfreformierung (SR) und wird durch die folgende Gleichung beschrieben: ⓘ
Über die Wasser-Gas-Verschiebungsreaktion (WGSR) wird durch die Reaktion von Wasser mit dem gemäß Gleichung [1] erzeugten Kohlenmonoxid zusätzlicher Wasserstoff freigesetzt: ⓘ
Einige zusätzliche Reaktionen, die im Rahmen von Dampfreformierungsprozessen auftreten, wurden untersucht. Üblicherweise wird auch die direkte Dampfreformierung (DSR) einbezogen: ⓘ
Da diese Reaktionen an sich sehr endotherm sind (mit Ausnahme der WGSR, die leicht exotherm ist), muss dem Reaktor eine große Menge an Wärme zugeführt werden, um die Temperatur konstant zu halten. Optimale Betriebsbedingungen für SMR-Reaktoren liegen in einem Temperaturbereich von 800 °C bis 900 °C bei mittleren Drücken von 20-30 bar. Es ist ein hoher Dampfüberschuss erforderlich, ausgedrückt durch das (molare) Dampf-Kohlenstoff-Verhältnis (S/C). Typische Werte für das S/C-Verhältnis liegen im Bereich von 2,5:1 bis 3:1. ⓘ
Industrielle Praxis
Die Reaktion wird in mehrröhrigen Schüttschichtreaktoren durchgeführt, einer Unterart der Kategorie der Pfropfenströmungsreaktoren. Diese Reaktoren bestehen aus einer Reihe langer und schmaler Rohre, die sich in der Brennkammer eines großen Industrieofens befinden und die notwendige Energie liefern, um den Reaktor während des Betriebs auf einer konstanten Temperatur zu halten. Je nach Brennerkonfiguration gibt es unterschiedliche Ofenkonstruktionen, die typischerweise in folgende Kategorien eingeteilt werden: von oben befeuerte, von unten befeuerte und von der Seite befeuerte Öfen. Eine bemerkenswerte Konstruktion ist der Foster-Wheeler-Terrassenwandreformer. ⓘ
In den Rohren wird ein Gemisch aus Dampf und Methan mit einem Nickelkatalysator in Kontakt gebracht. Katalysatoren mit einem großen Verhältnis von Oberfläche zu Volumen werden bevorzugt, da die Diffusion bei hohen Betriebstemperaturen eingeschränkt ist. Beispiele für verwendete Katalysatorformen sind Speichenräder, Zahnräder und Ringe mit Löchern (siehe: Raschig-Ringe). Außerdem haben diese Formen einen geringen Druckabfall, was für diese Anwendung von Vorteil ist. ⓘ
Die Dampfreformierung von Erdgas hat einen Wirkungsgrad von 65-75 %. ⓘ
In den Vereinigten Staaten werden 9-10 Millionen Tonnen Wasserstoff pro Jahr produziert, hauptsächlich durch Dampfreformierung von Erdgas. Die weltweite Ammoniakproduktion unter Verwendung von durch Dampfreformierung gewonnenem Wasserstoff belief sich 2018 auf 144 Millionen Tonnen. Der Energieverbrauch wurde von 100 GJ/Tonne Ammoniak im Jahr 1920 auf 27 GJ im Jahr 2019 gesenkt. ⓘ
Weltweit werden fast 50 % des Wasserstoffs durch Dampfreformierung erzeugt. Sie ist derzeit die kostengünstigste Methode der Wasserstofferzeugung, was die Kapitalkosten angeht. ⓘ
In dem Bestreben, die Wasserstoffproduktion zu dekarbonisieren, werden in der Industrie Methoden zur Kohlenstoffabscheidung und -speicherung (CCS) eingesetzt, die das Potenzial haben, bis zu 90 % des im Prozess entstehenden CO2 zu entfernen. Dennoch ist die Umsetzung dieser Technologie nach wie vor problematisch und kostspielig und erhöht den Preis des erzeugten Wasserstoffs erheblich. ⓘ
Autothermes Reformieren
Bei der autothermen Reformierung (ATR) werden Sauerstoff und Kohlendioxid oder Dampf in einer Reaktion mit Methan zur Bildung von Synthesegas eingesetzt. Die Reaktion findet in einer einzigen Kammer statt, in der das Methan teilweise oxidiert wird. Die Reaktion ist exotherm. Wenn der ATR Kohlendioxid verwendet, beträgt das erzeugte H2:CO-Verhältnis 1:1; wenn der ATR Dampf verwendet, beträgt das erzeugte H2:CO-Verhältnis 2,5:1. Die Austrittstemperatur des Synthesegases liegt zwischen 950-1100 °C und der Austrittsdruck kann bis zu 100 bar betragen. ⓘ
Zusätzlich zu den Reaktionen [1] - [3] wird bei ATR die folgende Reaktion durchgeführt: ⓘ
Der Hauptunterschied zwischen SMR und ATR besteht darin, dass bei SMR nur Luft zur Verbrennung als Wärmequelle für die Dampferzeugung verwendet wird, während bei ATR gereinigter Sauerstoff eingesetzt wird. Der Vorteil von ATR ist, dass das H2:CO-Verhältnis variiert werden kann, was für die Herstellung von Spezialprodukten nützlich sein kann. Aufgrund des exothermen Charakters einiger zusätzlicher Reaktionen bei ATR kann der Prozess im Wesentlichen mit einer Nettoenthalpie von Null (ΔH = 0) durchgeführt werden. ⓘ
Partielle Oxidation
Partielle Oxidation (POX) tritt auf, wenn ein unterstöchiometrisches Brennstoff-Luft-Gemisch in einem Reformer teilweise verbrannt wird und dabei wasserstoffreiches Synthesegas entsteht. POX ist in der Regel viel schneller als die Dampfreformierung und erfordert einen kleineren Reaktorbehälter. Bei der POX wird pro Einheit des eingesetzten Brennstoffs weniger Wasserstoff erzeugt als bei der Dampfreformierung desselben Brennstoffs. ⓘ
Dampfreformierung in kleinem Maßstab
Die Kapitalkosten für Dampfreformierungsanlagen werden für kleine bis mittlere Anwendungen als unerschwinglich angesehen. Die Kosten für diese aufwendigen Anlagen lassen sich nicht gut skalieren. Herkömmliche Dampfreformierungsanlagen arbeiten bei Drücken zwischen 200 und 600 psi (14-40 bar) mit Austrittstemperaturen im Bereich von 815 bis 925 °C. ⓘ
Für Verbrennungsmotoren
Abgefackeltes Gas und entweichende flüchtige organische Verbindungen (VOC) sind bekannte Probleme in der Offshore-Industrie und in der Öl- und Gasindustrie an Land, da beide Treibhausgase in die Atmosphäre abgeben. Die Reformierung für Verbrennungsmotoren nutzt die Dampfreformierungstechnologie zur Umwandlung von Abgasen in eine Energiequelle. ⓘ
Die Reformierung für Verbrennungsmotoren basiert auf der Dampfreformierung, bei der Nicht-Methan-Kohlenwasserstoffe (NMHC) minderwertiger Gase in Synthesegas (H2 + CO) und schließlich in Methan (CH4), Kohlendioxid (CO2) und Wasserstoff (H2) umgewandelt werden, wodurch die Qualität des Brenngases (Methanzahl) verbessert wird. ⓘ
Für Brennstoffzellen
Es besteht auch Interesse an der Entwicklung wesentlich kleinerer Anlagen, die auf einer ähnlichen Technologie basieren, um Wasserstoff als Ausgangsstoff für Brennstoffzellen zu erzeugen. Kleine Dampfreformierungsanlagen zur Versorgung von Brennstoffzellen sind derzeit Gegenstand von Forschung und Entwicklung, wobei in der Regel Methanol reformiert wird, aber auch andere Brennstoffe wie Propan, Benzin, Autogas, Dieselkraftstoff und Ethanol in Betracht gezogen werden. ⓘ
Benachteiligungen
Der Reformer - das Brennstoffzellensystem wird noch erforscht, aber in naher Zukunft würden die Systeme weiterhin mit bestehenden Kraftstoffen wie Erdgas, Benzin oder Diesel betrieben. Es gibt jedoch eine lebhafte Debatte darüber, ob die Verwendung dieser Brennstoffe zur Herstellung von Wasserstoff vorteilhaft ist, da die globale Erwärmung ein Thema ist. Durch die Reformierung fossiler Brennstoffe wird die Freisetzung von Kohlendioxid in die Atmosphäre zwar nicht verhindert, aber die Kohlendioxidemissionen werden reduziert und die Kohlenmonoxidemissionen im Vergleich zur Verbrennung herkömmlicher Brennstoffe aufgrund des höheren Wirkungsgrads und der Eigenschaften der Brennstoffzellen nahezu eliminiert. Dadurch, dass die Freisetzung von Kohlendioxid zu einer Punktquelle und nicht zu einer verteilten Freisetzung wird, besteht die Möglichkeit der Kohlendioxidabscheidung und -speicherung, wodurch die Freisetzung von Kohlendioxid in die Atmosphäre verhindert würde, was jedoch die Kosten des Prozesses erhöht. ⓘ
Die Kosten der Wasserstofferzeugung durch die Reformierung fossiler Brennstoffe hängen von der Größe des Prozesses, den Kapitalkosten des Reformers und der Effizienz der Anlage ab, so dass die Kosten für ein Kilogramm Wasserstoff im industriellen Maßstab nur wenige Dollar betragen, während sie im kleineren Maßstab, wie er für Brennstoffzellen benötigt wird, teurer sein können. ⓘ
Herausforderungen bei der Versorgung von Brennstoffzellen mit Reformern
Mit dieser Technologie sind mehrere Herausforderungen verbunden:
- Die Reformierungsreaktion findet bei hohen Temperaturen statt, so dass sie nur langsam anläuft und teure Hochtemperaturmaterialien erfordert.
- Schwefelverbindungen im Kraftstoff vergiften bestimmte Katalysatoren, was es schwierig macht, diese Art von System mit normalem Benzin zu betreiben. Einige neue Technologien haben diese Herausforderung mit schwefeltoleranten Katalysatoren überwunden.
- Eine weitere Ursache für die Deaktivierung des Katalysators bei der Dampfreformierung ist die Verkokung. Hohe Reaktionstemperaturen, ein niedriges Dampf-Kohlenstoff-Verhältnis (S/C) und die komplexe Beschaffenheit schwefelhaltiger kommerzieller Kohlenwasserstoffbrennstoffe begünstigen die Verkokung besonders. Olefine, typischerweise Ethylen, und Aromaten sind bekannte Kohlenstoffvorläufer, weshalb ihre Bildung während der Dampfreformierung reduziert werden muss. Außerdem wurde berichtet, dass Katalysatoren mit geringerem Säuregehalt weniger anfällig für Verkokungen sind, da sie Dehydrierungsreaktionen unterdrücken. H2S, das Hauptprodukt bei der Reformierung von organischem Schwefel, kann sich an alle Übergangsmetallkatalysatoren binden, um Metall-Schwefel-Bindungen zu bilden und anschließend die Katalysatoraktivität zu verringern, indem es die Chemisorption von Reformierungsreaktanten hemmt. Gleichzeitig erhöht die adsorbierte Schwefelspezies den Säuregrad des Katalysators und fördert somit indirekt die Verkokung. Edelmetallkatalysatoren wie Rh und Pt neigen weniger zur Bildung von Massensulfiden als andere Metallkatalysatoren wie Ni. Rh und Pt sind weniger anfällig für Schwefelvergiftungen, da sie nur Schwefel chemisch absorbieren und keine Metallsulfide bilden.
- Niedertemperatur-Polymer-Brennstoffzellenmembranen können durch das im Reaktor erzeugte Kohlenmonoxid (CO) vergiftet werden, so dass komplexe CO-Entfernungssysteme erforderlich sind. Festoxid-Brennstoffzellen (SOFC) und Schmelzkarbonat-Brennstoffzellen (MCFC) haben dieses Problem nicht, arbeiten aber bei höheren Temperaturen, was die Anlaufzeit verlangsamt und kostspielige Materialien und sperrige Isolierungen erfordert.
- Der thermodynamische Wirkungsgrad des Prozesses liegt je nach Reinheit des Wasserstoffprodukts zwischen 70 und 85 % (LHV-Basis). ⓘ
Geschichte
Die Entwicklung der Dampfreformierung geht auf Carl Bosch zurück, der in den 1920er Jahren auf der Suche nach preiswerten Wasserstoffquellen für das Haber-Bosch-Verfahren zur Synthese von Ammoniak war. Das erste Patent wurde Georg Schiller von der I.G. Farben erteilt, dem die Dampfreformierung von Methan mittels eines Nickeloxid-Katalysators gelang. Die I.G. Farben erteilte der Standard Oil of New Jersey eine Lizenz. Schon 1931 nahm das Unternehmen die Wasserstoffproduktion durch Dampfreformierung in ihrem Werk in Baton Rouge in Louisiana auf. Die Dampfreformierung von Erdgas produzierte 2014 etwa 48 Prozent des global verwendeten Wasserstoffs, davon nutzte das Haber-Bosch-Verfahren zirka 60 Prozent. ⓘ
Feststoffe
Da komplexe Feststoffe wie Holz, Klärschlamm oder kommunale Abfälle nicht verdampft werden können, müssen diese unter anderen Bedingungen reformiert werden. Die Reformierung erfolgt mittels überkritischem Wasser an einem heterogenen Katalysator bei 250–300 bar, 400–550 °C und großem Wasserüberschuss. Die Entstehung von Luftschadstoffen wie in der Müllverbrennung spielt unter diesen extremen Bedingungen praktisch keine Rolle. ⓘ



![{\displaystyle [1]\qquad \mathrm {CH} _{4}+\mathrm {H} _{2}\mathrm {O} \rightleftharpoons \mathrm {CO} +3\,\mathrm {H} _{2}\qquad \Delta H_{SR}=206\ \mathrm {kJ/mol} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/18425745de19e67ce1101ed40e14d1495dd1dd6f)
![{\displaystyle [2]\qquad \mathrm {CO} +\mathrm {H} _{2}\mathrm {O} \rightleftharpoons \mathrm {CO} _{2}+\mathrm {H} _{2}\qquad \Delta H_{WGSR}=-41\ \mathrm {kJ/mol} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/df5ce0b280b4adf926379079f62fc688cd58195f)
![{\displaystyle [3]\qquad \mathrm {CH} _{4}+2\,\mathrm {H} _{2}\mathrm {O} \rightleftharpoons \mathrm {CO} _{2}+4\,\mathrm {H} _{2}\qquad \Delta H_{DSR}=165\ \mathrm {kJ/mol} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/9102dbbc7ddf45c3b07f0c78e61d8a731c315ef0)
![{\displaystyle [4]\qquad \mathrm {CH} _{4}+0.5\,\mathrm {O} _{2}\rightleftharpoons \mathrm {CO} +2\,\mathrm {H} _{2}\qquad \Delta H_{R}=-24.5\ \mathrm {kJ/mol} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/e215fcd23897a98f2810ec168bfe701ddc53323c)