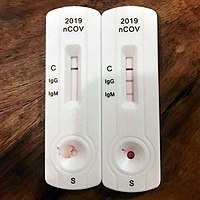
Corona-Test
| Teil einer Serie über die ⓘ |
| COVID-19-Pandemie |
|---|
|

Bei COVID-19-Tests werden Proben analysiert, um das aktuelle oder frühere Vorhandensein von SARS-CoV-2 festzustellen. Die beiden Haupttypen von Tests weisen entweder das Vorhandensein des Virus oder die als Reaktion auf eine Infektion gebildeten Antikörper nach. Molekulare Tests zum Nachweis des Virus anhand seiner molekularen Bestandteile werden zur Diagnose einzelner Fälle und zur Verfolgung und Eindämmung von Ausbrüchen durch die Gesundheitsbehörden eingesetzt. Antikörpertests (Serologie-Immunoassays) hingegen zeigen, ob jemand die Krankheit schon einmal hatte. Sie sind für die Diagnose aktueller Infektionen weniger nützlich, da sich Antikörper möglicherweise erst Wochen nach der Infektion entwickeln. Sie werden verwendet, um die Prävalenz der Krankheit zu ermitteln, was die Schätzung der Sterblichkeitsrate erleichtert. ⓘ
Die einzelnen Gerichtsbarkeiten haben unterschiedliche Testprotokolle eingeführt, u. a. in Bezug auf die zu testenden Personen, die Häufigkeit der Tests, die Analyseprotokolle, die Probenentnahme und die Verwendung der Testergebnisse. Diese Unterschiede haben sich wahrscheinlich erheblich auf die gemeldeten Statistiken ausgewirkt, einschließlich der Fall- und Testzahlen, der Sterblichkeitsraten und der demografischen Daten der Fälle. Da die SARS-CoV-2-Übertragung Tage nach der Exposition (und vor dem Auftreten von Symptomen) erfolgt, ist eine häufige Überwachung und eine schnelle Verfügbarkeit der Ergebnisse dringend erforderlich. ⓘ
Die Testanalyse wird häufig in automatisierten medizinischen Labors mit hohem Durchsatz von Labormedizinern durchgeführt. Schnell-Selbsttests und Point-of-Care-Tests sind ebenfalls verfügbar und können eine schnellere und kostengünstigere Methode zum Nachweis des Virus darstellen, wenn auch mit geringerer Genauigkeit. ⓘ

Nur wenige Monate nach Beginn der COVID-19-Pandemie kamen erste PCR-Tests zum Nachweis des damals neuartigen SARS-CoV-2 zur Anwendung. So konnten Infizierte schnell identifiziert und durch Quarantäne isoliert sowie ihre Kontaktpersonen nachverfolgt werden. Im weiteren Verlauf der Pandemie wurden zudem auch Antigen-Schnelltests entwickelt, die zwar nicht ganz so sensitiv sind, jedoch eine breite Anwendung (auch durch Laien) ermöglichen. ⓘ
Methoden

Positive Virustests weisen auf eine aktuelle Infektion hin, während positive Antikörpertests auf eine frühere Infektion hindeuten. Andere Verfahren umfassen eine Computertomographie, die Überprüfung einer erhöhten Körpertemperatur, die Überprüfung eines niedrigen Sauerstoffgehalts im Blut und die Erkennung durch ausgebildete Hunde. ⓘ
Nachweis des Virus
Der Nachweis des Virus erfolgt in der Regel entweder durch die Suche nach der inneren RNA des Virus oder nach Proteinstücken an der Außenseite des Virus. Tests, bei denen nach den viralen Antigenen (Teilen des Virus) gesucht wird, werden Antigentests genannt. ⓘ
Es gibt mehrere Arten von Tests, die das Virus durch den Nachweis der RNA des Virus nachweisen. Diese Tests werden als Nukleinsäure- oder Molekulartests bezeichnet, nach der Molekularbiologie. Ab 2021 ist die gängigste Form des molekularen Tests der Reverse-Transkriptions-Polymerase-Kettenreaktion (RT-PCR) Test. Andere Methoden, die bei molekularen Tests eingesetzt werden, sind CRISPR, isotherme Nukleinsäureamplifikation, digitale Polymerasekettenreaktion, Microarray-Analyse und Sequenzierung der nächsten Generation. ⓘ
Test mit umgekehrter Transkription und Polymerase-Kettenreaktion (RT-PCR)
Die Polymerase-Kettenreaktion (PCR) ist ein Verfahren, bei dem ein kleines, genau definiertes DNA-Segment viele hunderttausend Mal vervielfältigt (repliziert) wird, so dass eine für die Analyse ausreichende Menge davon entsteht. Die Testproben werden mit bestimmten Chemikalien behandelt, die eine Extraktion der DNA ermöglichen. Bei der reversen Transkription wird die RNA in DNA umgewandelt. ⓘ
Bei der Polymerase-Kettenreaktion mit reverser Transkription (RT-PCR) wird zunächst durch reverse Transkription DNA gewonnen und anschließend durch PCR vervielfältigt, so dass eine für die Analyse ausreichende Menge an DNA entsteht. Die RT-PCR kann somit SARS-CoV-2 nachweisen, das nur RNA enthält. Der RT-PCR-Prozess dauert im Allgemeinen einige Stunden. Diese Tests werden auch als molekulare oder genetische Assays bezeichnet. ⓘ
Die Echtzeit-PCR (qPCR) bietet Vorteile wie Automatisierung, höheren Durchsatz und zuverlässigere Geräte. Sie ist inzwischen die bevorzugte Methode. ⓘ
Die kombinierte Technik wurde als Echtzeit-RT-PCR oder quantitative RT-PCR bezeichnet und wird manchmal mit qRT-PCR, rRT-PCR oder RT-qPCR abgekürzt, obwohl manchmal auch RT-PCR oder PCR verwendet wird. In den MIQE-Leitlinien (Minimum Information for Publication of Quantitative Real-Time PCR Experiments) wird die Bezeichnung RT-qPCR vorgeschlagen, aber nicht alle Autoren halten sich daran. ⓘ
Die durchschnittliche Empfindlichkeit für molekulare Schnelltests hängt von der jeweiligen Marke ab. Für ID NOW lag die durchschnittliche Sensitivität bei 73,0 % mit einer durchschnittlichen Spezifität von 99,7 %; für Xpert Xpress betrug die durchschnittliche Sensitivität 100 % mit einer durchschnittlichen Spezifität von 97,2 %. ⓘ
Bei einem diagnostischen Test ist die Sensitivität ein Maß dafür, wie gut ein Test echte positive Ergebnisse erkennen kann, und die Spezifität ist ein Maß dafür, wie gut ein Test echte negative Ergebnisse erkennen kann. Bei allen Tests, sowohl bei diagnostischen als auch bei Screening-Tests, gibt es in der Regel einen Kompromiss zwischen Sensitivität und Spezifität, so dass eine höhere Sensitivität eine niedrigere Spezifität bedeutet und umgekehrt.
Ein Test, der zu 90 % spezifisch ist, identifiziert 90 % der nicht infizierten Personen korrekt, während 10 % ein falsch positives Ergebnis aufweisen. ⓘ
Die Proben können durch verschiedene Methoden gewonnen werden, z. B. durch einen Nasopharyngealabstrich, Sputum (abgehustetes Material), Rachenabstriche, über einen Absaugkatheter gewonnenes Material aus den tiefen Atemwegen oder Speichel. Drosten et al. merkten an, dass bei SARS 2003 "aus diagnostischer Sicht zu beachten ist, dass Nasen- und Rachenabstriche für die Diagnose weniger geeignet erscheinen, da diese Materialien wesentlich weniger virale RNA enthalten als Sputum, und das Virus möglicherweise dem Nachweis entgeht, wenn nur diese Materialien getestet werden." ⓘ
Die Sensitivität klinischer Proben mittels RT-PCR beträgt 63 % für Nasenabstriche, 32 % für Rachenabstriche, 48 % für Fäkalien, 72-75 % für Sputum und 93-95 % für bronchoalveoläre Lavage. ⓘ
Die Wahrscheinlichkeit, das Virus nachzuweisen, hängt von der Art der Entnahme und der Zeit ab, die seit der Infektion vergangen ist. Laut Drosten sind Tests mit Rachenabstrichen nur in der ersten Woche zuverlässig. Danach kann das Virus den Rachenraum verlassen und sich in der Lunge vermehren. In der zweiten Woche ist die Entnahme von Sputum oder tiefen Atemwegen vorzuziehen. ⓘ
Die Entnahme von Speichel kann ebenso wirksam sein wie Nasen- und Rachenabstriche, obwohl dies nicht sicher ist. Die Entnahme von Speichelproben kann das Risiko für das Gesundheitspersonal verringern, da eine enge körperliche Interaktion vermieden wird. Auch für den Patienten ist es angenehmer. Personen, die unter Quarantäne stehen, können ihre eigenen Proben entnehmen. Der diagnostische Wert eines Speicheltests hängt von der Entnahmestelle ab (tiefer Rachen, Mundhöhle oder Speicheldrüsen). Einige Studien haben ergeben, dass Speichel im Vergleich zu Abstrichproben eine höhere Empfindlichkeit und Konsistenz aufweist. ⓘ
Am 15. August 2020 erteilte die US-amerikanische FDA eine Notfallzulassung für einen an der Universität Yale entwickelten Speicheltest, der innerhalb weniger Stunden Ergebnisse liefert. ⓘ
Am 4. Januar 2021 gab die US FDA eine Warnung über das Risiko falscher Ergebnisse, insbesondere falscher negativer Ergebnisse, mit dem Echtzeit-RT-PCR-Test Curative SARS-Cov-2 Assay heraus. ⓘ
Die in Proben der oberen Atemwege gemessene Viruslast nimmt nach dem Auftreten von Symptomen ab. Nach der Genesung weisen viele Patienten in Proben der oberen Atemwege keine nachweisbare virale RNA mehr auf. Bei denjenigen, bei denen dies der Fall ist, liegen die RNA-Konzentrationen drei Tage nach der Genesung im Allgemeinen unter dem Bereich, in dem replikationskompetente Viren zuverlässig isoliert werden können. Es wurde keine eindeutige Korrelation zwischen der Dauer der Erkrankung und der Dauer der Ausscheidung viraler RNA in Proben der oberen Atemwege nach der Genesung beschrieben. ⓘ
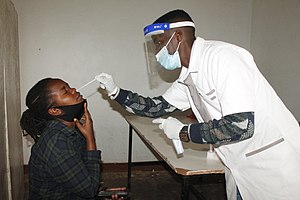
Video eines Nasopharyngealabstrichs für den COVID-19-Test ⓘ
Andere molekulare Tests
Isotherme Nukleinsäure-Amplifikationstests amplifizieren ebenfalls das Genom des Virus. Sie sind schneller als die PCR, da sie keine wiederholten Heiz- und Kühlzyklen erfordern. Bei diesen Tests wird die DNA in der Regel mit fluoreszierenden Markierungen nachgewiesen, die mit speziellen Geräten ausgelesen werden. ⓘ
Die CRISPR-Genbearbeitungstechnologie wurde für den Nachweis modifiziert: Wenn sich das CRISPR-Enzym an die Sequenz anlagert, färbt es einen Papierstreifen. Die Forscher gehen davon aus, dass der daraus resultierende Test kostengünstig und einfach in der Praxis anzuwenden sein wird. Der Test amplifiziert die RNA direkt, ohne den RNA-zu-DNA-Umwandlungsschritt der RT-PCR. ⓘ
Antigen-Tests


Ein Antigen ist der Teil eines Krankheitserregers, der eine Immunreaktion hervorruft. Bei Antigentests wird nach Antigenproteinen auf der Virusoberfläche gesucht. Im Falle eines Coronavirus handelt es sich dabei in der Regel um Proteine aus den Oberflächen-Spikes. SARS-CoV-2-Antigene können vor dem Auftreten von COVID-19-Symptomen (sobald SARS-CoV-2-Viruspartikel vorhanden sind) mit schnelleren Testergebnissen, aber mit geringerer Empfindlichkeit als PCR-Tests für das Virus nachgewiesen werden. ⓘ
COVID-19-Antigen-Schnelltests sind Lateral-Flow-Immunoassays, die das Vorhandensein eines spezifischen viralen Antigens nachweisen, das eine aktuelle Virusinfektion anzeigt. Antigentests liefern schnell Ergebnisse (innerhalb von etwa 15-30 Minuten), und die meisten können am Point-of-Care oder als Selbsttests verwendet werden. Selbsttests sind Schnelltests, die zu Hause oder an einem beliebigen Ort durchgeführt werden können, einfach zu handhaben sind und schnelle Ergebnisse liefern. Antigentests können an Nasopharyngeal-, Nasenabstrich- oder Speichelproben durchgeführt werden. ⓘ
Antigentests, mit denen SARS-CoV-2 nachgewiesen werden kann, bieten eine schnellere und kostengünstigere Methode zum Nachweis des Virus. Antigentests sind in der Regel weniger empfindlich als die Reverse-Transkriptions-Polymerase-Kettenreaktion (RT-PCR) und andere Nukleinsäure-Amplifikationstests (NAATs). ⓘ
Antigentests können eine Möglichkeit sein, die Tests auf ein viel höheres Niveau zu bringen. Isotherme Nukleinsäure-Amplifikationstests können jeweils nur eine Probe pro Gerät verarbeiten. RT-PCR-Tests sind zwar genau, erfordern aber zu viel Zeit, Energie und geschultes Personal für die Durchführung der Tests. "Es wird nie die Möglichkeit geben, mit einem [PCR-]Test 300 Millionen Tests pro Tag durchzuführen oder alle Menschen zu testen, bevor sie zur Arbeit oder zur Schule gehen", sagte Deborah Birx, Leiterin der Coronavirus Task Force des Weißen Hauses, am 17. April 2020. "Aber mit dem Antigentest könnte es das geben." ⓘ
Die Proben können über einen Nasen-Rachen-Abstrich, einen Abstrich der vorderen Nasenlöcher oder aus dem Speichel (der mit verschiedenen Methoden gewonnen wird, einschließlich Lutschertests für Kinder) gewonnen werden. Die Probe wird dann auf Papierstreifen aufgebracht, die künstliche Antikörper enthalten, die an Coronavirus-Antigene binden sollen. Die Antigene binden an die Streifen und führen zu einer visuellen Anzeige. Das Verfahren dauert weniger als 30 Minuten, kann am Ort der Behandlung Ergebnisse liefern und erfordert keine teure Ausrüstung oder umfangreiche Schulung. ⓘ
Abstriche von Atemwegsviren enthalten oft nicht genügend Antigenmaterial, um nachweisbar zu sein. Dies gilt insbesondere für asymptomatische Patienten, die wenig oder gar keinen Nasenausfluss haben. Virale Proteine werden in einem Antigentest nicht vervielfältigt. Eine Cochrane-Review auf der Grundlage von 64 Studien, in denen die Wirksamkeit von 16 verschiedenen Antigentests untersucht wurde, ergab, dass diese eine COVID-19-Infektion bei durchschnittlich 72 % der Personen mit Symptomen korrekt nachweisen, verglichen mit 58 % der Personen ohne Symptome. Die Tests waren am genauesten (78 %), wenn sie in der ersten Woche nach Auftreten der ersten Symptome angewandt wurden, was wahrscheinlich darauf zurückzuführen ist, dass die Menschen in den ersten Tagen nach der Infektion die meisten Viren in ihrem Körper haben. Während einige Wissenschaftler bezweifeln, dass ein Antigentest gegen COVID-19 nützlich sein kann, haben andere argumentiert, dass Antigentests bei hoher Viruslast und Ansteckungsgefahr sehr empfindlich sind und sich daher für das Screening im öffentlichen Gesundheitswesen eignen. Mit routinemäßigen Antigentests lässt sich schnell feststellen, ob asymptomatische Personen ansteckend sind, während eine PCR-Folgeuntersuchung eingesetzt werden kann, wenn eine bestätigende Diagnose erforderlich ist. ⓘ
Antikörper-Tests
Der Körper reagiert auf eine Virusinfektion mit der Bildung von Antikörpern, die dazu beitragen, das Virus zu neutralisieren. Bluttests (auch Serologietests oder Serologie-Immunoassays genannt) können das Vorhandensein solcher Antikörper nachweisen. Mit Hilfe von Antikörpertests lässt sich feststellen, wie hoch der Anteil der Infizierten in einer Population ist, was wiederum zur Berechnung der Sterblichkeitsrate der Krankheit herangezogen werden kann. Sie können auch verwendet werden, um festzustellen, wie viel Antikörper in einer Einheit Rekonvaleszenzplasma für die COVID-19-Behandlung enthalten sind, oder um zu überprüfen, ob ein bestimmter Impfstoff eine angemessene Immunantwort hervorruft. ⓘ
Die Wirksamkeit und die Schutzdauer von SARS-CoV-2-Antikörpern sind noch nicht nachgewiesen. Daher bedeutet ein positiver Antikörpertest nicht unbedingt eine Immunität gegen eine künftige Infektion. Außerdem ist nicht geklärt, ob milde oder asymptomatische Infektionen genügend Antikörper produzieren, um von einem Test erfasst zu werden. Antikörper gegen einige Krankheiten bleiben viele Jahre lang im Blut, während andere wieder verschwinden. ⓘ
Die bemerkenswertesten Antikörper sind IgM und IgG. IgM-Antikörper sind in der Regel einige Tage nach der Erstinfektion nachweisbar, obwohl die Werte im Verlauf der Infektion und darüber hinaus nicht gut beschrieben sind. IgG-Antikörper sind in der Regel 10-14 Tage nach der Infektion nachweisbar und erreichen normalerweise etwa 28 Tage nach der Infektion ihren Höhepunkt. Dieses Muster der Antikörperentwicklung, das bei anderen Infektionen beobachtet wurde, gilt jedoch häufig nicht für SARS-CoV-2, wobei IgM manchmal nach IgG, zusammen mit IgG oder überhaupt nicht auftritt. Im Allgemeinen wird IgM jedoch im Median 5 Tage nach Auftreten der Symptome nachgewiesen, während IgG im Median 14 Tage nach Auftreten der Symptome nachgewiesen wird. Die IgG-Werte nehmen nach zwei oder drei Monaten deutlich ab. ⓘ
Genetische Tests weisen die Infektion früher nach als Antikörpertests. Nur 30 % der Personen mit einem positiven Gentest wiesen am 7. Tag ihrer Infektion einen positiven Antikörpertest auf. ⓘ
Antikörpertest-Typen
Diagnostischer Schnelltest (RDT)
RDTs verwenden in der Regel einen kleinen, tragbaren, positiven/negativen Lateral-Flow-Assay, der am Ort der Behandlung durchgeführt werden kann. RDTs können Blutproben, Speichelproben oder Nasenabstriche verarbeiten. RDTs erzeugen farbige Linien, um positive oder negative Ergebnisse anzuzeigen. ⓘ
Enzym-Immunoassay (ELISA)
ELISAs können qualitativ oder quantitativ sein und erfordern im Allgemeinen ein Labor. Für diese Tests werden normalerweise Vollblut-, Plasma- oder Serumproben verwendet. Eine Platte wird mit einem viralen Protein beschichtet, z. B. einem SARS-CoV-2-Spike-Protein. Die Proben werden mit dem Protein inkubiert, so dass sich etwaige Antikörper an das Protein binden können. Der Antikörper-Protein-Komplex kann dann mit einer weiteren Waschung von Antikörpern, die eine Farb-/Fluoreszenzanzeige erzeugen, nachgewiesen werden. ⓘ
Neutralisierungs-Assay
Mit Neutralisationstests wird untersucht, ob die Antikörper der Probe eine Virusinfektion in den Testzellen verhindern. Bei diesen Tests wird Blut, Plasma oder Serum verwendet. Für den Test werden Zellen kultiviert, die eine virale Vermehrung ermöglichen (z. B. Vero E6-Zellen). Durch Variation der Antikörperkonzentrationen können die Forscher sichtbar machen und quantifizieren, wie viele Testantikörper die Virusreplikation blockieren. ⓘ
Chemilumineszenz-Immunoassay
Chemilumineszenz-Immunoassays sind quantitative Labortests. Dabei werden Blut-, Plasma- oder Serumproben entnommen. Die Proben werden mit einem bekannten viralen Protein, Pufferreagenzien und spezifischen, enzymmarkierten Antikörpern vermischt. Das Ergebnis ist lumineszierend. Bei einem Chemilumineszenz-Mikropartikel-Immunoassay werden magnetische, proteinbeschichtete Mikropartikel verwendet. Die Antikörper reagieren mit dem viralen Protein und bilden einen Komplex. Sekundäre, mit Enzymen markierte Antikörper werden hinzugefügt und binden an diese Komplexe. Die daraus resultierende chemische Reaktion erzeugt Licht. Anhand der Strahlungsintensität wird die Anzahl der Antikörper berechnet. Mit diesem Test können mehrere Arten von Antikörpern nachgewiesen werden, darunter IgG, IgM und IgA. ⓘ
Neutralisierende vs. bindende Antikörper
Die meisten, wenn nicht sogar alle groß angelegten COVID-19-Antikörpertests suchen nur nach bindenden Antikörpern und messen nicht die wichtigeren neutralisierenden Antikörper (NAb). Ein NAb ist ein Antikörper, der die Infektiosität eines Viruspartikels neutralisiert, indem er dessen Anheftung an oder Eintritt in eine empfängliche Zelle blockiert. Umhüllte Viren, wie z. B. SARS-CoV-2, werden durch die Blockierung von Schritten im Replikationszyklus bis hin zur Membranfusion neutralisiert. Ein nicht neutralisierender Antikörper bindet entweder nicht an die entscheidenden Strukturen auf der Virusoberfläche oder er bindet zwar, lässt das Viruspartikel aber infektiös; der Antikörper kann dennoch zur Zerstörung von Viruspartikeln oder infizierten Zellen durch das Immunsystem beitragen. Er kann sogar die Infektiosität erhöhen, indem er mit Rezeptoren auf Makrophagen interagiert. Da die meisten COVID-19-Antikörpertests ein positives Ergebnis liefern, wenn sie nur bindende Antikörper finden, können diese Tests nicht anzeigen, dass die Testperson schützende NAbs gebildet hat, die vor einer erneuten Infektion schützen. ⓘ
Man geht davon aus, dass bindende Antikörper auf das Vorhandensein von NAbs hindeuten, und bei vielen Viruserkrankungen korrelieren die Gesamtantikörperreaktionen in gewissem Maße mit den NAb-Reaktionen, doch ist dies für COVID-19 nicht nachgewiesen. In einer Studie mit 175 genesenen Patienten in China, die leichte Symptome aufwiesen, wurde berichtet, dass bei 10 Personen bei der Entlassung oder danach keine NAbs nachweisbar waren. Es wurde nicht untersucht, wie sich diese Patienten ohne die Hilfe von NAbs erholten und ob für sie ein Risiko einer erneuten Infektion bestand. Eine zusätzliche Unsicherheit besteht darin, dass Viren wie HIV selbst bei Vorhandensein von NAbs die NAb-Reaktionen umgehen können. ⓘ
Studien haben gezeigt, dass NAbs gegen das ursprüngliche SARS-Virus (den Vorgänger des aktuellen SARS-CoV-2) zwei Jahre lang aktiv bleiben können und nach sechs Jahren verschwunden sind. Gedächtniszellen, einschließlich Gedächtnis-B-Zellen und Gedächtnis-T-Zellen, können jedoch viel länger aktiv bleiben und sind möglicherweise in der Lage, die Schwere der Reinfektion zu verringern. ⓘ
Der diagnostische Schnelltest zeigt Reaktionen von IgG- und IgM-Antikörpern an. ⓘ
Andere Tests
Schnuppertests
Der plötzliche Verlust des Geruchsinns kann genutzt werden, um Menschen im Alltag auf COVID-19 zu testen. Eine Studie der National Institutes of Health hat gezeigt, dass Personen, die mit SARS-CoV-2 infiziert sind, eine 25%ige Mischung aus Ethanol und Wasser nicht riechen können. Da verschiedene Erkrankungen zum Verlust des Geruchssinns führen können, wäre ein Schnuppertest nicht aussagekräftig, sondern würde auf die Notwendigkeit eines PCR-Tests hinweisen. Da sich der Verlust des Geruchssinns vor anderen Symptomen bemerkbar macht, wurde ein umfassender Schnuppertest gefordert. Die Bürokratie des Gesundheitswesens hat Schnuppertests im Allgemeinen ignoriert, obwohl sie schnell und einfach sind und täglich selbst durchgeführt werden können. Dies hat einige medizinische Fachzeitschriften dazu veranlasst, Leitartikel zu verfassen, die die Einführung von Schnuppertests unterstützen. ⓘ
Bildgebung
Typische sichtbare Merkmale auf dem CT sind zunächst bilaterale multilobare Mattigkeit mit einer peripheren oder posterioren Verteilung. COVID-19 kann im CT mit höherer Genauigkeit identifiziert werden als mit RT-PCR. ⓘ
Im weiteren Verlauf der Erkrankung können sich subpleurale Dominanz, Crazy Paving und Konsolidierung entwickeln. Thorax-CT-Scans und Thorax-Röntgenaufnahmen werden für die Diagnose von COVID-19 nicht empfohlen. Radiologische Befunde bei COVID-19 sind nicht spezifisch. ⓘ
Serologische Tests (CoLab-Score)
Der in der Notaufnahme durchgeführte Standard-Bluttest (Quick Scan) misst verschiedene Werte. Mit Hilfe des Blut-Schnelltests wird der CoLab-Score mit einem entwickelten Algorithmus berechnet, der darauf basiert, wie das Coronavirus Veränderungen im Blut verursacht. Die Software ist für den Einsatz in der Notaufnahme gedacht, um das Vorhandensein der Krankheit bei ankommenden Patienten schnell auszuschließen. Bei einem nicht negativen Ergebnis wird ein PCR- (Polymerase-Kettenreaktion) oder LAMP-Test (loop-mediated isothermal amplification) durchgeführt. ⓘ
Atemtests
Der Atemtest mit einem Coronavirus-Atemtestgerät ist ein Vorscreening-Test für Personen, die keine oder nur leichte Symptome von COVID-19 haben. Bei einem nicht negativen Ergebnis wird ein PCR- oder LAMP-Test durchgeführt. ⓘ
Tiere
Im Mai 2021 berichtete Reuters, dass niederländische Forscher der Universität Wageningen gezeigt haben, dass geschulte Bienen das Virus in infizierten Proben in Sekundenschnelle nachweisen können, was Ländern zugute kommen könnte, in denen Testeinrichtungen Mangelware sind. Eine zweimonatige Studie des Pariser Necker-Cochin-Krankenhauses in Zusammenarbeit mit der nationalen französischen Veterinärschule berichtete im Mai 2021, dass Hunde zuverlässiger seien als die derzeitigen Lateral-Flow-Tests. ⓘ
Im März 2022 berichteten Pariser Forscher in einer noch nicht begutachteten Vorabveröffentlichung, dass ausgebildete Hunde das Vorhandensein von SARS-Cov2 bei Menschen, ob sie Symptome zeigen oder nicht, sehr effektiv nachweisen können. Den Hunden wurden Schweißproben von 335 Personen zum Riechen vorgelegt, von denen 78 mit Symptomen und 31 ohne Symptome durch PCR positiv getestet wurden. Die Hunde erkannten 97 % der symptomatischen und 100 % der asymptomatischen Infektionen. Mit einer Genauigkeit von 91 % identifizierten sie Freiwillige, die nicht infiziert waren, und mit einer Genauigkeit von 94 % schlossen sie die Infektion bei Personen ohne Symptome aus. Weitere Studien werden sich auf das direkte Erschnüffeln durch Hunde konzentrieren, um Spürhunde für Massen-Vortests in Flughäfen, Häfen, Bahnhöfen, bei kulturellen Aktivitäten oder Sportveranstaltungen zu bewerten", so die Autoren. ⓘ
Funktionelle Assays
Tollotest ist ein molekularer Test, der die Aktivität einer SARS-CoV2-Protease nachweist, die ein Biomarker für eine aktive Infektion ist. ⓘ
Geschichte

Im Januar 2020 veröffentlichten Wissenschaftler aus China die ersten genetischen Sequenzen von SARS-CoV-2 über GISAID, ein Programm, das normalerweise genetische Sequenzdaten verarbeitet. Forscher in aller Welt nutzten diese Daten, um molekulare Tests für das Virus zu entwickeln. Später wurden antigen- und antikörperbasierte Tests entwickelt. ⓘ
Selbst als die ersten Tests entwickelt waren, war das Angebot begrenzt. Infolgedessen verfügte kein Land zu Beginn der Pandemie über zuverlässige Daten zur Prävalenz des Virus. Die WHO und andere Experten riefen dazu auf, die Zahl der Tests zu erhöhen, da dies der beste Weg sei, die Ausbreitung des Virus zu verlangsamen. Engpässe bei der Versorgung mit Reagenzien und anderen Testmaterialien wurden zu einem Engpass für Massentests in der EU, dem Vereinigten Königreich und den USA. Bei den ersten Tests traten auch Probleme mit der Zuverlässigkeit auf. ⓘ
Testprotokolle
Drive-Through-Tests
Bei Drive-Through-Tests bleibt die zu testende Person in einem Fahrzeug sitzen, während eine medizinische Fachkraft sich dem Fahrzeug nähert und eine Probe entnimmt, wobei sie entsprechende Vorsichtsmaßnahmen wie das Tragen von persönlicher Schutzausrüstung (PSA) trifft. Drive-Through-Zentren haben Südkorea geholfen, sein Testprogramm zu beschleunigen. ⓘ
Entnahme zu Hause
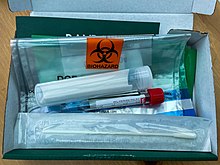
In Hongkong können die Testpersonen zu Hause bleiben und erhalten ein Probenröhrchen. Sie spucken hinein, geben es zurück und erhalten später das Ergebnis. ⓘ
Gepoolte Tests
Pooltests können die Durchlaufzeit verkürzen, indem sie eine Reihe von Proben zusammenfassen, die gemeinsam getestet werden. Fällt das Ergebnis des Pooltests negativ aus, sind alle Proben negativ. Ist das Testergebnis positiv, müssen die Proben einzeln getestet werden. ⓘ
In Israel haben Forscher des Technion und des Rambam-Krankenhauses eine Methode entwickelt, mit der Proben von 64 Patienten gleichzeitig getestet werden können, indem sie die Proben zusammenfassen und nur dann weiter testen, wenn die kombinierte Probe positiv ist. Pooltests wurden daraufhin in Israel, Deutschland, Ghana, Südkorea, Nebraska, China und in den indischen Bundesstaaten Uttar Pradesh, West Bengal, Punjab, Chhattisgarh und Maharashtra eingeführt. ⓘ
Mit den Open-Source-Multiplex-Designs von Origami Assays können bis zu 1122 Patientenproben mit nur 93 Assays getestet werden. Diese ausgewogenen Designs können in kleinen Labors ohne robotergestützte Liquid-Handler durchgeführt werden. ⓘ
Mehrstufige Tests
In einer Studie wurde ein Schnelltest für die Immunantwort als Screening-Test vorgeschlagen, mit einem bestätigenden Nukleinsäuretest für die Diagnose, gefolgt von einem Antikörper-Schnelltest, um das weitere Vorgehen zu bestimmen und die Exposition der Bevölkerung bzw. die Immunität zu bewerten. ⓘ
Erforderliches Volumen
Die Anzahl der erforderlichen Tests hängt von der Ausbreitung der Krankheit ab. Je mehr Fälle auftreten, desto mehr Tests sind erforderlich, um den Ausbruch zu kontrollieren. COVID-19 neigt dazu, zu Beginn eines Ausbruchs exponentiell zu wachsen, was bedeutet, dass die Zahl der erforderlichen Tests zunächst ebenfalls exponentiell ansteigt. Wenn die Zahl der gezielten Tests schneller wächst als die Zahl der Fälle, kann der Ausbruch eingedämmt werden. ⓘ
Die WHO empfiehlt, die Zahl der Tests zu erhöhen, bis weniger als 10 % der Fälle in einem bestimmten Land positiv sind. ⓘ
Vereinigte Staaten
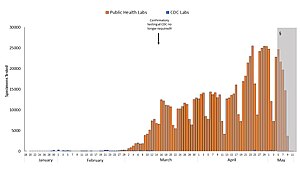
Blau: CDC-Labor
Orange: Öffentliches Gesundheitslabor
Grau: Daten unvollständig aufgrund von Verzögerungen bei der Berichterstattung
Nicht gezeigt: Tests in privaten Labors; die Gesamtzahl überstieg am 27. März 100.000 pro Tag. ⓘ
Der Wirtschaftswissenschaftler Paul Romer berichtete, dass die USA über die technischen Kapazitäten verfügen, um bis zu 20 Millionen Tests pro Tag durchzuführen, was seiner Schätzung nach der Größenordnung entspricht, die für eine vollständige Remobilisierung der Wirtschaft erforderlich ist. Das Edmond J. Safra Center for Ethics schätzte am 4. April 2020, dass diese Kapazität bis Ende Juli 2020 verfügbar sein könnte. Romer verwies auf die Einzelmolekül-Echtzeitsequenzierungsgeräte von Pacific Biosciences und auf die Ion Torrent Next-Generation Sequencing-Geräte von ThermoFisher Scientific. Jüngste Forschungsarbeiten deuten darauf hin, dass jedes dieser Geräte das Potenzial hat, bis zu Millionen von Tests pro Tag durchzuführen", so Romer. Dieser Plan erfordert die Beseitigung regulatorischer Hürden. Romer schätzt, dass die Kosten von 100 Milliarden Dollar gedeckt werden könnten. ⓘ
Romer behauptete auch, dass eine hohe Testgenauigkeit nicht erforderlich ist, wenn die Tests häufig genug durchgeführt werden. Er führte Modellsimulationen durch, bei denen 7 % der Bevölkerung täglich mit einem Test getestet werden, der eine Falsch-Negativ-Rate von 20 % und eine Falsch-Positiv-Rate von 1 % aufweist. Die durchschnittliche Person würde etwa alle zwei Wochen getestet werden. Diejenigen, die positiv getestet würden, kämen in Quarantäne. Die Simulation von Romer ergab, dass der Anteil der Bevölkerung, der zu einem bestimmten Zeitpunkt infiziert ist (die so genannte Ansteckungsrate), nach etwa dreißig Tagen einen Spitzenwert von etwa 8 % erreicht, bevor er allmählich abnimmt und bei den meisten Durchläufen nach 500 Tagen den Wert Null erreicht, wobei die kumulative Prävalenz unter 20 % bleibt. ⓘ
Schnappschuss-Massentest
Eine Studie ergab, dass der von der Slowakei durchgeführte Ansatz der Schnelltests, bei dem ~80 % der Bevölkerung innerhalb eines Wochenendes Ende Oktober 2020 auf COVID-19 getestet wurden, trotz einer möglicherweise suboptimalen Durchführung sehr wirksam war: Die beobachtete Prävalenz sank innerhalb einer Woche um 58 % und im Vergleich zu einem hypothetischen Szenario ohne Schnelltests um 70 %. Der signifikante Rückgang resultierte aus einer Reihe sich ergänzender Absperr- und Quarantänemaßnahmen, bei denen positiv getestete Bürger in den Wochen danach zeitgleich unter Quarantäne gestellt wurden. ⓘ
Überwachung und Screening von Bevölkerungsgruppen
Ab August 2020 erkennt die WHO die Abwasserüberwachung von SARS-CoV-2 als potenziell nützliche Quelle für Informationen über die Prävalenz und die zeitlichen Trends von COVID-19 in Gemeinden an, weist aber gleichzeitig darauf hin, dass Forschungslücken wie die Merkmale der Virusausscheidung geschlossen werden sollten. Durch solche aggregativen Tests könnten frühe Fälle entdeckt werden. Studien zeigen, dass die abwasserbasierte Epidemiologie das Potenzial für ein Frühwarnsystem und die Überwachung von COVID-19-Infektionen hat. Dies könnte sich als besonders nützlich erweisen, wenn große Teile der regionalen Bevölkerung geimpft oder genesen sind und keine Schnelltests mehr durchführen müssen, obwohl sie in einigen Fällen dennoch infektiös sind. ⓘ
Verfügbare Tests

Länder auf der ganzen Welt haben unabhängig voneinander und in Zusammenarbeit mit anderen Ländern Tests entwickelt. ⓘ
Nukleinsäure-Tests
Es gibt Tests, die mit Hilfe der Polymerase-Kettenreaktion (PCR) oder der LAMP-Technologie (loop-mediated isothermal amplification) nach viraler DNA suchen. ⓘ
Die in China, Frankreich, Deutschland, Hongkong, Japan, dem Vereinigten Königreich und den USA entwickelten Tests zielen auf unterschiedliche Teile des viralen Genoms ab. Die WHO hat das deutsche System für die Herstellung von Kits übernommen, die an Länder mit niedrigem Einkommen versandt werden, die nicht über die Mittel zur Entwicklung eigener Kits verfügen. ⓘ
PowerChek Coronavirus sucht nach dem "E"-Gen, das alle Beta-Coronaviren gemeinsam haben, und dem RdRp-Gen, das spezifisch für SARS-CoV-2 ist. ⓘ


Der ID Now-Nukleinsäuretest von Abbott Laboratories verwendet die isothermische Amplifikationstechnologie. Der Test amplifiziert eine einzigartige Region des RdRp-Gens des Virus; die resultierenden Kopien werden dann mit "fluoreszenzmarkierten molekularen Baken" nachgewiesen. Das Testkit verwendet das "toastergroße" ID Now-Gerät des Unternehmens, das in den USA weit verbreitet ist. Das Gerät kann in Laboratorien oder bei der Behandlung vor Ort eingesetzt werden und liefert Ergebnisse in höchstens 13 Minuten. ⓘ
Primerdesign bietet seinen Genesig Real-Time PCR Coronavirus (COVID-19) an. Der Cobas SARS-CoV-2 Qualitative Assay läuft auf den Cobas® 6800/8800 Systemen von Roche Molecular Systems. Sie werden von den Vereinten Nationen und anderen Beschaffungsstellen angeboten. ⓘ
Antigen-Tests
Antigen-Tests sind weltweit erhältlich und wurden von mehreren Gesundheitsbehörden zugelassen. ⓘ
Der "Sofia 2 SARS Antigen FIA" von Quidel ist ein Lateral-Flow-Test, der monoklonale Antikörper zum Nachweis des Nukleokapsid (N)-Proteins des Virus verwendet. Das Ergebnis wird von dem Sofia 2-Gerät des Unternehmens mittels Immunfluoreszenz ausgelesen. Der Test ist einfacher und billiger, aber weniger genau als Nukleinsäuretests. Er kann in Labors oder am Ort der Behandlung eingesetzt werden und liefert innerhalb von 15 Minuten Ergebnisse. Ein falsch negatives Ergebnis liegt vor, wenn der Antigengehalt der Probe zwar positiv ist, aber unter der Nachweisgrenze des Tests liegt, so dass eine Bestätigung durch einen Nukleinsäuretest erforderlich ist. ⓘ
Der qualitative SARS-CoV-2-Antigen-Schnelltest von Innova war nie für die Verwendung in den Vereinigten Staaten zugelassen, wurde aber dennoch von dem Unternehmen verkauft. Die FDA inspizierte im März und April 2021 Einrichtungen von Innova in Kalifornien und stellte eine unzureichende Qualitätssicherung der in China hergestellten Tests fest. Am 23. April 2021 gab das Unternehmen einen Rückruf heraus. Die FDA warnte die Verbraucher, die Geräte zurückzugeben oder zu vernichten, da die Rate der in klinischen Studien festgestellten falsch-positiven und falsch-negativen Ergebnisse höher war als die auf der Verpackung angegebene Rate. Mehr als eine Milliarde Tests des Unternehmens wurden im Vereinigten Königreich verteilt, mit einer Finanzierung von 3 Milliarden Pfund im Rahmen der Operation Moonshot, und die MHRK hat die Verwendung in Ausnahmefällen bis mindestens 28. August 2021 genehmigt. Besorgte Experten wiesen darauf hin, dass die Genauigkeit deutlich abnimmt, wenn das Screening von der Öffentlichkeit und nicht von medizinischem Fachpersonal durchgeführt wird, und dass der Test nicht für die Untersuchung asymptomatischer Personen konzipiert ist. Eine Studie aus dem Jahr 2020 ergab, dass 79 % der positiven Fälle gefunden wurden, wenn sie von Laborwissenschaftlern durchgeführt wurden, aber nur 58 %, wenn sie von der Allgemeinheit durchgeführt wurden, und 40 %, wenn sie für ein stadtweites Screening in Liverpool verwendet wurden. ⓘ
Serologische (Antikörper-)Tests
Antikörper sind in der Regel 14 Tage nach Ausbruch der Infektion nachweisbar. Mehrere Gerichtsbarkeiten untersuchen ihre Bevölkerung mit diesen Tests. Für den Test ist eine Blutprobe erforderlich. ⓘ
Private US-Labors wie Quest Diagnostics und LabCorp bieten auf Anfrage Antikörpertests an. ⓘ
Bestimmte Antikörpertests sind in mehreren europäischen Ländern und auch in den USA erhältlich. Quotient Limited hat einen CE-gekennzeichneten Antikörpertest entwickelt, der auch eine Notfallzulassung der US-FDA erhalten hat. ⓘ
Roche bietet einen selektiven ELISA-Serologietest an. ⓘ
In einer zusammenfassenden Übersichtsarbeit im BMJ wurde festgestellt, dass zwar einige serologische Tests ... billiger und am Ort der Behandlung einfacher durchzuführen sein könnten [als RT-PCR]" und dass solche Tests bereits infizierte Personen identifizieren können, dass aber Vorsicht geboten ist ... bei der Verwendung serologischer Tests für die epidemiologische Überwachung". Der Bericht forderte Studien von höherer Qualität, die die Genauigkeit anhand eines Standards von RT-PCR an mindestens zwei aufeinanderfolgenden Proben und, wenn möglich, unter Einbeziehung von Viruskulturen" bewerten. Die CEBM-Forscher forderten, dass bei der Falldefinition im Krankenhaus "CT-Lungenbefunde und zugehörige Bluttests" erfasst werden und dass die WHO ein "Protokoll zur Standardisierung der Verwendung und Interpretation der PCR" mit kontinuierlicher Rekalibrierung erstellt. ⓘ
Genauigkeit
| Quelle der Proben | Positive Rate ⓘ |
|---|---|
| Proben aus bronchoalveolärer Lavageflüssigkeit | 93% (14/15) |
| Sputum | 72% (75/104) |
| Nasenabstriche | 63% (5/8) |
| Fibrobronchoskop-Bürstenbiopsie | 46% (6/13) |
| Pharyngeale Abstriche | 32% (126/398) |
| Fäkalien | 29% (44/153) |
| Blut | 1% (3/307) |
Die Genauigkeit wird anhand der Spezifität und Selektivität gemessen. Testfehler können falsch positiv (der Test ist positiv, aber das Virus ist nicht vorhanden) oder falsch negativ (der Test ist negativ, aber das Virus ist vorhanden) sein. ⓘ
Sensitivität und Spezifität
Die Sensitivität gibt an, ob der Test das Vorhandensein des Virus genau feststellt. Jeder Test erfordert eine Mindestmenge an Viruslast, um ein positives Ergebnis zu liefern. Ein Test, der zu 90 % empfindlich ist, erkennt 90 % der Infektionen korrekt, während die übrigen 10 % nicht erkannt werden (falsch negativ). Selbst relativ hohe Sensitivitätsraten können in Populationen mit niedrigen Inzidenzraten zu hohen Raten von falsch-negativen Ergebnissen führen. ⓘ
Bei einem diagnostischen Test ist die Sensitivität ein Maß dafür, wie gut ein Test echte positive Ergebnisse erkennen kann, und die Spezifität ist ein Maß dafür, wie gut ein Test echte negative Ergebnisse erkennen kann. Bei allen Tests, sowohl bei diagnostischen als auch bei Screening-Tests, gibt es in der Regel einen Kompromiss zwischen Sensitivität und Spezifität, so dass eine höhere Sensitivität eine niedrigere Spezifität bedeutet und umgekehrt.
Ein Test, der zu 90 % spezifisch ist, identifiziert 90 % der nicht infizierten Personen korrekt, während 10 % ein falsch positives Ergebnis aufweisen. ⓘ
Tests mit geringer Spezifität haben einen niedrigen positiven prädiktiven Wert (PPV), wenn die Prävalenz niedrig ist. Nehmen wir zum Beispiel an, die Inzidenz beträgt 5 %. Würde man 100 Personen nach dem Zufallsprinzip mit einem Test testen, der eine Spezifität von 95 % hat, würden im Durchschnitt 5 Personen, die eigentlich negativ sind, fälschlicherweise positiv getestet. Da 5 % der Testpersonen tatsächlich positiv sind, würden weitere 5 Personen ebenfalls korrekt positiv testen, was insgesamt 10 positive Ergebnisse ergibt. Der PPV beträgt also 50 %, ein Ergebnis, das sich nicht von dem eines Münzwurfs unterscheidet. Wenn man davon ausgeht, dass das Ergebnis eines zweiten Tests unabhängig vom ersten Test ist, erhöht sich der PPV auf 94,5 %, wenn man die Personen mit einem ersten positiven Ergebnis erneut testet, was bedeutet, dass nur 4,5 % der zweiten Tests ein falsches Ergebnis liefern würden, also im Durchschnitt weniger als ein falsches Ergebnis. ⓘ
Die Sensitivität des Testverfahrens gibt also den Anteil der positiv Getesteten zur Gesamtheit der tatsächlich Infizierten an, die Spezifität hingegen gibt den Anteil der negativ Getesteten zur Gesamtheit der tatsächlich Nicht-Infizierten an, als Formeln ausgedrückt:
- bzw. ⓘ
Für ein zuverlässiges Testergebnis werden für beide Kriterien Werte nahe 100 % angestrebt; eine hohe Sensitivität stellt sicher, dass kein Infizierter versehentlich übersehen wird; eine hohe Spezifität spricht dafür, dass kein „Fehlalarm“ (z. B. durch Kreuzreaktivität) ausgelöst wird. ⓘ
Ursachen für Testfehler
Der zeitliche Verlauf der Infektion beeinträchtigt die Genauigkeit einiger Tests. Die Proben können entnommen werden, bevor sich das Virus etablieren konnte oder nachdem der Körper begonnen hat, es zu eliminieren. Eine Überprüfung von PCR-RT-Tests im Mai 2020 ergab, dass die mittlere Wahrscheinlichkeit eines falsch-negativen Ergebnisses von 100 % an Tag 1 auf 67 % an Tag 4 abnahm. Am Tag des Auftretens der Symptome lag die Wahrscheinlichkeit bei 38 %, die 3 Tage später auf 20 % sank. ⓘ
PCR-basierter Test

Die RT-PCR ist der am häufigsten eingesetzte diagnostische Test. PCR-Tests mittels Nasopharyngealabstrich haben eine Sensitivität von 73 %, aber eine systematische Analyse der Spezifität wurde nicht durchgeführt, da es keine PCR-Studien mit einer Kontrollgruppe gibt. ⓘ
In einer Studie war die Sensitivität in der ersten Woche am höchsten (100 %), gefolgt von 89,3 %, 66,1 %, 32,1 %, 5,4 % und Null in der sechsten Woche nach Auftreten der Symptome. ⓘ
Die Sensitivität hängt auch von der Anzahl der PCR-Zyklen sowie von der Zeit und der Temperatur zwischen der Probenentnahme und der Analyse ab. Eine Zyklusschwelle von 20 Zyklen wäre ausreichend, um SARS-Cov-2 bei einer hochinfizierten Person nachzuweisen. Zyklusschwellen von mehr als 34 Zyklen führen mit zunehmender Wahrscheinlichkeit zu falsch positiven Ergebnissen außerhalb von Einrichtungen mit hoher biologischer Sicherheitsstufe. ⓘ
Am 16. Juli 2020 wies Dr. Anthony Fauci vom US CDC darauf hin, dass positive Ergebnisse von RT-PCR-Tests, die mit mehr als 35 Zyklen durchgeführt wurden, fast immer "nur tote Nukleotide" waren. Am 29. August 2020 berichtete die New York Times, dass "in drei von Beamten in Massachusetts, New York und Nevada zusammengestellten Testdatensätzen, die Zyklusschwellenwerte enthalten, ... die meisten Tests die Grenze bei 40 [Zyklen] setzen, einige bei 37" und dass die CDC die Verwendung von Zyklusschwellenwerten "für politische Entscheidungen" prüfe. Am 21. Juli 2021 wies die CDC in ihrer "Real-Time RT-PCR Diagnostic Pan: Instructions for Use", dass die Testergebnisse bei 40 Zyklen bestimmt werden sollten. ⓘ
Eine von der CDC geleitete niederländische Laboruntersuchung verglich 7 PCR-Kits. Die Testkits von BGI, R-Biopharm AG, BGI, KH Medical und Seegene zeigten eine hohe Empfindlichkeit. ⓘ
Kits mit hoher Empfindlichkeit werden für die Untersuchung von Personen ohne Symptome empfohlen, während Tests mit geringerer Empfindlichkeit für die Diagnose von Patienten mit Symptomen ausreichen. ⓘ
Das Centre for Evidence-Based Medicine (CEBM) der Universität Oxford wies auf die zunehmenden Belege dafür hin, dass "ein großer Teil der 'neuen' leichten Fälle und der Personen, die nach der Quarantäne oder der Entlassung aus dem Krankenhaus mittels RT-PCR erneut positiv getestet werden, nicht infektiös sind, sondern lediglich harmlose Viruspartikel ausscheiden, die ihr Immunsystem effizient beseitigt hat", und forderte "internationale Anstrengungen zur Standardisierung und regelmäßigen Kalibrierung der Tests". Am 7. September veröffentlichte die britische Regierung "Leitlinien für Verfahren, die in Laboratorien eingeführt werden müssen, um positive SARS-CoV-2-RNA-Ergebnisse in Zeiten niedriger Prävalenz zu gewährleisten, wenn der Vorhersagewert positiver Testergebnisse sinkt". ⓘ
Am 4. Januar 2021 gab die US FDA eine Warnung über das Risiko falscher Ergebnisse, insbesondere falscher negativer Ergebnisse, mit dem Echtzeit-RT-PCR-Test Curative SARS-Cov-2 Assay heraus. ⓘ
Isothermer Nukleinsäure-Amplifikationstest
In einer Studie wurde berichtet, dass der ID Now COVID-19-Test eine Sensitivität von 85,2 % aufweist. Abbott antwortete, dass dieses Problem durch Verzögerungen bei der Analyse verursacht worden sein könnte. Eine andere Studie lehnte den Test in ihrem klinischen Umfeld wegen dieser geringen Sensitivität ab. ⓘ
Bestätigende Tests
Die WHO empfiehlt Ländern, die nicht über Testkapazitäten verfügen, und nationalen Laboratorien mit begrenzter Erfahrung mit COVID-19, die ersten fünf positiven und die ersten zehn negativen COVID-19-Proben zur Bestätigung an eines der 16 WHO-Referenzlaboratorien zu schicken. Von den sechzehn Referenzlaboratorien befinden sich sieben in Asien, fünf in Europa, zwei in Afrika, eines in Nordamerika und eines in Australien. ⓘ
Nationale oder regionale Reaktionen
Island
Island hat die Pandemie mit aggressiver Kontaktverfolgung, Einreisebeschränkungen, Tests und Quarantäne, aber mit weniger aggressiven Abriegelungen bewältigt. ⓘ
Italien
Die Forscher testeten die gesamte Bevölkerung von Vo', dem Ort des ersten COVID-19-Todesfalls in Italien. Sie testeten etwa 3 400 Personen zweimal im Abstand von zehn Tagen. Etwa die Hälfte der positiv getesteten Personen hatte keine Symptome. Alle festgestellten Fälle wurden unter Quarantäne gestellt. Zusammen mit der Einschränkung des Reiseverkehrs in die Gemeinde wurden neue Infektionen verhindert. ⓘ
Japan
Im Gegensatz zu anderen asiatischen Ländern gab es in Japan weder eine SARS- noch eine MERS-Pandemie, so dass das PCR-Testsystem des Landes nicht weit entwickelt war. In Japan wurden anfangs vor allem Patienten mit schweren Erkrankungen und deren enge Kontaktpersonen getestet. Das japanische Expertentreffen für neuartige Coronaviren wählte Cluster-Maßnahmen, um Infektionscluster zu identifizieren. Das Expertentreffen analysierte den Ausbruch in Wuhan und ermittelte Bedingungen, die zu Clustern führen (geschlossene Räume, überfüllte Räume und enge Kontakte), und forderte die Menschen auf, diese zu meiden. ⓘ
Im Januar wurden kurz nach dem Auftreten der ersten Infektion Maßnahmen zur Ermittlung von Kontaktpersonen ergriffen. Zunächst wurden nur administrative Tests durchgeführt, bis die Versicherung am 6. März begann, PCR-Tests zu bezahlen. Private Unternehmen begannen zu testen, und das Testsystem wurde nach und nach erweitert. ⓘ
Am 3. April wurde es den positiv getesteten Personen gesetzlich gestattet, sich zu Hause oder in einem Hotel zu erholen, wenn sie asymptomatisch oder leicht erkrankt waren, wodurch der Mangel an Krankenhausbetten beendet wurde. Die erste Welle (aus China) konnte eingedämmt werden, aber eine zweite Welle (verursacht durch Rückkehrer aus Europa und den USA) Mitte März führte zu einer Ausbreitung der Infektion im April. Am 7. April wurde in Japan der Notstand ausgerufen (weniger streng als eine Abriegelung, da keine Städte gesperrt oder Ausflüge eingeschränkt wurden). Am 13. Mai wurden Antigen-Testkits von der Versicherung übernommen und mit einem PCR-Test zur Diagnose kombiniert. ⓘ
Die Zahl der PCR-Tests pro Kopf blieb in Japan weitaus geringer als in einigen anderen Ländern, obwohl die Rate der positiven Tests niedriger war. Im März wurde eine überhöhte Sterblichkeit beobachtet. Auf dem Expertentreffen wurde festgestellt: "Das japanische Gesundheitssystem führt ursprünglich eine Überwachung der Lungenentzündung durch, wodurch die meisten schwer kranken Patienten, die eine Lungenentzündung entwickeln, erkannt werden können. In Japan gibt es eine große Anzahl von Computertomographen, die in kleinen Krankenhäusern im ganzen Land verteilt sind, so dass Lungenentzündungspatienten nur selten übersehen werden. In dieser Hinsicht erfüllt es die gleichen Standards wie andere Länder, die hauptsächlich PCR-Tests durchführen. Die Gruppe empfahl, für die Diagnose die Daten von CT-Scans und die Befunde von Ärzten zu verwenden. Auf dem Kreuzfahrtschiff Diamond Princess wurden viele Personen, die zunächst negativ getestet wurden, später positiv getestet. Bei der Hälfte der Coronavirus-Positiven, die keine oder nur geringe Symptome aufwiesen, wurde auf den CT-Scans eine Lungenentzündung festgestellt, und das CT-Bild zeigte einen für die Infektion charakteristischen Milchglasschatten. ⓘ
Bis zum 18. Juli wurden in Japan täglich etwa 32.000 PCR-Tests durchgeführt, mehr als das Dreifache der 10.000 Fälle vom April. Rechnet man den Antigentest hinzu, liegt die Zahl bei 58.000. Die Zahl der Tests pro 1.000 Personen ist in den Vereinigten Staaten etwa 27 Mal so hoch wie in Japan, im Vereinigten Königreich 20 Mal, in Italien 8 Mal und in Südkorea doppelt so hoch (Stand: 26. Juli). Die Zahl der mit dem Coronavirus infizierten Personen und der stationär behandelten Patienten ist im Juli gestiegen, die Zahl der schweren Fälle jedoch nicht. Es wird vermutet, dass dies auf die ordnungsgemäße Untersuchung der Infizierten im Juli im Vergleich zum April zurückzuführen ist. Im April konnte die Zahl der Tests nicht mit dem Anstieg der Zahl der Infizierten Schritt halten, und die Teststandards waren streng, so dass die Rate der positiven Tests in der Spitze über 30 % lag. Das bedeutet, dass es eine ganze Reihe von Fällen gab, in denen die Infizierten nicht PCR-getestet wurden. Es wird vermutet, dass schwere Fälle bevorzugt getestet wurden, obwohl es während der ersten Welle viele leichte Fälle und asymptomatische Träger vor allem unter jungen Menschen gab. Mit anderen Worten: Durch den Ausbau des Testsystems konnte die tatsächliche Infektionssituation viel besser erfasst werden als zuvor. Ende Juli waren die Unterbringungsmöglichkeiten für leichte und asymptomatische Träger voll, und die Behörden forderten die Krankenhäuser auf, Betten für leichte Fälle bereitzustellen. Aufgrund der Belegung der Krankenhausbetten durch Patienten mit leichten Symptomen wurde es jedoch schwierig, Patienten mit anderen Krankheiten zu behandeln und das System der Intensivstation einschließlich des Personals aufrechtzuerhalten. ⓘ
Russland
Am 27. April 2020 wurden in Russland 3 Millionen Menschen getestet und 183.000 positive Ergebnisse erzielt. Am 28. April erklärte Anna Popowa, Leiterin des Föderalen Dienstes für die Überwachung im Gesundheitswesen (Roszdravnadzor), dass 506 Labors Tests durchführten, dass 45 % der positiv getesteten Personen keine Symptome hatten, dass 5 % der Patienten eine schwere Form aufwiesen und dass 40 % der Infektionen von Familienmitgliedern stammten. Der Krankheitsverlauf verbesserte sich von sechs Tagen bis zu einem Tag nach Auftreten der Symptome. Bei 3.200 Moskauer Ärzten wurden Antikörpertests durchgeführt, die eine Immunität von 20 % ergaben. ⓘ
Singapur
Durch die Rückverfolgung von Kontaktpersonen, Einreisebeschränkungen, Tests und Quarantäne hat Singapur die anfängliche Ausbreitung ohne vollständige Abriegelung eingedämmt. ⓘ
Slowakei
Ende Oktober 2020 wurden in der Slowakei an einem Wochenende 3,62 Millionen Menschen getestet. Von den 5,4 Millionen Einwohnern, die 67 % der Gesamtbevölkerung (oder 82 % der erwachsenen Bevölkerung) ausmachen, wurden 38 359 positiv getestet, was 1,06 % der Getesteten entspricht. Die Regierung war der Ansicht, dass der Massentest wesentlich zur Kontrolle des Virus und zur Vermeidung einer Abriegelung beitragen würde, und wird die Übung möglicherweise zu einem späteren Zeitpunkt wiederholen. ⓘ
Südkorea
Südkoreas breit angelegter Testansatz trug zur Eindämmung der Ausbreitung bei. Anfang der 2000er Jahre baute die südkoreanische Regierung über mehrere Jahre hinweg Testkapazitäten auf, die größtenteils in Labors des privaten Sektors untergebracht waren. ⓘ
Die Regierung nutzte das System der Einwohnerregistrierungsnummern (RRN). Die Behörden mobilisierten junge Männer, die für den Militärdienst in Frage kamen, als Sozialdienstleistende, Sicherheitsbeamte und Ärzte im öffentlichen Gesundheitswesen. Die Ärzte des öffentlichen Gesundheitswesens wurden vor allem in öffentlichen Gesundheitszentren und Behandlungszentren eingesetzt, in denen leicht erkrankte Patienten untergebracht waren. Sie führten PCR-Tests durch und betreuten leichte Patienten. Sozialdienstmitarbeiter arbeiteten in Apotheken, um Personalengpässe auszugleichen. Mit 10 000 PCR-Tests pro eine Million Einwohner hatte Korea am 13. April die weltweit höchste Zahl an PCR-Tests, die bis Mitte Juni auf 20 000 anstieg. Siebenundzwanzig koreanische Unternehmen exportierten im März Testkits im Wert von 48,6 Millionen Dollar und wurden von mehr als 120 Ländern um die Bereitstellung von Testkits oder humanitäre Hilfe gebeten. Die koreanischen Behörden richteten ein Behandlungszentrum ein, um Patienten mit asymptomatischen und leichteren Erkrankungen in einer Einrichtung zu isolieren und zu behandeln, damit Krankenhausbetten für schwerere Erkrankungen frei werden. ⓘ
Die Zentren wurden hauptsächlich in nationalen Einrichtungen und Schulungszentren von Unternehmen eingerichtet. Nach dem Scheitern der koreanischen MERS-Quarantäne im Mai 2015 war Korea besser auf COVID-19 vorbereitet als Länder, die nicht mit dieser Pandemie konfrontiert waren. Dann erlaubte Präsidentin Park Geun-hye 2016 dem koreanischen CDC, Tests für Infektionskrankheiten im privaten Sektor zuzulassen. Korea verfügte bereits über ein System, um Patienten mit Infektionskrankheiten zu isolieren, zu testen und getrennt von anderen zu behandeln. Patienten mit Atemwegserkrankungen, die keine epidemiologische Relevanz hatten, wurden im Nationalen Krankenhaus behandelt, während Patienten mit epidemiologischer Relevanz in ausgewählten Kliniken behandelt wurden. ⓘ
Korea führte ein groß angelegtes Drive-Through/Walk-Through"-Testprogramm ein. Die häufigste Methode war jedoch die "mobile Untersuchung". In Daegu City wurden 54 % der Proben bis zum 23. März zu Hause oder im Krankenhaus entnommen. Durch die Probenentnahme von Tür zu Tür wurde das Risiko vermieden, dass möglicherweise infizierte Patienten auf Reisen gehen, aber es wurde zusätzliches Personal benötigt. Korea löste das Problem durch die Einstellung von mehr als 2.700 Ärzten der öffentlichen Krankenversicherung. ⓘ
Die Regierung gab über das KCDC persönliche Informationen ohne Zustimmung der Patienten an die Öffentlichkeit weiter. Die Behörden nutzten die digitale Überwachung, um eine mögliche Ausbreitung zu verfolgen. ⓘ
Taiwan
Krankenversicherungs- und nationale Ausweisnummern wurden zur Rückverfolgung von Kontakten verwendet. ⓘ
Vereinigte Arabische Emirate
Im Januar 2021 gerieten die COVID-19-Testergebnisse der Vereinigten Arabischen Emirate in die Kritik, da Dänemark die Flüge der Emirate für fünf Tage aussetzte. Das europäische Land erklärte, es habe die Flüge aus den VAE gesperrt, weil der Verdacht auf Unregelmäßigkeiten im Testverfahren in dem Golfstaat gewachsen sei. Der dänische Verkehrsminister Benny Engelbrecht erklärte, man nehme sich Zeit, um sicherzustellen, dass die negativen Tests bei Reisenden aus den Emiraten tatsächlich ordnungsgemäß durchgeführt worden seien. ⓘ
Vereinigte Staaten
Staat New York
Die Bekämpfungsmaßnahmen des Bundesstaates New York bestanden aus PCR-Tests, Hausbesuchen und der Stärkung des Gesundheitssystems. Am 29. Februar, noch vor dem ersten Fall, erlaubte der Staat Tests im Wordsworth Center. Es gelang, die CDC davon zu überzeugen, Tests in staatlichen Labors zuzulassen, und die FDA, ein Testkit zu genehmigen. Ab dem 13. März führte der Staat täglich mehr als 1.000 Tests durch, die am 19. März auf 10.000/Tag anstiegen. Im April lag die Zahl bei über 20.000. Viele Menschen standen in den Krankenhäusern Schlange, um sich testen zu lassen. Am 21. März wiesen die Gesundheitsbehörden der Stadt New York die medizinischen Dienstleister an, nur diejenigen zu testen, die das Krankenhaus betraten, weil sie keine PSA hatten. ⓘ
USS Theodore Roosevelt
Nach einem Ausbruch wurden 94 % der 4.800 Besatzungsmitglieder des Flugzeugträgers getestet. Etwa 60 Prozent der über 600 positiv getesteten Matrosen waren asymptomatisch. Fünf infizierte Matrosen, die die Quarantäne überstanden hatten, entwickelten anschließend grippeähnliche Symptome und wurden erneut positiv getestet. ⓘ
Nevada
Im Jahr 2020 erhielt Nevada eine Spende von 250.000 Covid-Testkits, die von Chinas führendem Genetikunternehmen, der BGI Group, hergestellt wurden. Die Gruppe 42, ein in den Vereinigten Arabischen Emiraten ansässiges Unternehmen im Besitz von Tahnoun bin Zayed Al Nahyan, hatte sich mit der BGI Group zusammengetan, um die Testkits nach Nevada zu liefern. Das US-Ministerium für Innere Sicherheit und das Außenministerium warnten die Krankenhäuser in Nevada jedoch davor, die in China hergestellten Testkits zu verwenden, da es Bedenken hinsichtlich der Beteiligung der chinesischen Regierung, der Genauigkeit der Tests und der Privatsphäre der Patienten gab. ⓘ
Verspätete Tests
Ein Mangel an geschulten medizinischen Laborwissenschaftlern, Testreagenzien, Analysegeräten, Transportmitteln und PSA in Verbindung mit einer hohen Nachfrage hatte die Verfügbarkeit von Tests zunächst eingeschränkt und zu erheblich längeren Durchlaufzeiten geführt. ⓘ
Teststatistiken nach Ländern
Die Teststrategien variieren von Land zu Land und im Laufe der Zeit, wobei einige Länder sehr breit testen, während andere sich zeitweise auf die Untersuchung von Schwerkranken beschränken. In einem Land, in dem nur Personen mit Symptomen getestet werden, ist die Zahl der "Bestätigten / Getesteten" höher als in einem Land, das auch andere Personen testet. Wenn zwei Länder in jeder Hinsicht gleich sind, einschließlich der Personen, die sie testen, wird das Land, das mehr Personen testet, eine höhere "Bestätigte/Bevölkerung" haben. Studien haben auch ergeben, dass Länder, die im Verhältnis zur Zahl der Todesfälle mehr testen, niedrigere geschätzte Todesfallraten und eine jüngere Altersverteilung der Fälle aufweisen. ⓘ
| Land oder Region | Datum | Getestet | Einheiten | Bestätigte (Fälle) |
Bestätigt / getestet, % |
Getestet / Bevölkerung, % |
Bestätigt / Bevölkerung, % |
Ref. ⓘ |
|---|---|---|---|---|---|---|---|---|
| 17 Dez 2020 | 154,767 | Proben | 49,621 | 32.1 | 0.40 | 0.13 | ||
| 18 Feb 2021 | 428,654 | Proben | 96,838 | 22.6 | 15.0 | 3.4 | ||
| 2 Nov 2020 | 230,553 | Proben | 58,574 | 25.4 | 0.53 | 0.13 | ||
| 23. Februar 2022 | 300,307 | Proben | 37,958 | 12.6 | 387 | 49.0 | ||
| 2 Feb 2021 | 399,228 | Proben | 20,981 | 5.3 | 1.3 | 0.067 | ||
| 6. März 2021 | 15,268 | Proben | 832 | 5.4 | 15.9 | 0.86 | ||
| 16 Apr 2022 | 35,716,069 | Proben | 9,060,495 | 25.4 | 78.3 | 20.0 | ||
| 29 Mai 2022 | 3,099,602 | Proben | 422,963 | 13.6 | 105 | 14.3 | ||
| 15 Jul 2022 | 74,999,209 | Proben | 8,687,125 | 11.6 | 299 | 34.6 | ||
| 15 Jul 2022 | 191,905,533 | Proben | 4,632,173 | 2.4 | 2,156 | 52.0 | ||
| 11 Mai 2022 | 6,838,458 | Proben | 792,638 | 11.6 | 69.1 | 8.0 | ||
| 17. Juli 2022 | 245,265 | Proben | 36,454 | 14.9 | 63.6 | 9.5 | ||
| 16. Juli 2022 | 10,110,089 | Proben | 647,935 | 6.4 | 644 | 41.3 | ||
| 24 Jul 2021 | 7,417,714 | Proben | 1,151,644 | 15.5 | 4.5 | 0.70 | ||
| 17. Juli 2022 | 716,572 | Proben | 87,754 | 12.2 | 250 | 30.6 | ||
| 9. Mai 2022 | 13,217,569 | Proben | 982,809 | 7.4 | 139 | 10.4 | ||
| 14. Juli 2022 | 34,784,155 | Proben | 4,349,050 | 12.5 | 302 | 37.8 | ||
| 8 Juni 2022 | 572,900 | Proben | 60,694 | 10.6 | 140 | 14.9 | ||
| 4 Mai 2021 | 595,112 | Proben | 7,884 | 1.3 | 5.1 | 0.067 | ||
| 28 Feb 2022 | 1,736,168 | Proben | 12,702 | 0.73 | 234 | 1.71 | ||
| 5 Juni 2022 | 4,358,669 | Fälle | 910,228 | 20.9 | 38.1 | 8.0 | ||
| 13 Jul 2022 | 1,799,158 | Proben | 380,211 | 21.1 | 52.6 | 11.1 | ||
| 11 Jan 2022 | 2,026,898 | 232,432 | 11.5 | 89.9 | 10.3 | |||
| 19 Feb 2021 | 23,561,497 | Proben | 10,081,676 | 42.8 | 11.2 | 4.8 | ||
| 2 Aug 2021 | 153,804 | Proben | 338 | 0.22 | 33.5 | 0.074 | ||
| 15 Jul 2022 | 10,173,151 | Proben | 1,183,877 | 11.6 | 146 | 17.0 | ||
| 4 Mär 2021 | 158,777 | Proben | 12,123 | 7.6 | 0.76 | 0.058 | ||
| 5 Jan 2021 | 90,019 | 884 | 0.98 | 0.76 | 0.0074 | |||
| 1 Aug 2021 | 1,812,706 | 77,914 | 4.3 | 11.2 | 0.48 | |||
| 18 Feb 2021 | 942,685 | Proben | 32,681 | 3.5 | 3.6 | 0.12 | ||
| 9 Jul 2022 | 63,036,094 | Proben | 3,978,338 | 6.3 | 166 | 10.5 | ||
| 2 Mär 2021 | 99,027 | Proben | 4,020 | 4.1 | 0.72 | 0.029 | ||
| 15 Jul 2022 | 41,282,462 | Proben | 4,122,401 | 10.0 | 216 | 21.6 | ||
| 31 Jul 2020 | 160,000,000 | Fälle | 87,655 | 0.055 | 11.1 | 0.0061 | ||
| 14. Juli 2022 | 35,781,769 | Proben | 6,223,497 | 17.4 | 74.1 | 12.9 | ||
| 2. November 2021 | 2,575,363 | Proben | 561,054 | 21.8 | 51.5 | 11.2 | ||
| 18. Juli 2022 | 5,002,475 | Fälle | 1,169,342 | 23.4 | 123 | 28.7 | ||
| 18. Juli 2022 | 14,005,144 | Proben | 1,106,930 | 7.9 | 124 | 9.8 | ||
| 3. Juli 2022 | 25,689,321 | Proben | 530,510 | 2.1 | 2,976 | 61.5 | ||
| 14. Juli 2022 | 21,963,566 | Proben | 3,949,492 | 18.0 | 205 | 36.9 | ||
| 18. Juli 2022 | 66,407,155 | Proben | 3,209,307 | 4.8 | 1,140 | 55.1 | ||
| 28 Apr 2022 | 305,941 | 15,631 | 5.1 | 33.2 | 1.7 | |||
| 20 Jun 2022 | 209,803 | Fälle | 14,821 | 7.1 | 293 | 20.7 | ||
| 12 Jul 2022 | 3,548,349 | Proben | 620,237 | 17.5 | 32.6 | 5.7 | ||
| 28 Feb 2021 | 124,838 | 25,961 | 20.8 | 0.14 | 0.029 | |||
| 23 Jul 2021 | 1,627,189 | Proben | 480,720 | 29.5 | 9.5 | 2.8 | ||
| 23 Jul 2021 | 3,137,519 | Proben | 283,947 | 9.1 | 3.1 | 0.28 | ||
| 18 Mär 2022 | 1,847,861 | Proben | 161,052 | 8.7 | 28.5 | 2.5 | ||
| 14. Juli 2022 | 349,765 | 16,584 | 4.7 | 26.7 | 1.3 | |||
| 19 Jul 2022 | 3,431,425 | Proben | 584,489 | 17.0 | 258 | 44.0 | ||
| 8 Dez 2021 | 415,110 | 49,253 | 11.9 | 36.5 | 4.3 | |||
| 24 Jun 2021 | 2,981,185 | Proben | 278,446 | 9.3 | 2.6 | 0.24 | ||
| 27 Feb 2022 | 774,000 | Proben | 34,237 | 4.4 | 1,493 | 65.7 | ||
| 18. Juli 2022 | 592,054 | Proben | 66,975 | 11.3 | 66.0 | 7.5 | ||
| 14 Jan 2022 | 9,042,453 | Proben | 371,135 | 4.1 | 163 | 6.7 | ||
| 15 Mai 2022 | 272,417,258 | Proben | 29,183,646 | 10.7 | 417 | 44.7 | ||
| 23 Jul 2021 | 958,807 | Proben | 25,325 | 2.6 | 3.1 | 0.082 | ||
| 15 Feb 2021 | 43,217 | Proben | 4,469 | 10.3 | 2.0 | 0.21 | ||
| 3. November 2021 | 4,888,787 | Proben | 732,965 | 15.0 | 132 | 19.7 | ||
| 7. Juli 2021 | 65,247,345 | Proben | 3,733,519 | 5.7 | 77.8 | 4.5 | ||
| 3. Juli 2021 | 1,305,749 | Proben | 96,708 | 7.4 | 4.2 | 0.31 | ||
| 10 Jul 2022 | 86,634,526 | Proben | 3,843,142 | 4.4 | 805 | 35.7 | ||
| 30 Jan 2022 | 164,573 | Proben | 10,662 | 6.5 | 293 | 19.0 | ||
| 11. Mai 2021 | 28,684 | 161 | 0.56 | 25.7 | 0.14 | |||
| 12 Jul 2022 | 5,033,330 | Proben | 963,117 | 19.1 | 29.2 | 5.6 | ||
| 21. Juli 2021 | 494,898 | Proben | 24,878 | 5.0 | 3.8 | 0.19 | ||
| 7. Juli 2022 | 145,231 | 8,400 | 5.8 | 7.7 | 0.45 | |||
| 15 Jun 2022 | 648,569 | Fälle | 66,129 | 10.2 | 82.5 | 8.4 | ||
| 6 Jul 2022 | 210,836 | Fälle | 31,980 | 15.2 | 1.8 | 0.28 | ||
| 26 Nov 2021 | 1,133,782 | Proben | 377,859 | 33.3 | 11.8 | 3.9 | ||
| 10 Mai 2022 | 11,394,556 | Proben | 1,909,948 | 16.8 | 118 | 19.8 | ||
| 14. Juli 2022 | 1,979,580 | Proben | 199,611 | 10.1 | 543 | 54.8 | ||
| 8. Juli 2022 | 866,177,937 | Proben | 43,585,554 | 5.0 | 63 | 31.7 | ||
| Fälle | ||||||||
| 31. Mai 2022 | 52,269,202 | Proben | 7,232,268 | 13.8 | 62.8 | 8.7 | ||
| 13 Jul 2022 | 18,904,478 | Proben | 2,393,726 | 12.7 | 47.0 | 6.0 | ||
| 13 Jul 2022 | 12,466,865 | Proben | 1,628,745 | 13.1 | 253 | 33.1 | ||
| 17. Januar 2022 | 41,373,364 | Proben | 1,792,137 | 4.3 | 451 | 19.5 | ||
| 20 Jul 2022 | 233,898,775 | Proben | 20,385,814 | 8.7 | 388 | 33.8 | ||
| 3. März 2021 | 429,177 | Proben | 33,285 | 7.8 | 1.6 | 0.13 | ||
| 12 Jul 2022 | 1,137,392 | Proben | 144,213 | 12.7 | 41.7 | 5.3 | ||
| 1 Mär 2021 | 8,487,288 | 432,773 | 5.1 | 6.7 | 0.34 | |||
| 6 Jun 2021 | 7,407,053 | Proben | 739,847 | 10.0 | 69.5 | 6.9 | ||
| 28. Mai 2021 | 11,575,012 | Proben | 385,144 | 3.3 | 62.1 | 2.1 | ||
| 5 Mär 2021 | 1,322,806 | Proben | 107,729 | 8.1 | 2.8 | 0.23 | ||
| 31. Mai 2021 | 611,357 | Fälle | 107,410 | 17.6 | 33.8 | 5.9 | ||
| 9 Mär 2022 | 7,754,247 | Proben | 624,573 | 8.1 | 181 | 14.6 | ||
| 10 Feb 2021 | 695,415 | Proben | 85,253 | 12.3 | 10.7 | 1.3 | ||
| 1 Mär 2021 | 114,030 | Fälle | 45 | 0.039 | 1.6 | 0.00063 | ||
| 5 Sep 2021 | 3,630,095 | Proben | 144,518 | 4.0 | 189 | 7.5 | ||
| 14 Jun 2021 | 4,599,186 | Proben | 542,649 | 11.8 | 67.4 | 8.0 | ||
| 30 Mär 2022 | 431,221 | 32,910 | 7.6 | 21.5 | 1.6 | |||
| 17 Jul 2021 | 128,246 | 5,396 | 4.2 | 2.5 | 0.11 | |||
| 14 Apr 2022 | 2,578,215 | Proben | 501,862 | 19.5 | 37.6 | 7.3 | ||
| 18. Juli 2022 | 8,748,975 | Proben | 1,075,695 | 12.3 | 313 | 38.5 | ||
| 12 Mai 2022 | 4,248,188 | Proben | 244,182 | 5.7 | 679 | 39.0 | ||
| 19 Feb 2021 | 119,608 | Fälle | 19,831 | 16.6 | 0.46 | 0.076 | ||
| 15 Jul 2022 | 596,813 | Proben | 86,900 | 14.6 | 3.1 | 0.45 | ||
| 7. September 2021 | 23,705,425 | Fälle | 1,880,734 | 7.9 | 72.3 | 5.7 | ||
| 13 Mär 2022 | 2,216,560 | Proben | 174,658 | 7.9 | 398 | 31.3 | ||
| 7. Juli 2021 | 322,504 | Proben | 14,449 | 4.5 | 1.6 | 0.071 | ||
| 8 Sep 2021 | 1,211,456 | Proben | 36,606 | 3.0 | 245 | 7.4 | ||
| 16 Apr 2021 | 268,093 | 18,103 | 6.8 | 6.1 | 0.41 | |||
| 22 Nov 2020 | 289,552 | Proben | 494 | 0.17 | 22.9 | 0.039 | ||
| 15 Okt 2021 | 10,503,678 | Fälle | 3,749,860 | 35.7 | 8.2 | 2.9 | ||
| 20 Apr 2022 | 3,213,594 | Proben | 516,864 | 16.1 | 122 | 19.6 | ||
| 10 Jul 2021 | 3,354,200 | Fälle | 136,053 | 4.1 | 100 | 4.1 | ||
| 10. Mai 2021 | 394,388 | Proben | 98,449 | 25.0 | 62.5 | 15.6 | ||
| 13 Jul 2022 | 13,313,359 | Fälle | 1,244,892 | 9.4 | 36.1 | 3.4 | ||
| 22. Juli 2021 | 688,570 | Proben | 105,866 | 15.4 | 2.2 | 0.34 | ||
| 16. September 2021 | 4,047,680 | Proben | 440,741 | 10.9 | 7.4 | 0.81 | ||
| 4. Juli 2022 | 1,062,663 | Proben | 166,229 | 15.6 | 38.7 | 6.1 | ||
| 7 Jun 2022 | 5,719,524 | Proben | 979,213 | 17.1 | 20.4 | 3.5 | ||
| 6 Jul 2021 | 14,526,293 | Fälle | 1,692,834 | 11.7 | 83.4 | 9.7 | ||
| 3 Sep 2021 | 41,962 | Proben | 136 | 0.32 | 15.7 | 0.050 | ||
| 17. Juli 2022 | 7,339,041 | Proben | 1,498,402 | 20.4 | 147 | 30.1 | ||
| 22 Feb 2021 | 79,321 | Fälle | 4,740 | 6.0 | 0.35 | 0.021 | ||
| 28 Feb 2021 | 1,544,008 | Proben | 155,657 | 10.1 | 0.75 | 0.076 | ||
| 25 Nov 2020 | 16,914 | Fälle | 0 | 0 | 0.066 | 0 | ||
| 1. Juli 2021 | 881,870 | Proben | 155,689 | 17.7 | 42.5 | 7.5 | ||
| 12 Jul 2022 | 7,096,998 | Proben | 103,034 | 1.5 | 2,177 | 31.6 | ||
| 20 Jan 2022 | 9,811,888 | Proben | 554,778 | 5.7 | 183 | 10.3 | ||
| 28 Okt 2020 | 509,959 | Proben | 114,434 | 22.4 | 11.0 | 2.5 | ||
| 5 Mär 2021 | 9,173,593 | Proben | 588,728 | 6.4 | 4.2 | 0.27 | ||
| 5 Feb 2022 | 3,078,533 | Proben | 574,105 | 18.6 | 60.9 | 11.4 | ||
| 8. Juli 2022 | 6,637,861 | Proben | 932,710 | 14.1 | 159 | 22.3 | ||
| 17. Februar 2021 | 47,490 | Fälle | 961 | 2.0 | 0.53 | 0.011 | ||
| 27. März 2022 | 2,609,819 | Proben | 647,950 | 24.8 | 36.6 | 9.1 | ||
| 26 Jun 2022 | 31,403,367 | Proben | 3,616,929 | 11.5 | 95.7 | 11.0 | ||
| 14. Juli 2022 | 31,081,194 | Proben | 3,725,382 | 12.0 | 30.8 | 3.7 | ||
| 27 Apr 2022 | 36,064,311 | Proben | 5,993,861 | 16.6 | 94.0 | 15.6 | ||
| 5 Jan 2022 | 27,515,490 | Proben | 1,499,976 | 5.5 | 268 | 14.6 | ||
| 16. Juli 2022 | 3,699,239 | Fälle | 393,834 | 10.6 | 128 | 13.7 | ||
| 29 Jan 2021 | 5,405,393 | Proben | 724,250 | 13.4 | 27.9 | 3.7 | ||
| 6 Jun 2022 | 295,542,733 | Proben | 18,358,459 | 6.2 | 201 | 12.5 | ||
| 6 Okt 2021 | 2,885,812 | Proben | 98,209 | 3.4 | 22.3 | 0.76 | ||
| 26 Aug 2021 | 30,231 | Fälle | 995 | 3.3 | 57.6 | 1.9 | ||
| 19 Jul 2022 | 202,420 | Proben | 27,533 | 13.6 | 111.3 | 15.1 | ||
| 12 Jul 2022 | 109,009 | Fälle | 9,183 | 8.4 | 98.9 | 8.3 | ||
| 18. Juli 2022 | 165,252 | Proben | 19,253 | 11.7 | 483 | 56.2 | ||
| 26 Apr 2022 | 41,849,069 | Proben | 753,632 | 1.8 | 120 | 2.2 | ||
| 12 Jul 2021 | 624,502 | Proben | 46,509 | 7.4 | 3.9 | 0.29 | ||
| 15 Jul 2022 | 10,026,607 | Fälle | 2,052,116 | 20.5 | 144 | 29.5 | ||
| 3 Aug 2021 | 16,206,203 | Proben | 65,315 | 0.40 | 284 | 1.1 | ||
| 17. Juli 2022 | 7,201,031 | Proben | 1,806,246 | 25.1 | 132 | 33.1 | ||
| 17. Juli 2022 | 2,694,213 | Proben | 1,060,783 | 39.4 | 129 | 50.7 | ||
| 24. Mai 2021 | 11,378,282 | Fälle | 1,637,848 | 14.4 | 19.2 | 2.8 | ||
| 1 Mär 2021 | 6,592,010 | Proben | 90,029 | 1.4 | 12.7 | 0.17 | ||
| 26. Mai 2021 | 164,472 | 10,688 | 6.5 | 1.3 | 0.084 | |||
| 1. Juli 2021 | 54,128,524 | Proben | 3,821,305 | 7.1 | 116 | 8.2 | ||
| 30. März 2021 | 2,384,745 | Proben | 93,128 | 3.9 | 10.9 | 0.43 | ||
| 7 Jan 2021 | 158,804 | Proben | 23,316 | 14.7 | 0.36 | 0.053 | ||
| 24. Mai 2021 | 9,996,795 | Proben | 1,074,751 | 10.8 | 96.8 | 10.4 | ||
| 19 Jul 2022 | 22,203,108 | Proben | 3,911,499 | 17.6 | 258 | 45.4 | ||
| 19 Jul 2022 | 22,179,496 | Proben | 4,309,904 | 19.43 | 94.0 | 18.259 | ||
| 18 Nov 2020 | 3,880 | 509 | 13.1 | 0.0065 | 0.00085 | |||
| 4 Mär 2021 | 1,579,597 | Fälle | 26,162 | 1.7 | 2.3 | 0.038 | ||
| 15 Jul 2022 | 761,320 | 37,776 | 5.0 | 8.8 | 0.44 | |||
| 3 Jan 2022 | 512,730 | Fälle | 92,997 | 18.1 | 37.6 | 6.8 | ||
| 23 Aug 2021 | 2,893,625 | Proben | 703,732 | 24.3 | 24.5 | 6.0 | ||
| 2 Jul 2021 | 61,236,294 | Proben | 5,435,831 | 8.9 | 73.6 | 6.5 | ||
| 11 Feb 2021 | 852,444 | Proben | 39,979 | 4.7 | 1.9 | 0.087 | ||
| 24. November 2021 | 15,648,456 | Proben | 3,367,461 | 21.5 | 37.2 | 8.0 | ||
| 15 Jul 2022 | 173,570,214 | Proben | 970,586 | 0.56 | 1,808 | 10.1 | ||
| 19 Mai 2022 | 522,526,476 | Proben | 22,232,377 | 4.3 | 774 | 32.9 | ||
| 13 Jul 2022 | 921,423,930 | Proben | 88,932,937 | 9.7 | 278 | 26.9 | ||
| 16 Apr 2022 | 6,089,116 | Proben | 895,592 | 14.7 | 175 | 25.8 | ||
| 7 Sep 2020 | 2,630,000 | Proben | 43,975 | 1.7 | 7.7 | 0.13 | ||
| 30. März 2021 | 3,179,074 | Proben | 159,149 | 5.0 | 11.0 | 0.55 | ||
| 19 Juni 2022 | 45,253,655 | Proben | 10,737,646 | 23.7 | 45.8 | 10.9 | ||
| 10 Mär 2022 | 3,301,860 | Proben | 314,850 | 9.5 | 19.0 | 1.8 | ||
| 14. Juli 2022 | 2,424,666 | Proben | 256,083 | 10.6 | 16.3 | 1.7 | ||
Einzelne Verfahren
Antigen-Schnelltests
Einsatz als Selbsttest


Antigen-Schnelltests können prinzipiell auch von ungeschultem Personal in Eigenanwendung benutzt werden. Die Selbstanwendung wurde jedoch lange Zeit nicht zugelassen, weil erst nachgewiesen werden musste, dass „die Probenentnahme und -auswertung entsprechend einfach“ ist und somit von jedermann verlässlich durchgeführt werden kann. Mittlerweile sind Schnelltests zur Eigenanwendung im Einzelhandel erhältlich. ⓘ
Der Ablauf eines nasalen Selbsttests erfolgt in folgenden Schritten:
- Vorbereitung: Desinfektion der Hände, Entnahme des Tests
- Probenentnahme: Das Wattestäbchen wird mehrere Zentimeter in die Nase eingeführt und für einige Sekunden gedreht. (Andere Testformen siehe oben)
- Entwicklung: Das Stäbchen wird in das Reagenzröhrchen mit der Trägerflüssigkeit gesteckt, gedreht und gequetscht (bei Spuck-Tests wird der Speichel mit der Flüssigkeit gemischt). Damit wird entnommenes Material in die Trägerflüssigkeit übertragen. Daraufhin wird das Röhrchen verschlossen und geschüttelt.
- Testdurchführung: Die Flüssigkeitsprobe wird in das Loch am Ende des Testkits gegeben (siehe Bild). Sie zieht daraufhin langsam auf dem Trägerpapier nach oben.
- Ablesung: Erscheint dort nach 15 Minuten nur der Kontrollstreifen (C-Strich), ist der Test negativ. Erscheint der zweite Teststreifen (T-Strich) – auch nur schwach – ist er positiv. Erscheint gar kein Streifen oder nur der T-Strich, ist er ungültig und muss wiederholt werden. ⓘ
Antikörper-Tests
Aussagekraft
Falls ein bestimmter Antikörper an mehr als einem Antigen bindet, handelt es sich um eine Kreuzreaktivität, die zu falsch positiven Testergebnissen führt, da mehr als das eigentliche Antigen reagiert. Als Antigene von SARS-CoV-2 sind die im Abschnitt Merkmale beschriebenen Strukturen geeignet, beispielsweise das Nukleokapsidprotein (N) oder das Spikeprotein (S) als Ganzes bzw. alternativ die S1- und S2-Domäne. In der Literatur werden mögliche Kreuzreaktionen zu den Coronaviren SARS-CoV-1, MERS-CoV, HCoV-HKU1, HCoV-OC43, HCoV-NL63, HCoV-229E sowie bei Katzen und Schweinen vorkommende Coronaviren genannt. ⓘ
Für die Methodenvalidierung serologischer Nachweise wird als Referenzmethode (auch als Goldstandard bezeichnet) der Neutralisationstest (NT), im Detail der Plaque-Reduktions-Neutralisationstest (PRNT) verwendet. Für die als Proben eingesetzten Patientenseren gilt, dass bei den Patienten zuvor das SARS-CoV-2 durch PCR nachgewiesen wurde bzw. bei den Kontrollen die anderen Coronaviren oder weiteren Viren. Für die Aussagekraft der Spezifität ist weiterhin wichtig, dass Proben mit Antikörpern gegen viele verschiedene Viren getestet werden. ⓘ
Weitere Methoden
Genomanalyse
Laboratorien mit Ausstattung für eine Genomanalyse (DNA-Sequenzierung des Genoms), also einem Sequenzierautomaten, können SARS-CoV-2 auch auf diese Weise identifizieren. Vollständige Genomanalysen von SARS-CoV-2-Isolaten zum Vergleich sind beispielsweise in der Gendatenbank des National Center for Biotechnology Information (NCBI) oder über die GISAID-Plattform verfügbar (vergleiche Abschnitt Molekulargenetik und Phylogenetik). ⓘ
TMA
Die TMA ist eine Methode zur Detektion von RNS- und DNS-Sequenzen auf der Basis einer autokatalytischen Amplifikation. Sie steht seit 2020 für die SARS-CoV-2-Analytik zur Verfügung und ist einfacher handhabbar und liefert schneller Ergebnisse als die PCR. ⓘ
Kartuschentest
Bei einem Kartuschensystem wird ein technisch aufwändiges, aber dennoch von den Größenabmessungen transportables Gerät (englisch analyzer) verwendet, in dem eine dafür konstruierte Kartusche (englisch cartridge) eingesetzt wird. Die Kartusche wird zuvor mit dem Probenmaterial, z. B. dem Abstrichtupfer bestückt, weitere Chemikalien und biologische Arbeitsstoffe für die Probevorbereitung und die Analyse sind in der Kartusche enthalten. Die für den Einmalgebrauch konzipierte Kartusche verkürzt die Dauer bis zum Vorliegen des Testergebnisses und bietet für den Benutzer den Vorteil, den Kontakt mit den Infektionserregern zu minimieren (vergleiche Abschnitt Risikogruppe nach Biostoffverordnung). Kartuschentests, auch als engl. panel bezeichnet, werden seit 2018 für die Diagnostik von Krankheitserregern, die Atemwegserkrankungen verursachen, eingesetzt. Die Methode basiert auch hier auf der RT-qPCR, der real-time quantitativen Reverse-Transkriptase-Polymerase-Kettenreaktion, da aber gleichzeitig Gene mehrerer Krankheitserreger analysiert werden, wird sie der Multiplex-PCR zugerechnet. ⓘ
Das Biotechnologieunternehmen Qiagen N.V. entwickelte am Standort in Hilden einen Kartuschentest als Schnelltest, der auf einem bereits international für die Diagnostik von Krankheitserregern zugelassenen Verfahren basiert, mit dem sich u. a. SARS-assoziierte Viren und EHEC nachweisen lassen. Das Verfahren wurde um den Nachweis der im SARS-CoV-2-Genom vorhandenen Gene ORF1b und E erweitert und die Ergebnisse wurden mit denen der RT-PCR-Methode verglichen. Das Unternehmen arbeitete mit der WHO zusammen, um eine Validierung zu erreichen. Das tragbare Diagnosegerät ist für den Einsatz in Arztpraxen oder an Flughäfen geeignet. Als Probenmaterial ist ein Abstrich aus dem Rachenraum oder eine Blutprobe geeignet, Testergebnisse liegen innerhalb von 60 Minuten vor. In Deutschland ist die vorläufige Zulassung durch das Bundesinstitut für Arzneimittel und Medizinprodukte beantragt. Die Diagnosegeräte wurden im Februar 2020 in französischen und chinesischen Krankenhäusern getestet und erhielten die Zulassung der US-amerikanischen und europäischen Behörden (Stand 27. März 2020). Im Vergleich zur routinemäßig eingesetzten RT-qPCR-Methode sind Kartuschentests teurer, zudem wird das dazugehörige Analyse-Gerät benötigt. ⓘ
Zwei weitere Diagnostik-Firmen in Deutschland entwickeln ebenfalls derartige Schnelltests. Die US-amerikanische Firma Cepheid Inc hat im März 2020 eine beschleunigte Zulassung durch die FDA erhalten. Auch hier handelt es sich um ein Kartuschensystem auf der Basis von RT-qPCR mit dazugehörigem Analyzer, Testergebnisse sollen nach 45 Minuten vorliegen. Von den passenden Analyse-Geräten werden zurzeit weltweit etwa 23.000 verwendet, zumeist in Krankenhäusern, ein Analyzer kann bis zu vier Kartuschen gleichzeitig aufnehmen (Stand 27. März 2020). Die Robert Bosch GmbH entwickelte zusammen mit der britischen Firma Randox Laboratories ebenfalls einen Kartuschentest, mit dem Testergebnisse nach 2,5 Stunden vorliegen sollen. Das Testsystem kam im April 2020 auf den Markt, zuerst nur mit einer Zulassung für Forschungseinrichtungen. Im September 2020 wurde eine verkürzte Analyszeit von 39 Minuten veröffentlicht; im Dezember 2020 eine Zeit von unter 30 Minuten. ⓘ
Zellkultur
Die Vermehrung des Virus zu Forschungszwecken in einer Zellkultur ist unter anderem in China, Australien, Frankreich, Deutschland und den USA gelungen. Die chinesischen Wissenschaftler verwenden hierbei Epithelzellen des menschlichen Atemtrakts, die das mehrschichtige mukoziliäre Epithelgewebe (Flimmerepithel) simulieren, ebenso werden die Zelllinien Vero E6 und Huh-7 (isoliert aus humanem Leberkarzinom) eingesetzt. ⓘ
Deutschland
Der Erregernachweis sowie Krankheits- und Todesfälle in Bezug auf COVID-19 sind seit dem 1. Februar 2020 meldepflichtig (§ 6 Abs. 1 Satz 1 Nr. 1 lit. t, § 7 Abs. 1 Satz 1 Nr. 44a IfSG). Zur Testung von Patienten auf Infektion mit dem neuartigen Coronavirus SARS-CoV-2 hat das Robert Koch-Institut gem. § 4 Abs. 2 Nr. 1 IfSG Hinweise erstellt. ⓘ
Wer wird getestet?
Einen Anspruch auf Testung haben
- symptomatische Personen mit Verdacht auf COVID-19 im Rahmen einer ambulanten Kranken- oder Krankenhausbehandlung (§ 27, § 39 SGB V)
- asymptomatische Personen nach der Coronavirus-Testverordnung (§ 1 Abs. 3 TestV):
- nachweislich infizierte Personen in Absonderung und Personen, die in den letzten 14 Tagen Kontakt zu einer mit dem Coronavirus SARS-CoV-2 infizierten Person hatten (Kontaktpersonen) einschließlich Personen, die über die Corona-Warn-App des Robert Koch-Instituts eine Warnung mit der Statusanzeige erhöhtes Risiko erhalten haben (§ 2 TestV)
- Bewohner, Personal und Besucher bestimmter Einrichtungen wie Krankenhäuser und Altenheime (§ 3, § 4 TestV)
- Bürgertestung (PoC-Antigen-Test), § 4a TestV
- bestätigende Diagnostik und variantenspezifische PCR-Testung nach einem positiven Bürgertest oder Antigen-Test in Eigenanwendung (§ 4b TestV). ⓘ
Einen Testnachweis vorlegen müssen
- Personen, die das sechste Lebensjahr vollendet haben, in die Bundesrepublik Deutschland einreisen und nicht genesen oder geimpft sind (§ 5 Abs. 1 Coronavirus-Einreiseverordnung) sowie Personen, die sich zu einem beliebigen Zeitpunkt in den letzten zehn Tagen vor der Einreise in die Bundesrepublik Deutschland in einem Virusvariantengebiet aufgehalten haben, auch wenn sie genesen oder geimpft sind (§ 5 Abs. 2 CoronaEinreiseV, § 2 Nr. 17 IfSG)
- Personen, für die bei Vorlage eines negativen Testnachweises Ausnahmen und Erleichterungen von Coronaschutz-, Quarantäne- und Absonderungsverordnungen der Länder vorgesehen sind (3G-Regel). ⓘ

Testdokumentation
Die Durchführung oder Überwachung einer Testung in Bezug auf einen Erregernachweis des Coronavirus SARS-CoV-2 ist schriftlich zu dokumentieren. ⓘ
Bei einem positiven Erregernachweis erfolgt eine Genesenendokumentation (§ 22 Abs. 4a IfSG), bei einem negativen eine Testdokumentation (§ 22 Abs. 4c IfSG). ⓘ
Die Testdokumentation muss gem. § 22 Abs. 4d IfSG zu jeder Testung folgende Angaben enthalten:
- Datum der Testung,
- Name der getesteten Person und deren Geburtsdatum sowie Name und Anschrift der zur Durchführung oder Überwachung der Testung befugten Person,
- Angaben zur Testung, einschließlich der Art der Testung. ⓘ
Auf Wunsch der betroffenen Person ist die Testung zusätzlich in einem digitalen Zertifikat in Form eines QR-Codes zu bescheinigen (§ 22a Abs. 7 IfSG). ⓘ
Testnachweis bei COVID-19
Seit dem 19. März 2022 ist in § 22a Abs. 3 IfSG legaldefiniert, welche Voraussetzungen ein Testnachweis erfüllen muss. ⓘ
Ein Nachweis hinsichtlich des Nichtvorliegens einer Infektion mit dem Coronavirus SARS-CoV-2 muss danach durch In-vitro-Diagnostika erfolgen, die für den direkten Erregernachweis des Coronavirus SARS-CoV-2 bestimmt oder auf Grund ihrer CE-Kennzeichnung oder auf Grund einer gemäß § 11 Abs. 1 des Medizinproduktegesetzes erteilten Sonderzulassung verkehrsfähig sind, die zugrundeliegende Testung maximal 24 Stunden zurückliegt und
- vor Ort unter Aufsicht desjenigen stattgefunden hat, der der jeweiligen Schutzmaßnahme unterworfen ist,
- im Rahmen einer betrieblichen Testung im Sinne des Arbeitsschutzes durch Personal erfolgt ist, das die dafür erforderliche Ausbildung oder Kenntnis und Erfahrung besitzt, oder
- von einem Leistungserbringer nach § 6 Abs. 1 TestV vorgenommen oder vor Ort überwacht worden ist. ⓘ
Vor-Ort-Testungen können als Selbsttests mit dazu geeigneten, marktfähigen Antigenschnelltests unter Aufsicht durchgeführt werden, um bei Vorliegen eines negativen Ergebnisses eine Zugangsberechtigung im Sinne eines Testnachweises zu dem Ort zu erhalten, an dem die Testung erfolgt, wie Pflegeeinrichtungen, Restaurants, Veranstaltungsstätten, Sportstudios und Arbeitsstätten. Testnachweise für Antigenschnelltests, die unter Aufsicht oder in Eigenanwendung etwa von Pflegepersonal durchgeführt wurden, sind jedoch in ihrer Gültigkeit auf den Ort der Testung beschränkt und berechtigen nicht zum Zugang zu anderen Orten oder Einrichtungen. In diesem Zusammenhang dürfen daher anders als bei betrieblichen Testungen oder Tests durch Leistungserbringer nach der TestV auch keine Testnachweise ausgestellt werden, die auch in anderen 3G-Kontexten verwendet werden können. ⓘ